-
地壳中含量最多的金属元素是( )
A.氧 B.硅 C.铝 D.铁
难度: 简单查看答案及解析
-
下列符号中,表示2个氢原子的是( )
A.H2 B.2H C.2H+ D.2H2
难度: 中等查看答案及解析
-
下列变化属于化学变化的是( )
A.榨取果汁 B.海水晒盐 C.食物变质 D.冰雪融化
难度: 中等查看答案及解析
-
在空气的成分中,体积分数约占78%的是( )
A.氮气 B.氧气 C.二氧化碳 D.稀有气体
难度: 简单查看答案及解析
-
能保持氧气化学性质的粒子是( )
A.O B.2O C.O2 D.O2﹣
难度: 中等查看答案及解析
-
下列物质中,属于纯净物的是( )
A.食醋 B.果汁 C.牛奶 D.蒸馏水
难度: 中等查看答案及解析
-
日常生活中见到的“加碘食盐”、“高钙牛奶”中的“碘、钙”应理解为( )
A.原子 B.元素 C.离子 D.分子
难度: 中等查看答案及解析
-
香烟烟气中能与血红蛋白结合的有毒气体是( )
A.氮气 B.氧气 C.二氧化碳 D.一氧化碳
难度: 中等查看答案及解析
-
下列物质中,属于溶液的是( )
A.糖水 B.牛奶 C.米粥 D.豆浆
难度: 中等查看答案及解析
-
决定元素种类的是原子的( )
A.质子数 B.中子数 C.电子数 D.最外层电子数
难度: 简单查看答案及解析
-
合格碘盐是在食盐中加入碘酸钾(KIO3),碘酸钾中碘元素的化合价是( )
A.+2 B.+3 C.+4 D.+5
难度: 中等查看答案及解析
-
下列数据为常见水果的近似pH,其中呈碱性的是( )




A.杨梅pH=2.5 B.苹果pH=4.1 C.菠萝pH=5.1 D.柿子pH=8.5
难度: 简单查看答案及解析
-
农作物缺钾时,抗病虫害和抗倒伏能力降低,此时应该施用的化肥是( )
A.KCl B.Ca3(PO4)2 C.NH4Cl D.CO(NH2)2
难度: 中等查看答案及解析
-
硒元素被誉为“抗癌大王”,它在元素周期表中的信息如图所示.对图中信息解释不正确的是( )
A.原子序数为“34” B.元素名称为“硒”
C.元素符号为“Se” D.核电荷数为“78.96”
难度: 中等查看答案及解析
-
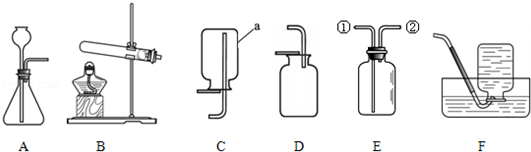
下列实验操作中,正确的是( )
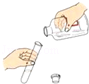



A.倾倒液体 B.称量固体 C.取用固体粉末 D.点燃酒精灯
难度: 简单查看答案及解析
-
下列物质溶于水时,溶液温度明显降低的是( )
A.氯化钠 B.氢氧化钠 C.浓硫酸 D.硝酸铵
难度: 简单查看答案及解析
-
下列化学方程式书写正确的是( )
A.C+O2═CO2
B.4P+5O2
2P2O5
C.H2SO4+NaOH═NaSO4+H2O
D.2Fe+6HCl═2FeCl3+3H2↑
难度: 中等查看答案及解析
-
下列物质的应用中,利用物理性质的是( )
A.氧气用于气焊 B.一氧化碳用作燃料
C.干冰用作制冷剂 D.用氢氧化钙中和硫酸厂的废酸液
难度: 中等查看答案及解析
-
下列做法中,不正确的是( )
A.用燃烧法识别羊毛和合成纤维
B.用甲醛溶液浸泡海产品进行保鲜
C.保护金属资源的有效途径之一是将废旧金属回收
D.解决水污染的有效途径之一是农业上合理施用化肥和农药
难度: 中等查看答案及解析
-
铝可与碱溶液发生反应:2Al+2NaOH+2H2O=2NaAlO2+3X↑,关于此反应的叙述不正确的是( )
A.X的化学式为H2
B.NaAlO2属于氧化物
C.此反应不属于复分解反应
D.铝锅不宜长时间盛放碱性食品
难度: 中等查看答案及解析
-
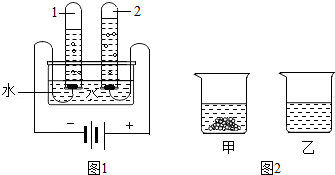
甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是( )
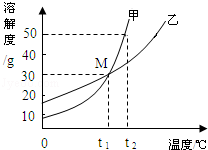
A.t1℃时,甲、乙各30g分别加入70g水中均恰好完全溶解
B.t1℃时,甲、乙两物质形成的溶液溶质的质量分数相等
C.t2℃时,在l00g水中放入60g甲,所得溶液溶质的质量分数为37.5%
D.t2℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和
难度: 困难查看答案及解析
-
下列实验方案中,能达到实验目的是( )
选项 实验目的 实验方案
A 除去CaO中的CaCO3 加足量稀盐酸,过滤
B 检验一瓶气体是否为二氧化碳 将燃着的木条伸入瓶中,观察是否熄灭
C 除去氯化钠固体中的少量碳酸钠 加入适量稀盐酸,充分反应后,蒸发
D 鉴别氯化钠溶液、氢氧化钠溶液和稀盐酸 各取少量溶液于试管中,分别滴加无色酚酞溶液,观察溶液颜色的变化
难度: 中等查看答案及解析
-
在一定条件下,反应物的溶液中溶质质量分数越大,化学反应速率越快.现有100g溶质质量分数为27%的硫酸溶液与足量的锌粒反应,为了减缓化学反应的速率,而又不影响生成氢气的总质量,可向该溶液中加入适量的( )
A.水 B.盐酸溶液 C.碳酸钠溶液 D.氢氧化钠溶液
难度: 中等查看答案及解析
-
在点燃条件下,M和N反应生成X和Y.反应前后分子变化的微观示意图如下所示(其中“
”代表氢原子,“
”代表碳原子,“
”代表氧原子).下列叙述中,不正确的是( )
物质
M
N
X
Y
微观示意图
A.生成物均为氧化物
B.在该反应中,生成X和Y的质量比为9:22
C.M中碳、氢、氧三种元素的质量比为12:3:8
D.在该反应中,M和N两种物质的分子个数比为1:3
难度: 困难查看答案及解析
-
下列实验内容符合如图所示变化趋势的是( )
序号
实验内容
横坐标表示的量
纵坐标表示的量
①
过量红磷测定空气中氧气含量
时间
红磷的质量
②
过氧化氢溶液与二氧化锰制氧气
时间
二氧化锰的质量
③
向铜、锌混合物粉末中加入盐酸
加入盐酸的质量
剩余固体的质量
④
向硝酸钾饱和溶液中加入水
加入水的质量
溶质的质量分数
A.①② B.①③ C.②③ D.③④
难度: 困难查看答案及解析
-
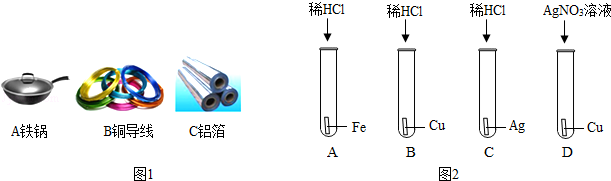
化学与生活息息相关.
(1)下列物品中能提供丰富蛋白质的是 (填字母序号,下同);属于有机合成材料的是 .

(2)微量元素对人体健康的影响很大,如缺 元素会引起贫血.
(3)煤、 、天然气称为化石燃料.天然气的主要成分为甲烷,甲烷在空气中燃烧的化学方程式为 ________ .化石燃料燃烧会加剧温室效应.下列做法符合低碳生活理念的是 ________ (填字母序号).
A.分类处理并回收垃圾 B.开发和利用风能、太阳能等新能源
C.提高煤炭等燃料的利用率 D.减少汽车的使用率,提倡绿色出行.
难度: 中等查看答案及解析