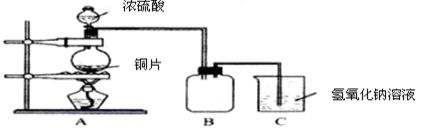
-
下列做法不能减少大气污染的是( )
A.大力发展清洁能源,烟气脱硫 B.大力发展私家车,减少公共交通
C.利用太阳能、风能等替代化石能源 D.多使用电动车和自行车
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.纯碱是碱 B.食盐是盐 C.王水是水 D.干冰是冰
难度: 简单查看答案及解析
-
标况下,两个等体积的干燥圆底烧瓶中分别充满:①NH3 ②NO2,进行喷泉实验。下列说法正确的是( )
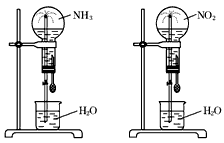
A.最终液体均能充满烧瓶
B.若在烧杯中的水中滴加酚酞,均能看到美丽的红色喷泉
C.实验结束后,烧瓶中的溶液的浓度均约为0.045mol/L
D.喷泉的原理均是气体极易溶于水,使烧瓶内的压强减小
难度: 中等查看答案及解析
-
将含有m ml NO和n ml NO2气体的量筒倒立于水槽中,然后通入m ml O2, 则充分反应后量筒内气体的体积可能为( )
①
ml ②
ml ③ 0 ml ④
ml ⑤
ml
A.①②③ B.①④⑤ C.①②⑤ D.③④⑤
难度: 中等查看答案及解析
-
下列溶液中通入SO2一定不会产生沉淀的是( )
A.Ba(OH)2 B.Ba(NO3)2 C.Na2S D.BaCl2
难度: 简单查看答案及解析
-
下列有关试剂的保存方法,错误的是( )
A.浓HNO3保存在无色玻璃试剂瓶中
B.NaOH溶液保存在具有橡皮塞的玻璃试剂中瓶中
C.少量的钠保存在煤油
D.新制的氯水通常保存在棕色玻璃试剂瓶中
难度: 中等查看答案及解析
-
标准状况下,1体积水吸收560体积氨气,得到的氨水的密度是0.91g/mL,该氨水的物质的量浓度约是( )
A.4 mol /L B.8 mol / L C.10 mol /L D.16 mol / L
难度: 中等查看答案及解析
-
下列各组离子中,能大量共存的是( )
A.K+、Cl-、CO32+、Ca2+ B.H+、Fe2+、NO3-、Na+
C.NH4+、SO42-、K+、OH- D.Na+、NH4+、Cl-、NO3-
难度: 中等查看答案及解析
-
向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
操作
现象
结论
A
滴加BaCl2溶液
生成白色沉淀
原溶液中有SO42-
B
加氯水和CCl4,振荡、静置
下层溶液显紫色
原溶液中有I-
C
用洁净铂丝蘸取溶液进行焰色反应
火焰呈黄色
原溶液中有Na+无K+
D
滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口
试纸不变蓝
原溶液中无 NH4+
难度: 中等查看答案及解析
-
下列离子方程式的书写正确的是( )
A.实验室用大理石和稀盐酸制取CO2:2H++CO32- = CO2↑+H2O
B.过量的铁和稀硝酸反应:Fe+2H+ = H2↑+Fe2+
C.NH4HCO3溶液中加入过量的NaOH溶液并加热:NH4++OH-
NH3↑+H2O
D.NaHCO3溶液与NaOH溶液反应:OH-+ HCO3-= CO32-+H2O
难度: 中等查看答案及解析
-
两种大气污染物NO2和SO2在一定条件下可以发生如下反应:NO2+ SO2=NO+SO3,在体积为V L的密闭容器中通入a molNO2和bmolSO2,反应后容器内硫原子和氧原子个数比为( )
A.3b/a B.b/2[(a+b)] C.1/3 D.3b/(a+3b)
难度: 中等查看答案及解析
-
NA表示阿伏加德罗常数的值,下列说法一定正确的是( )
A.标准状况下,2.24L氯气与足量的铁反应,转移电子数为0.2NA
B.标准状况下,2.24L NO2所含电子总数为3.9 NA
C.7.8gNa2S和Na2O2的混合物中含有的阴离子总数大于0.1 NA
D.常温常压下,将0.1mol氯气通入水中发生化学反应,转移电子数为0.1 NA
难度: 中等查看答案及解析
-
下列说法错误的是( )
A.2H2S+SO2=3S+2H2O中,氧化产物和还原产物物质的量之比为2:1
B.4Zn+10HNO3=4Zn(NO3)2+NH4NO3+3H2O中,氧化剂和还原剂物质的量之比为5:2
C.3I2+6KOH
5KI+KIO3+3H2O中,被氧化和被还原的碘元素物质的量之比为1:5
D.2FeS+6H2SO4(浓)
Fe2(SO4)3+3SO2+2S↓+6H2O中,反应中发生氧化反应和发生还原反应的硫元素物质的量之比为2:3
难度: 中等查看答案及解析
-
有质量和溶质质量分数均相同的稀H2SO4溶液4瓶,分别投入足量下列物质:A瓶中加MgCO3;B瓶中加Mg(OH)2;C瓶中加MgO;D瓶中加Mg,反应后溶液中MgSO4质量分数的大小顺序是( )
A.D > B > C > A B.D > A = C > B
C.C > A = B > D D.D > A > C > B
难度: 中等查看答案及解析
-
溶质质量分数为98%的浓硫酸(ρ=1.84g/mL),其物质的量浓度为18.4mol/L,取10mL该硫酸与amL水混合,配制成溶质质量分数为49%的硫酸(ρ=1.40g/mL),其物质的量浓度为bmol/L,则a、b分别为( )
A. a>10 b<9.2 B. a<10 b>9.2
C. a=10 b=9.2 D. a>10 b=9.2
难度: 中等查看答案及解析
-
为了除去KNO3晶体中所含的CaCO3和MgSO4,先将它配成溶液,然后加入KOH、K2CO3、HNO3、Ba(NO3)2等试剂,配以过滤、蒸发结晶等操作,制成纯净的KNO3晶体。加入试剂的顺序是( )
A.Ba(NO3)2、KOH、K2CO3、HNO3 B.Ba(NO3)2、KOH、HNO3、K2CO3
C.KOH、K2CO3、Ba(NO3)2、HNO3 D.K2CO3、Ba(NO3)2、KOH、HNO3
难度: 中等查看答案及解析
-
如下图是实验室制取气体的装置。其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示。下列选项中正确的是( )
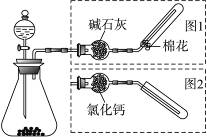
发生装置中的药品
干燥和集气装置
A
电石和水
图2
B
大理石和稀盐酸
图1
C
铜和稀硝酸
图2
D
氧化钙和浓氨水
图1
难度: 中等查看答案及解析
-
同温同压下,将NO2、NO、O2按一定的体积比充满一容器积比充满一容器,再倒置于盛水的水槽中.片刻后液体充满容器.则反应前NO2、NO、O2气体的体积比可能是( )
A.4:4:3 B.4:3:1 C.4:24:19 D.4:14:7
难度: 中等查看答案及解析
-
某氧化还原反应的离子方程式的已知部分为:2口+5口+口H+=5口+2口十8口
若对应于上述离子方程式的电子转移总数为10,则反应物和生成物对应正确的是( )
序号
氧化剂
还原剂
其它反应物
氧化产物
还原产物
A
Cl2
FeBr2
FeCl3
/
FeCl3、Br2
B
KMnO4
H2O2
H2SO4
O2
MnSO4
C
KClO3
HCl(浓)
/
Cl2
Cl2
D
KMnO4
HCl(浓)
/
Cl2
MnCl2
难度: 中等查看答案及解析
-
足量的铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol/LNaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是 ( )
A.60mL B.45mL C.30mL D.15mL
难度: 中等查看答案及解析