-
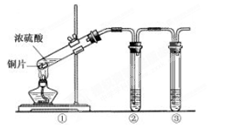
用铜锌合金制成的假金元宝欺骗行人的事件屡有发生。下列不易区分真伪的方法是
A. 在空气中加热 B. 放入硝酸中 C. 放入盐酸中 D.观察外观
难度: 简单查看答案及解析
-
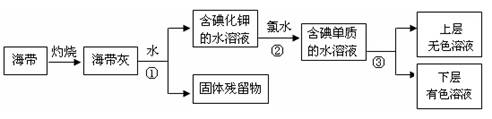
为了消除碘缺乏病,我国政府规定在食用盐中加入一定量的
A.碘(I2) B. 碘化钾(KI) C.碘酸钾(KIO3) D.高碘酸钾(KIO4)
难度: 简单查看答案及解析
-
下列反应的离子方程式正确的是
A.FeCl3溶液中加入铁粉:Fe3++Fe=2Fe2+
B.钠和水反应:Na+H2O =Na++OH-+H2↑
C.硫酸溶液中滴加氢氧化钡溶液:Ba2++SO42-=BaSO4 ↓
D.向烧碱溶液中滴加盐酸:OH-+H+=H2O
难度: 简单查看答案及解析
-
下列说法错误的是
A.溶液、胶体和浊液这三种分散系的根本区别是分散质粒子的大小
B.NO可用排空气法进行收集
C.不可用浓硫酸干燥氨气
D.SO2 的大量排放会引起酸雨
难度: 简单查看答案及解析
-
设 NA 为阿伏加德罗常数的数值,下列说法正确的是
A.NA个CH4分子的质量为16g/mol
B.1mol/LNaCl溶液含有NA 个Na+
C.等物质的量的N2和CO所含分子数、原子个数、电子总数均相同
D.22.4LCO2中含有 NA个CO2分子
难度: 简单查看答案及解析
-
下列关于NaHCO3和Na2CO3的叙述不正确的是
A. NaHCO3比Na2CO3稳定
B. NaHCO3、Na2CO3可相互转化
C.NaHCO3 可用于焙制糕点;Na2CO3可用于玻璃、造纸等工业
D.都能与澄清石灰水反应生成白色沉淀
难度: 简单查看答案及解析
-
在下列变化①大气通过闪电固氮 ②硝酸分解 ③实验室用氯化铵和消石灰制取氨气④二氧化氮溶于水中,按氮元素被还原、被氧化、既被氧化又被还原、既不被氧化又不被还原的顺序排列,正确的是
A.②①④③ B.①②③④ C.②④①③ D.①③④②
难度: 简单查看答案及解析
-
用于区别下列各组物质的试剂错误的是
A.硝酸银溶液和硫酸钠溶液:氯化钡溶液和稀硝酸
B.浓硫酸和稀硫酸:小木条
C.NH4Cl溶液和NaCl溶液:NaOH溶液和红色石蕊试纸
D.Na2O2和硫粉:水
难度: 简单查看答案及解析
-
对下列药品或事故的处理正确的是
A.漂白粉保存在烧杯中
B.浓硝酸保存在无色透明的试剂瓶中
C.金属钠着火燃烧时用砂子灭火
D.大量氯气泄漏时用氢氧化钠溶液浸湿的软布蒙面并迅速离开现场
难度: 简单查看答案及解析
-
下列叙述不正确的是
A.Na 在空气中燃烧主要生成Na2O
B. 金刚石、石墨、C60是碳元素的同素异形体
C.NH3·H2O、CH3COOH是弱电解质
D. 当光束通过Fe(OH)3胶体时,能产生丁达尔效应
难度: 简单查看答案及解析
-
某溶液中有NH4+、Mg2+、Fe2+和Fe3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量增加的阳离子是
A. NH4+ B. Fe2+ C. Fe3+ D. Mg2+
难度: 简单查看答案及解析
-
欲除去FeCl2溶液中少量的FeCl3,可行的办法
A.滴入KSCN B.通入氯气 C.加入铁粉 D.加入铜粉
难度: 简单查看答案及解析
-
现有CO、CO2、O3(臭氧)三种气体,下列叙述不正确的是
A.同温同压同体积时质量比为7:11:12
B.相同质量时所含氧原子的物质的量之比为1:2:3
C.标况下密度比为7:11:12
D .都含有1mol氧原子时则三种气体的物质的量之比为6∶3∶2
难度: 简单查看答案及解析
-
低碳,英文为low carbon。意指较低(更低)的温室气体(二氧化碳为主)排放。下列做法不能体现低碳生活的是
A.节约纸张平时做草稿时正反面使用 B.大量使用薪柴为燃料
C.尽量购买本地的、当季的食物 D.注意节约用电做到随手关灯
难度: 简单查看答案及解析
-
下列溶液中,Na+物质的量浓度最大的是
A.1mL 0.5mol·L-1的NaNO3溶液 B.100mL 0.01mol·L-1的NaCl溶液
C.10mL 0.1mol·L-1的NaOH溶液 D.100mL 0.1mol·L-1的Na2SO4溶液
难度: 简单查看答案及解析
-
下图装置可用于
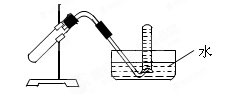
A.加热NaHCO3固体制CO2
B.Cu和稀HNO3反应制NO
C.NH4Cl与浓Ca(OH)2溶液反应制NH3
D.Cu和浓HNO3反应制NO2
难度: 简单查看答案及解析
-
下列物质的分类合理的是

难度: 简单查看答案及解析
-
将一小块金属钠投入过量的硫酸铜溶液中,主要生成物是
A. Na2SO4和Cu B. NaOH和H2
C. Cu(OH)2和H2 D. Na2SO4、Cu(OH)2和H2
难度: 简单查看答案及解析
-
将氯水滴入紫色石蕊试液、硝酸银溶液,将依次观察到紫色石蕊试液先变红后退色、有白色沉淀产生等现象。这些现象与氯水所含的下列哪种微粒无直接关系
A.HClO B.H2O C.Cl— D.H+
难度: 简单查看答案及解析
-
下列各组中的离子,能在溶液中大量共存的是:
A.K+、H+、SO42-、OH- B.Na+、Ca2+、CO32-、NO3-
C.Na+、Cu2+、Cl-、SO42- D.Na+、H+、Cl-、CO32-
难度: 简单查看答案及解析
-
下列化学反应中,属于氧化还原反应的是
A.Na2CO3+2HCl=2NaCl+CO2↑+H2O B.CaO+H2O=Ca(OH)2
C. CaCO3
CaO+CO2↑ D. 2CO +O2
2CO2
难度: 简单查看答案及解析
-
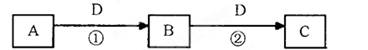
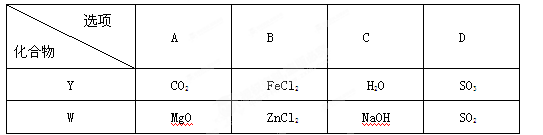
下表各选项中,不能利用置换反应通过Y得到W的一组化合物是
难度: 简单查看答案及解析