-
下列关于常见有机物的说法不正确的是( )
A.乙烯和苯都能与溴水反应
B.乙酸和油脂都能与氢氧化钠溶液反应
C.糖类和蛋白质都是人体重要的营养物质
D.乙烯和甲烷可用酸性高锰酸钾溶液鉴别难度: 中等查看答案及解析
-
下列热化学方程式书写正确的是(△H的绝对值均正确)( )
A.C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=-1367.0kJ/mol(燃烧热)
B.NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=+57.3kJ/mol(中和热)
C.S(s)+O2(g)═SO2(g);△H=-269kJ/mol(反应热)
D.2NO2═O2+NO;△H=+116.2kJ/mol(反应热)难度: 中等查看答案及解析
-
在下列各溶液中,离子一定能大量共存的是( )
A.强碱性溶液中:K+、Al3+、Cl-、SO42-
B.含有0.1mol•L-1Fe3+的溶液中:K+、Mg2+、I-、NO3-
C.含有0.1mol•L-1Ca2+溶液在中:Na+、K+、CO32-、Cl-
D.室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42-难度: 中等查看答案及解析
-
对于放热反应2H2(g)+O2(g)=2H2O(l),下列说法正确的是( )
A.产物H2O所具有的总能量高于反应物H2和O2所具有的总能量
B.反应物H2和O2所具有的总能量高于产物H2O所具有的总能量
C.反应物H2和O2所具有的总能量等于产物H2O所具有的总能量
D.反应物H2和O2比产物H2O稳定难度: 中等查看答案及解析
-
下列物质中,按只有氧化性,只有还原性,既有氧化性又有还原性的顺序排列的一组是( )
A.F2、K、HCl
B.Cl2、Al、H2
C.NO2、Na、Br2
D.O2、SO2、H2O难度: 中等查看答案及解析
-
下列各组物质的晶体中,化学键类型相同、晶体类型、物质发生状态变化所克服的粒子间的相互作用也相同的是( )
A.SO3和SiO2
B.CCl4和KCl
C.NaCl和HCl
D.CO2和H2O难度: 中等查看答案及解析
-
溶液、胶体和悬浊液这三种分散系的本质区别是( )
A.是否为大量分子或离子的集合体
B.能否透过滤纸或半透膜
C.分散质粒子的大小
D.能否产生丁达尔现象难度: 中等查看答案及解析
-
常温下,在下列溶液中发生如下反应①16H++10Z-+2XO4-→2X2++5Z2+8H2O ②2A2++B2→2A3++2B- ③2B-+Z2→B2+2Z-由此判断下列说法错误的是( )
A.反应Z2+2A2+=2A3++2Z-可以进行
B.Z元素在反应①③中均被还原
C.氧化性由强到弱的顺序是:XO4-、Z2、B2、A3+
D.还原性由强到弱的顺序是:A2+、B-、Z-、X2+难度: 中等查看答案及解析
-
下列叙述错误的是( )
A.合金材料中可能含有非金属元素
B.人造纤维,合成纤维和光导纤维都是有机高分子化合物
C.加热能杀死流感病毒是因为病毒的蛋白质受热变性
D.在汽车排气管上加装“催化转化器”是为了减少有害气体的排放难度: 中等查看答案及解析
-
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
A.CO2的电子式:
B.Cl-的结构示意图:
C.化学式NaCl既能表示物质的组成,又能表示物质的一个分子
D.质量数为37的氯原子Cl
难度: 中等查看答案及解析
-
下列说法中正确的是( )
A.离子晶体中每个离子周围均吸引着6个带相反电荷的离子
B.晶体中只要有阳离子就一定有阴离子
C.分子晶体的熔沸点很低,常温下都呈液态或气态
D.原子晶体中的各相邻原子都以共价键相结合难度: 中等查看答案及解析
-
下列反应中不属于氧化还原反应的是( )
A.3CO+Fe2O32Fe+3CO2
B.Cl2+H2O=HCl+HClO
C.CaCO3+SiO2CaSiO3+CO2↑
D.3CuS+8HNO3=3Cu(NO3)2+2NO↑+3S↓+4H2O难度: 中等查看答案及解析
-
用浓盐酸与MnO2共热制取Cl2的反应中,消耗的氯化氢的物质的量与作还原剂的氯化氢的物质的量之比是( )
A.2:1
B.4:1
C.1:1
D.1:2难度: 中等查看答案及解析
-
根据实验目的判断下列实验操作或装置正确的是( )
A. 实验室制O2
实验室制O2
B.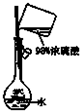 配制稀硫酸溶液
配制稀硫酸溶液
C. 在铁制品上镀铜
在铁制品上镀铜
D. 净化、精制淀粉胶体
净化、精制淀粉胶体 难度: 中等查看答案及解析
-
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C
2AlN+3CO.下列叙述正确的是( )
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2 mol AlN,N2得到3 mol电子
C.氮化铝中氮元素的化合价为-3
D.氮化铝晶体属于分子晶体难度: 中等查看答案及解析
-
将m1 g锌加到m2 g 20% HCl溶液中去,反应结果共放出n L氢气(在标准状况下),则被还原的HCl的物质的量是( )
A.mol
B.mol
C.mol
D.mol
难度: 中等查看答案及解析
-
设阿伏加德罗常数(NA)的数值为nA,下列说法正确的是( )
A.1molCl2与足量H2反应,形成的共价数为nA
B.0.5molNa2O2中含有的质子总数为19nA
C.常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3nA
D.标准状况下,11.2L的SO3所含分子数为0.5nA难度: 中等查看答案及解析
-
下列化合物,按其晶体的熔点由高到低排列正确的是( )
A.金刚石晶体SiNaMg
B.SiO2CsClCBr4CF4
C.HIHBrHClHF
D.CsClRbClKClNaCl难度: 中等查看答案及解析
-
下列反应的离子方程式正确的是( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3↓+3H+
B.用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O
C.实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-═Cl2↑+Mn2++H2O
D.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu═Fe2++Cu2+难度: 中等查看答案及解析
-
元素X的单质及X与Y形成的化合物能按如图所示的关系发生转化.则X为( )
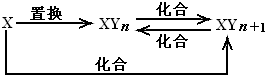
A.当n=1时,X可能是Mg
B.当n=1时,X可能是N2
C.当n=2时,X可能是S
D.当n=2时,X可能是Fe难度: 中等查看答案及解析
-
一种从植物中提取的天然化合物α-damascone可用于制作香水,其结构为:
,有关该化合物的下列说法不正确的是( )
A.分子式为C13H20O
B.该化合物可发生聚合反应
C.1mol该化合物完全燃烧消耗19 mol O2
D.与Br2的CCl4溶液反应生成的产物经水解、稀硝酸酸化后可用AgNO3溶液检验难度: 中等查看答案及解析
-
市场上经常见到的标记为Li-ion的电池称为“锂离子电池”.它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料.这种锂离子电池的电池反应式为:Li+2Li0.35NiO2
2Li0.85NiO2.下列说法不正确的是( )
A.放电时,负极的电极反应式:Li-e-=Li+
B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中Li+向负极移动难度: 中等查看答案及解析