-
三峡电厂发电量可提供相当于每年0.5亿吨原煤的火力发电厂产生的电能,从而有助于控制( )
①白色污染 ②酸雨的形成 ③臭氧空洞扩大 ④温室效应 ⑤三峡库区水质的富营养化
A.②④ B.③④ C.①②④ D.①②⑤
难度: 简单查看答案及解析
-
下列过程中,需要增大化学反应速率的是( )
A.钢铁腐蚀 B.食物腐败 C.塑料老化 D.工业合成氨
难度: 中等查看答案及解析
-
下列关于化学变化的叙述错误的是( )
A.化学变化一定伴随能量变化
B.化学变化一定有化学键的断裂和生成
C.化学变化一定伴随物质的状态变化
D.化学变化一定有新物质生成
难度: 中等查看答案及解析
-
在宾馆、办公楼等公共场所,常使用一种电离式烟雾报警器,其主体是一个放有镅﹣241(
Am)放射源的电离室.
Am原子核内中子数与核外电子数之差是( )
A. 241 B. 146 C. 95 D. 51
难度: 中等查看答案及解析
-
下列物质属于含有共价键的离子化合物的是( )
A.MgCl2 B.Na2O2 C.K2O D.H2O2
难度: 中等查看答案及解析
-
下列叙述中错误的是( )
A. 原子半径:Cl>S>O B. 还原性:Na>Mg>Al
C. 稳定性:HF>HCl>HBr D. 酸性:HClO4>H2SO4>H3PO4
难度: 中等查看答案及解析
-
10ml浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的下列物质,能加快反应速率但又不影响氢气生成的是( )
A.KNO3 B.CH3COONa C.CuSO4 D.Na2CO3
难度: 中等查看答案及解析
-
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )
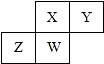
A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:X>W>Z
C. 最简单气态氢化物的热稳定性:Y>X>W>Z
D. 元素X、Z、W的最高化合价分别与其主族序数相等
难度: 中等查看答案及解析
-
把500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A.
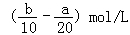
B.
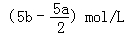
C.(2b﹣a)mol/L
D.(10b﹣5a)mol/L
难度: 困难查看答案及解析
-
下列制备和收集气体的实验装置合理的是( )

A.装置①:用氯化铵和氢氧化钙制NH3
B.装置②:收集NO气体
C.装置③:用锌粒和稀硫酸制H2
D.装置④:用双氧水和二氧化锰制O2
难度: 中等查看答案及解析
-
有A、B、C、D、E五种金属元素.在相同条件下,B元素的最高价氧化物对应水化物的碱性比A的弱;A、B单质均可以从C盐溶液中置换出C;D单质可以与冷水剧烈反应并放出氢气;A、B、C、E四种单质分别投入盐酸中,只有E不放出氢气.则五种金属元素的金属性由强到弱的顺序为( )
A.D>B>A>C>E B.D>A>B>C>E
C.A>B>C>E>D D.D>E>B>A>C
难度: 中等查看答案及解析
-
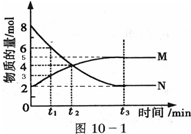
在一定温度下,体积不变的密闭容器中,可逆反应X(g)+3Y(g)
2Z(g)达到平衡的标志是( )
A.气体总质量保持不变
B.气体密度保持不变
C.X、Y、Z的物质的量不再发生变化
D.X、Y、Z的分子数之比为1:3:2
难度: 中等查看答案及解析
-
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )
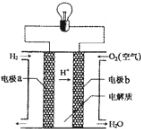
A.该电池工作时电能转化为化学能
B.该电池中电极a是正极
C.外电路中电子由电极a通过导线流向电极b
D.该电池的总反应:H2+O2=H2O
难度: 中等查看答案及解析
-
下列有关反应能量变化图象的判断错误的是( )

A.Ⅰ可表示需加热的放热反应
B.Ⅱ可表示需加热的放热反应
C.Ⅲ可表示爆炸反应
D.Ⅳ可表示醋酸和碱的中和反应
难度: 中等查看答案及解析
-
在通常条件下,NO2和SO2可以很容易发生反应生成NO和SO3.现将碳跟浓硫酸共热产生的气体X和碳跟浓硝酸共热产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )

A.洗气瓶中产生的沉淀是碳酸钡
B.洗气瓶中产生的沉淀是硫酸钡
C.在Z导管出来的气体中无二氧化碳
D.反应一段时间后洗气瓶中溶液的酸性减弱
难度: 困难查看答案及解析
-
将6molA气体和3molB气体在2L的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g)
2C(g),若经3s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应的平均速率为0.2 mol·(L·s)-1
②用物质B表示的反应的平均速率为0.2mol·(L·s)-1
③3 s时物质B的转化率为10%
④3 s时物质B的浓度为2.7 mol·L-1 其中正确的是( )
A.①③ B.①④ C. ①② D.③④
难度: 困难查看答案及解析