-
关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水.这些叙述中正确的是( )
A.①②③④
B.②③
C.①②④
D.②③④难度: 中等查看答案及解析
-
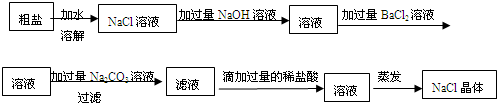
下列除去杂质的方法,正确的是( )
A.除去N2中的少量O2:通过灼热的CuO粉末,收集气体
B.除去CO2中的少量HCl:通入Na2CO3溶液,收集气体
C.除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤
D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤难度: 中等查看答案及解析
-
关于同温同压下等体积的CO2和CO,下列叙述:①质量相等;②密度相等;③所含分子数相等;④所含碳原子数相等,其中正确的是( )
A.①②③④
B.②③④
C.③④
D.③难度: 中等查看答案及解析
-
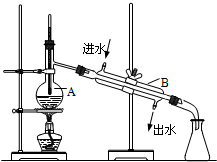
某同学用CCl4 从碘水中提取碘,下面对此实验的有关操作的描述中,错误的是( )
A.碘水和CCl4加入分液漏斗中后,塞上上口部的塞子,用右手压住分液漏斗上口部,左手握住活塞部分,把分液漏斗倒转过来振荡
B.静置,待分液漏斗中液体分层后,先使分液漏斗内外空气相通(准备放出液体)
C.打开分液漏斗的活塞,使下层液体沿承接液体的烧杯内壁慢慢流出
D.最后继续打开活塞,另用容器承接并保存上层液体难度: 中等查看答案及解析
-
下列实验中均需要的仪器是( )
①配制一定物质的量浓度的溶液 ②使用pH试纸测溶液的pH值 ③过滤 ④蒸发.
A.试管
B.胶头滴管
C.玻璃棒
D.漏斗难度: 中等查看答案及解析
-
如图所示,若用1L水来代表地球上的总水量,要比较精确地量取地球上的淡水量,应选择的仪器是( )

A.100mL烧杯
B.50mL烧杯
C.100mL量筒
D.50mL量筒难度: 中等查看答案及解析
-
如图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是( )
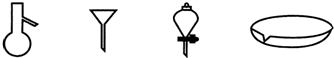
A.蒸馏、蒸发、萃取、过滤
B.萃取、过滤、蒸馏、蒸发
C.蒸馏、过滤、萃取、蒸发
D.过滤、蒸发、萃取、蒸馏难度: 中等查看答案及解析
-
下列实验操作和处理方法可能会引发安全事故的是( )
①将水沿着烧杯内壁缓慢加入浓硫酸中,并用玻璃棒不断搅拌
②给试管中的液体加热时,试管口不朝向任何人
③夜间厨房发生煤气泄漏时,立即开灯检查煤气泄漏原因,并打开所有门窗通风
④酒精灯不慎打翻起火,立即用水浇灭.
A.①②③
B.①③④
C.②③④
D.①②③④难度: 中等查看答案及解析
-
若某原子的摩尔质量为M g•mol-1,则一个该原子的真实质量是( )
A.Mg
B.g
C.g
D.g
难度: 中等查看答案及解析
-
下列有关气体体积的叙述中,正确的是( )
A.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子的大小决定
B.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子数决定
C.不同的气体若体积不同,则它们所含的分子数也不同
D.气体摩尔体积是指1mol任何气体所占的体积约为22.4L难度: 中等查看答案及解析
-
只给出下列甲和乙中对应的物理量,不能求出物质的量的是( )
A.甲:物质的质量;乙:物质的摩尔质量
B.甲:标准状况下的气体摩尔体积;乙:标准状况下的气体的体积
C.甲:固体的体积;乙:固体的密度
D.甲:溶液中溶质的物质的量浓度;乙:溶液体积难度: 中等查看答案及解析
-
某固态非金属单质A和氧气发生化合反应生成B(B为气体),在同温同压的条件下,气体B的体积是反应掉氧气体积的两倍.以下对B的分子组成的推测一定正确的是( )
A.有1个氧原子
B.有2个氧原子
C.有1个A原子
D.有2个A原子难度: 中等查看答案及解析
-
下列说法中正确的是( )
A.标准状况下,22.4L水中所含的分子数约为6.02×1023
B.标准状况下,aL的氧气和氮气的混合物含有的分子数约为×6.02×1023
C.常温常压下,48gO3气体含有的氧原子数为6.02×1023
D.2.24LCO2中含有的原子数为0.3×6.02×1023难度: 中等查看答案及解析
-
VL Fe2(SO4)3溶液中含有Fe3+mg,则溶液中SO42-的物质的量浓度为( )
A.mol/L
B.mol/L
C.mol/L
D.mol/L
难度: 中等查看答案及解析
-
20gA物质和14gB物质恰好完全反应,生成8.8gC物质、3.6gD物质和0.2molE物质,则E物质的摩尔质量为( )
A.100g/mol
B.108g/mol
C.55g/mol
D.96g/mol难度: 中等查看答案及解析
-
在某温度下,NaOH的溶解度为20g,该温度下将80gNaOH投入220g水中,充分搅拌后,测得溶液的密度为1.2g/mL,则该溶液中溶质的物质的量浓度为( )
A.0.02mol/L
B.2.0mol/L
C.5.0mol/L
D.7.5mol/L难度: 中等查看答案及解析