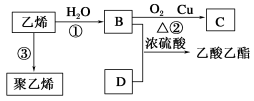
-
把①蔗糖,②淀粉,③纤维素,④乙酸乙酯在稀硫酸存在下分别进行水解,最终产物只有1种的是
A.①和② B.只有③ C.只有④ D.只有②和③
难度: 简单查看答案及解析
-
下列有关工业生产的叙述不正确的是
A.用海水淡化后的浓缩海水作原料提取溴
B.在太阳能资源相对充足的沿海地区建造海水淡化厂
C.利用“海水→氯化钠→金属钠→氢氧化钠”的工艺流程生产烧碱
D.利用“海水→氢氧化镁→氯化镁→金属镁”的工艺流程生产金属镁
难度: 中等查看答案及解析
-
向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时,按正反应速率由大到小排列顺序正确的是
甲 500 ℃,10 mol SO2和5 mol O2的反应
乙 500 ℃,用V2O5作催化剂,10 mol SO2和5 mol O2的反应
丙 450 ℃,8 mol SO2和5 mol O2的反应
丁 500 ℃,8 mol SO2和5 mol O2的反应
A.甲、乙、丙、丁 B.乙、甲、丁、丙
C.乙、甲、丙、丁 D.丁、丙、乙、甲
难度: 中等查看答案及解析
-
下列变化不是化学变化的是
A.在蛋白质溶液中,加入饱和硫酸铵溶液,有沉淀析出
B.皮肤不慎沾上浓硝酸而呈黄色
C.在蛋白质溶液中加入硫酸铜溶液,有沉淀析出
D.用稀释的福尔马林溶液浸泡植物种子
难度: 中等查看答案及解析
-
下列关于常见有机物的说法不正确的是
A.乙酸和油脂都能与NaOH溶液反应
B.蛋白质、纤维素、蔗糖、油脂都是高分子化合物
C.淀粉水解与纤维素水解得到的最终产物相同
D.乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别
难度: 中等查看答案及解析
-
由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是
A.②④⑤③① B.③②④①⑤ C.③④②⑤① D.②④③⑤①
难度: 中等查看答案及解析
-
有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验
装置
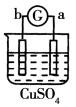
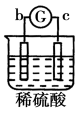
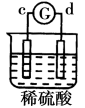
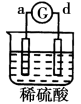
部分实验现象
a极质量减小b极质量增加
溶液中的SO42-向b极移动
d极溶解c极有气体产生
电流从a极流向d极
由此可判断这四种金属的活动性顺序是
A. a>b>c>d B. b>c>d>a C. d>a>b>c D. a>b>d>c
难度: 困难查看答案及解析
-
下列叙述中正确的是
A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B.除短周期外,其他周期均有18种元素
C.副族元素中没有非金属元素
D.碱金属元素是指IA族的所有元素
难度: 中等查看答案及解析
-
卤素是最活泼的一族非金属,下列关于卤族元素的说法正确的是
A.卤素单质的最外层电子数都是7
B.从上到下,卤素原子的电子层数依次增多,半径依次减小
C.从F到I原子核对最外层电子的吸引能力依次减弱,原子得电子能力依次减弱
D.卤素单质与H2化合的容易程度为F2<Cl2<Br2<I2
难度: 中等查看答案及解析
-
钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2===2Fe(OH)2。以下说法正确的是
A.负极发生的反应为:Fe-2e-===Fe2+
B.正极发生的反应为:2H2O+O2+2e-===4OH-
C.原电池是将电能转变为化学能的装置
D.钢柱在水下部分比在水面处更容易腐蚀
难度: 困难查看答案及解析
-
下列装置中,都伴随有能量变化,其中是由化学能转变为电能的是


难度: 简单查看答案及解析
-
少量铁粉与100 mL 0.01 mol/L的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O ②加NaOH固体③滴入几滴浓盐酸 ④加CH3COONa固体 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10 mL 0.1 mol/L盐酸
A、①⑥⑦ B、③⑤⑧ C、③⑦⑧ D、⑤⑦⑧
难度: 中等查看答案及解析
-
一定条件下,在体积为1 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g) +Y(g)
Z(g),下列叙述能证明该反应已达到化学平衡状态的是
A.X的百分含量不再发生变化
B.c(X):c(Y):c(Z)=2:1:1
C.容器内原子总数不再发生变化
D.同一时间内消耗2n mol X的同时生成n mol Z
难度: 困难查看答案及解析
-
2SO2(g)+O2(g)
2SO3(g)的反应中,经过一段时间后,SO3的浓度增加了0.9mol/L,此时间内用O2表示的平均速率为0.45mol/(L·s),则这段时间是
A.1 s B.0.44 s C.2 s D.1.33 s
难度: 中等查看答案及解析
-
下列说法正确的是
A.相对分子质量相同的物质是同种物质
B.分子式相同的不同有机物一定是同分异构体
C.具有同一通式的物质属于同系物
D.同分异构现象只存在于有机物中
难度: 中等查看答案及解析
-
有机物
 与氯气发生取代反应,生成的一氯代物有
与氯气发生取代反应,生成的一氯代物有A.1种 B.2种 C.3种 D.4种
难度: 中等查看答案及解析
-
将甲苯与液溴混合加入铁粉,其反应产物可能为
①

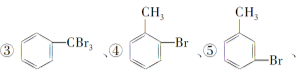

A.①②③ B.⑦ C.全部都有 D.④⑤⑥⑦
难度: 中等查看答案及解析
-
按下图装置,持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体是

A.H2 B.CO和H2
C.NH3 D.CH3CH2OH(气)
难度: 困难查看答案及解析
-
丙烯醇(CH2===CH—CH2OH)可发生的化学反应有
①加成 ②氧化 ③燃烧 ④加聚 ⑤取代
A.只有①②③ B.只有①②③④ C.①②③④⑤ D.只有①③④
难度: 中等查看答案及解析
-
初步提纯下列物质(括号内为少量杂质),选用的试剂和分离方法均正确的是
序号
物质
试剂
分离方法
①
乙酸乙酯(乙酸)
NaOH溶液
分液
②
溴苯(溴)
NaOH溶液
分液
③
乙醇(水)
生石灰
蒸馏
④
苯 (环己烷)
水
分液
A.①② B.①③ C.②③ D.④③
难度: 中等查看答案及解析
-
下列排列有错误的是
A.粒子半径:Al3+>Mg2+>Na+>F-
B.稳定性:HF>HCl>HBr>HI
C.酸性:H4SiO4<H3PO4<H2SO4<HClO4
D.碱性:Al(OH)3<Mg(OH)2<Ca(OH)2<KOH
难度: 中等查看答案及解析
-
下列有关叙述:①非金属单质M能从N的盐溶液中置换出非金属单质N;②M原子比N原子容易得到电子;③单质M形成的气态氢化物比N形成的气态氢化物稳定; ④气态氢化物水溶液的酸性HmM>HnN;⑤氧化物对应水化物的酸性HmMOx>HnNOy;⑥熔点M>N。能说明非金属元素M比N的非金属性强的是
A.②⑤ B.①②③ C.①②③⑤ D.全部
难度: 中等查看答案及解析
-
下列电子式或结构式错误的是


难度: 困难查看答案及解析
-
下列关于化学键的说法正确的是
①含有金属元素的化合物一定是离子化合物 ②第ⅠA族和第ⅦA族原子化合时,一定生成离子键 ③由非金属元素形成的化合物一定不是离子化合物 ④活泼金属与非金属化合时,能形成离子键
⑤含有离子键的化合物一定是离子化合物 ⑥离子化合物中可能同时含有离子键和共价键
A.①②⑤ B.④⑤⑥ C.①③④ D.②③⑤
难度: 困难查看答案及解析