-
下列属于物质化学性质的是
A. 导热性 B. 延展性 C. 氧化性 D. 挥发性
难度: 简单查看答案及解析
-
下列属于纯净物的是
A. 液态氧 B. 矿泉水 C. 不锈钢 D. 食用醋
难度: 简单查看答案及解析
-
下列化学用语正确的是
A. 钙离子-Ca+2 B. 氯化钾-KClO3 C. 三个氢原子—H3 D. 二氧化硅-SiO2
难度: 简单查看答案及解析
-
下列做法正确的是
A. 海鲜防腐,甲醛浸泡 B. 回收塑料,再生减污
C. 煤气泄漏,明火检查 D. 禁用农药,保护水源
难度: 简单查看答案及解析
-
下列归类不正确的是
选 项
归 类
内容
A
可燃性气体
氢气、一氧化碳、甲烷
B
人体中微量元素
铜元素、铁元素、碘元素
C
由分子构成的物质
二氧化碳、氧气、氦气
D
合金
青铜、硬铝、生铁
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
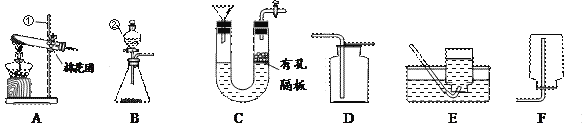
下图是“粗盐的初步提纯”实验的部分操作,其中对应操作不规范的是
A.
 甲:称量 B.
甲:称量 B. 乙:溶解
C.
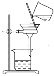 丙:过滤 D.
丙:过滤 D. 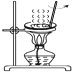 丁:蒸发
丁:蒸发难度: 简单查看答案及解析
-
下列实验方法正确的是
A. 用明矾对自水进行杀菌消毒 B. 用燃烧红磷的方法测定空气中O2的体积分数
C. 用点燃的方法除去CO2中的CO D. 用活性炭软化硬水
难度: 简单查看答案及解析
-
下列排序正确的是
A. 利用金属的年代
B. 铁元素质量分数
C. 碳元素的化合价:
D. 金属的活动性
难度: 简单查看答案及解析
-
下列对实验现象的描述或实验操作正确的是
A. 镁条在空气中燃烧,有大量黑色固体生成
B. 为加快过滤速度,用玻璃棒搅拌滤纸上的悬浊液
C. 硫酸铜溶液与氢氧化钠溶液混合 ,出现蓝色沉淀
D. 配制一定体积的稀硫酸时,将水倒入盛有浓硫酸的量筒中,并搅拌
难度: 简单查看答案及解析
-
下图是甲转化为丙的微观过程。下列说法不正确的是

A. 反应前后原子种类不变 B. 转化①中甲和O2反应的分子个数比为1:1
C. 转化②是化合反应 D. 丙中氢、硫、氧元素的质量比为1:16:32
难度: 中等查看答案及解析
-
下列指定反应的化学方程式正确的是
A. 铝的“自我保护”:2Al+3O2 === 2Al2O3
B. 铁罐不能装稀盐酸:2Fe+6HCl=2FeCl3+3H2↑
C. 用石灰石浆处理二氧化硫:SO2 + CaCO3 + O2CaSO4 +CO2
D. 证明铁的金属活动性比铜强:Fe+Cu(NO3)2 Fe(NO3)2+Cu
难度: 简单查看答案及解析
-
物质性质决定用途。下列说法不正确的是
A. 氧气具有可燃性,可用于炼钢
B. 洗洁精有乳化作用,可用于洗去碗筷上的油污
C. 氩气的化学性质稳定,可用作焊工接金属的保护气
D. 食醋具有酸性,可用于除去水壶中的水垢
难度: 简单查看答案及解析
-
下列物质的转化在给定条件下均能实现的是
A. Fe
Fe2O3
CO2 B. Cu
CuSO4
Cu(OH)2
C. H2O2
H2
H2O D. O2
CO2
CO
难度: 中等查看答案及解析
-
下列实验操作中不能达到实验目的是
选项
物质
目的
主要实验操作
A
双氧水 、蒸馏水
鉴别
取样,加二氧化锰,观察现象
B
CH4中是否含有H2
检验
点燃,罩一干冷烧杯,观察燃烧产物
C
KCl与MnO2固体混合物
分离
加水充分溶解后过滤、洗涤、烘干,蒸发
D
FeSO4溶液(CuSO4)
除杂
加过量Fe粉、过滤
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
已知:Cu2O+H2SO4═Cu+CuSO4+H2O.16.0g CuO与CO反应得到Cu、Cu2O混合物13.6g,将此混合物溶于足量的100.0g稀H2SO4得9.6gCu.下列说法正确的是( )
A. 生成2.4g CO2
B. 混合物中含9.6g铜元素
C. 混合物中Cu与Cu2O的质量之比为8:9
D. 反应后溶液中CuSO4的质量分数约为7.0%
难度: 中等查看答案及解析
-
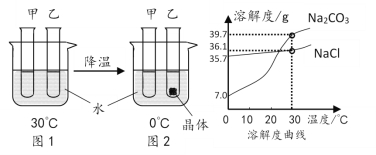
下列说法正确的是
A. 原子通过得失电子形成离子,离子一定不能形成原子
B. 不饱和溶液转化为饱和溶液,溶质的质量分数一定增大
C. 置换反应生成单质和化合物,则有单质和化合物生成的反应一定是置换反应
D. 单质中只含有一种元素,只含有一种元素的纯净物一定是单质
难度: 简单查看答案及解析
-
通常情况下,下列各组物质,不用其他试剂就不能鉴别出来的是
A. 稀H2SO4、FeSO4溶液、CuSO4溶液、KMnO4溶液 B. CO2、 N2、NH3、CO
C. H2O NaOH NH4NO3 NaCl D. Mg 、CuO、Fe2O3、NaCl
难度: 中等查看答案及解析