-
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏
B.萃取、蒸馏、分液
C.分液、蒸馏、萃取
D.蒸馏、萃取、分液难度: 中等查看答案及解析
-
近几年,我国的航天事业成就斐然,“神舟六号”载人飞船已发射成功,“嫦娥”探月工程也在稳步进行中.据科学家预测,月球的土壤中吸附着数百万吨的3He,每百吨3He核聚变所释放出的能量相当于目前人类一年消耗的能量.在地球上,该元素主要以4He的形式存在.下列说法正确的是( )
A.4He原子核内含有4个质子
B.3He和4He互为同位素
C.3He原子核内含有3个中子
D.4He的最外层电子数为2,所以4He具有较强的金属性难度: 中等查看答案及解析
-
2005年3月29日晚,京沪高速公路上发生特大交通事故,一辆装载近35吨液氯的槽车因爆胎与迎面大客车相撞大量液氯外泄,导致多人死伤.下列有关现场处置方法不正确的是( )
A.将槽罐吊入盛烧碱的临时水池中
B.将人、畜迅速转移到地势较高的地方
C.用毛巾浸透NaOH溶液捂住鼻子
D.用毛巾浸透肥皂水或苏打溶液捂住鼻子难度: 中等查看答案及解析
-
质子数和中子数相同的原子A,其阳离子An+核外共有X个电子,则A的质量数为( )
A.2(x+n)
B.2(x-n)
C.2
D.n+2难度: 中等查看答案及解析
-
发射“神六”的运载火箭,其推进剂引燃后发生剧烈反应,产生大量高温无色气体(CO2.H2O.N2.NO)从火箭尾部喷出.但在发射现场看到火箭尾部喷出大量棕红色的气体,产生棕红色的气体的原因是( )
A.NO遇空气生成NO2
B.高温下N2遇空气生成NO2
C.CO2与N2反应生成CO和NO2
D.NO和H2O反应生成H2和NO2难度: 中等查看答案及解析
-
现有下列四种因素:①温度和压强 ②所含微粒数 ③微粒本身大小 ④微粒间的距离,其中对气体物质体积有显著影响的是( )
A.①②③
B.①③④
C.①②④
D.①②③④难度: 中等查看答案及解析
-
有同学将NaOH固体、P2O5固体、无水CaCl2固体划分为一类.据此分类,下列A~D选项中能与这三种物质归为一类的是 ( )
A.浓硫酸
B.CaO
C.碱石灰
D.NaCl难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.1mol H2O的质量为18g/mol
B.CO2的摩尔质量为44g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1mol任何物质体积均为22.4L难度: 中等查看答案及解析
-
20世纪末,纳米科技开始为世人所瞩目,以下分散系的分散质粒子与纳米粒子的大小大致相当的是( )
A.澄清石灰水
B.新制Cu(OH)2的悬浊液
C.NaCl溶于酒精中形成胶体
D.食盐水难度: 中等查看答案及解析
-
环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动中过度排放有关物质引起的.下列环境问题与所对应的物质不相关的是( )
A.温室效应--二氧化碳
B.酸雨--二氧化碳
C.臭氧层破坏--氟氯烃
D.光化学烟雾--二氧化氮难度: 中等查看答案及解析
-
下列情况会对人体健康造成较大危害的是( )
A.自来水中通入少量Cl2进行消毒杀菌
B.利用SO2的漂白作用使食品增白
C.用食醋清洗热水瓶胆内壁附着的水垢(CaCO3)
D.用小苏打(NaHCO3)发酵面团制作馒头难度: 中等查看答案及解析
-
下列反应的离子方程式正确的是( )
A.铝片踉氢氧化钠溶液反应:Al+2OH-═AlO2-+H2↑
B.硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓
C.碳酸钙跟醋酸反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑
D.氯化铝中加入过量的氢氧化钠:Al3++3OH-═Al(OH)3↓难度: 中等查看答案及解析
-
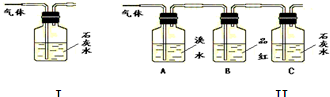
已知气体的摩尔质量越小,扩散速度越快.右图所示为气体扩散速度的试验,两种气体扩散相遇时形成白色烟环.下列关于物质甲、乙的判断正确的是( )
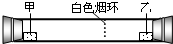
A.甲是浓氨水,乙是浓硫酸
B.甲是浓盐酸,乙是浓氨水
C.甲是浓氨水,乙是浓盐酸
D.甲是浓硝酸,乙是浓氨水难度: 中等查看答案及解析
-
右图的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与试验事实不相符的是( )
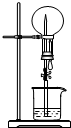
A.NO(H2O含石蕊)红色喷泉
B.NH3(H2O含酚酞)红色喷泉
C.SO2(NaOH溶液)无色喷泉
D.HCl(AgNO3溶液)白色喷泉难度: 中等查看答案及解析
-
将一小块钠投入到FeCl3的稀溶液中,以下对实验现象的描述中最恰当的是( )
A.Na溶解,溶液里有黑色固体析出和无色气体逸出
B.钠与溶液剧烈反应,溶液里有红褐色沉淀生成和无色气体放出
C.钠在溶液的表面上静静地消失,溶液里有红褐色沉淀生成
D.钠迅速消失,溶液里快速地冒出很多的气泡,同时有白色固体生成难度: 中等查看答案及解析
-
下列关于Fe2+和Fe3+的叙述中,错误的是( )
A.Fe2+的水溶液为浅绿色
B.Fe2+既有氧化性,又有还原性
C.Fe3+的水溶液为黄色
D.Fe3+溶液中滴入SCN-,立即出现红色沉淀难度: 中等查看答案及解析
-
硫酸、硝酸与盐酸是工业上常用的三大强酸.工业上制备硫酸常用接触法,工业上制硝酸是用氨的催化氧化法.下列关于工业上制硫酸与硝酸的说法中不正确的是( )
A.在接触室中进行的反应为:4FeS2+11O22Fe2O3+8SO2
B.氨被氧气催化氧化:4NH3+5O24NO+6H2O
C.硫酸工业、硝酸工业都需要对工业尾气进行处理
D.接触法制硫酸的原料为:二氧化硫、空气、水难度: 中等查看答案及解析
-
下列说法正确的是( )
A.工业制取硫酸的设备依次是沸腾炉、热交换器、吸收塔
B.硅是制造光导纤维的材料
C.水玻璃是建筑行业常用的一种黏合剂
D.纯碱、石灰石是制取水泥的原料难度: 中等查看答案及解析
-
下列溶液中不与单质Cu反应(必要时可加热)的是( )
A.浓盐酸
B.稀硝酸
C.浓硫酸
D.FeCl3溶液难度: 中等查看答案及解析
-
下列除杂方法(括号中为杂质)错误的是( )
A.N2(NO2)通过水洗涤
B.Na2CO3固体(NaHCO3)加热
C.Mg(Al)加NaOH溶液并过滤
D.NaCl溶液(I2)用CCl4萃取并分液难度: 中等查看答案及解析
-
下列除杂的操作方法,正确的是( )
A.NH3中混有少量水蒸气:通过装有浓硫酸的洗气瓶
B.NO中混有少量NO2气体:用水洗涤后再干燥
C.食盐中混有少量NH4Cl:加过量烧碱溶液后加热蒸干
D.硝酸混有少量硫酸:加适量BaCl2后再过滤难度: 中等查看答案及解析
-
最新的研究表明:一氧化氮吸入治疗法可快速改善SARS中重症患者的缺氧状况,缓解病情.病毒学研究证实,一氧化氮对SARS病毒有直接抑制作用.下列关于一氧化氮的叙述正确的是( )
A.一氧化氮是一种红棕色的气体
B.常温常压下,一氧化氮不能与空气中的氧气直接化合
C.含等质量氧元素的一氧化氮与一氧化碳的物质的量相等
D.一氧化氮易溶于水,不能用排水法收集难度: 中等查看答案及解析
-
相同质量的四份铜片,分别置于足量的下列酸中,所得到的气体的物质的量最多的是( )
A.稀硫酸
B.浓硫酸
C.稀硝酸
D.浓硝酸难度: 中等查看答案及解析