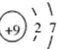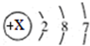-
A、B、C、D、E五瓶无色透明溶液,分别是HCl溶液、Na2CO3溶液、MgCl2溶液、NaNO3溶液、NaOH溶液中的一种.分别进行下列实验:
Ⅰ.将A分别滴入B、C、D、E中,均没有明显现象.
Ⅱ.将B分别滴入A、C、D、E中,C、E中均产生白色沉淀,其余没有明显现象.
Ⅲ.将C分别滴入A、B、D、E中,B中产生白色沉淀,D中有气泡冒出,其余没有明显现象.
(1)A是________,B是________,C是________;
(2)B加入E中的化学方程式是________;
(3)C加入D中的化学方程式是________.难度: 中等查看答案及解析
-
在“生石灰、明矾、碳酸钙、不锈钢、聚乙烯、纯碱”中选择适当的物质填空.
(1)用于制造医疗器械、炊具的是________;
(2)用作食品干燥剂的是________;
(3)用于造纸、纺织工业的盐是________;
(4)用作补钙的盐是________;
(5)属于有机高分子化合物的是________;
(6)净化水时可作絮凝剂的是________.难度: 中等查看答案及解析
-
用数字和化学符号填空:
(1)-2价的硫元素________;
(2)2个碳酸根离子________;
(3)氯酸钾________.难度: 中等查看答案及解析
-
如图是甲、乙两种固体物质的溶解度曲线,试回答下列相关问题.
(1)A点的含义________.
(2)t2℃时,100g水中溶解40g甲,溶液刚好饱和;那么,50g水中溶解________g甲,溶液达到饱和.
(3)t1℃时,若要将甲物质的不饱和溶液变为饱和溶液,可采用的方法是________(写出一种即可).
(4)t2℃时,甲、乙的饱和溶液分别降温至t1℃,析出晶体较多的是________(写“甲”、“乙”或“无法确定”)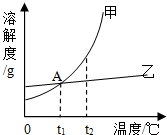
难度: 中等查看答案及解析
-
防腐剂山梨酸钾的化学式为C6H7KO2,试回答:
(1)山梨酸钾由________种元素组成.
(2)山梨酸钾的相对分子质量为________.
(3)山梨酸钾中钾元素的质量分数为________.难度: 中等查看答案及解析