-
化学与能源开发、环境保护、资源利用、食品安全等密切相关。下列说法正确是
A.自来水生产中应尽量用明矾净化、消毒
B.PM2.5是指大气中直径接近于2.5×10-6m的颗粒物,也称细颗粒物,这些细颗粒物分散在空气中形成混合物具有丁达尔效应
C.绿色化学的核心是利用化学反应原理治理环境污染
D.高纯硅及其氧化物在太阳能电池及信息高速传输中有重要应用
难度: 简单查看答案及解析
-
正确掌握好化学用语是学好化学的基础,下列有关表述正确的是
A.HClO的电子式
B.比例模型
:可以表示CH4,也可以表示CCl4
C.乙烯的结构简式:CH2CH2
D.碳酸氢根电离: HCO3-+ H2O
H3O++ CO32-
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数的值,下列叙述不正确的是
A.常温常压下,16g14CH4所含中子数目为8NA
B.1 mol -CH3含有9 NA个电子
C.常温常压下,44 g CO2气体含有氧原子的个数为2 NA
D.46gNO2和N2O4的混合物含有的原子数为3NA
难度: 中等查看答案及解析
-
卫生部发出公告,自2011年5月1日起,禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。下列对过氧化钙的叙述错误的是
A.CaO2具有氧化性,对面粉可能具有增白作用
B.CaO2和水反应时,每产生1 mol O2转移电子2 mol
C.CaO2中阴阳离子的个数比为2∶1
D.CaO2和CO2反应的化学方程式为:2CaO2+2CO2 =2Ca CO3+O2
难度: 中等查看答案及解析
-
下列物质中不能用化合反应的方法制得的是
①SiO2 ②H2SiO3 ③Fe(OH)3 ④Al(OH)3 ⑤FeCl2 ⑥ CaSiO3
A.①③ B.②④ C.②③④⑤ D.②④⑥
难度: 简单查看答案及解析
-
工业上冶炼金属钼的化学原理为:
①2MoS2+7O2
2MoO3+4SO2;
②MoO3+2NH3·H2O = (NH4)2MoO4+H2O;
③(NH4)2MoO4+2HCl = H2MoO4↓+2NH4Cl;
④H2MoO4
MoO3+H2O;
⑤用还原剂将MoO3还原成金属钼。则下列说法正确的是
A.上述①③⑤属于氧化还原反应,②④属于非氧化还原反应
B.MoO3是金属氧化物,也是碱性氧化物
C.H2MoO4是一种强酸
D.利用H2、CO和Al分别还原等量的MoO3,所消耗还原剂的物质的量之比为3∶3∶2
难度: 中等查看答案及解析
-
下列各组物质的无色溶液,不用其它试剂即可鉴别的是
①KOH Na2SO4 AlCl3 ②HCl NaAlO2 NaCl
③NaHCO3 Ba(OH)2 H2SO4 ④Ca(OH)2 Na2CO3 BaCl2
A.①② B.①③ C.①②③ D.①②④
难度: 中等查看答案及解析
-
中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去)。下列推断不正确的是
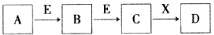
A.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
B.若D是一种强碱,则A、B、C均可与X反应生成D
C.若D为NaCl,且A可与C反应生成B,则E可能是CO2
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
难度: 困难查看答案及解析
-
25 ℃时,弱酸的电离平衡常数如表所示,下列离子反应方程式错误的是
弱酸
H2SO3
HClO
H2CO3
Ka1
1.54×10-2
2.95×10-8
4.30×10-7
Ka2
1.02×10-7
5.61×10-11
A.氯水中加入少量NaHCO3粉末:HCO3- + H+ = H2O+CO2↑
B.NaAl(OH)4溶液中通入足量的CO2:Al(OH)4-+CO2 =Al(OH)3↓+ HCO3-
C.NaClO溶液中通入少量CO2:2ClO- +H2O+CO2 = CO32- + 2HClO
D.Na2CO3溶液中通入少量SO2:2 CO32-+ H2O+ SO2 = SO32-+2HCO3-
难度: 中等查看答案及解析
-
下列离子方程式正确的是
A.向澄清石灰水中加入等物质的量的NaHCO3溶液:Ca2++2OH-+ 2HCO3- = CaCO3↓+CO32-+2H2O
B.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全:
Ba2+ + 2OH- + NH4+ + H+ + SO4 2- = BaSO4↓+ NH3·H2O + H2O
C.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O
D.明矾溶液中加入氢氧化钡溶液,使其产生沉淀的物质的量达最大值:
Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
难度: 中等查看答案及解析
-
在含有Fe3+、Fe2+、Al3+、NH4+的溶液中,加入足量Na2O2固体,微热充分反应后,再加入过量的稀盐酸,完全反应后,离子数目没有变化的是
A.Fe3+ B.Al3+ C.NH4+ D.Fe2+
难度: 中等查看答案及解析
-
化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是
A.检验溶液中是否含有SO32-时,用HNO3酸化后再加BaCl2溶液
B.为提高KMnO4溶液的氧化能力,用盐酸酸化KMnO4溶液
C.检验某溶液是否含有Fe3+时,用HNO3酸化后,加KSCN溶液
D.检验溶液中是否含有SO42-时,用HCl酸化后,加BaCl2溶液
难度: 中等查看答案及解析
-
下列除去杂质的方法正确的是
A.除去N2中的少量O2:通过灼热的CuO粉末,收集气体
B.除去CO2中的少量HCl:通入Na2CO3溶液,收集气体
C.除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤
D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤
难度: 中等查看答案及解析
-
下列可用来鉴别SO2和CO2气体的试剂有
①澄清石灰水②氢硫酸③氯水④酸性高锰酸钾⑤硝酸钡溶液⑥紫色石蕊试液⑦品红溶液
A.②③④⑤⑦ B.①④⑤⑥⑦ C.①②③⑥⑦ D.②③④⑥⑦
难度: 中等查看答案及解析
-
用36.5%的浓盐酸(密度1.2 g·cm-3)配1 mol·L-1的稀盐酸 100 mL,配制过程所用仪器,且使用先后顺序正确的是
①100 mL量筒 ②10 mL量筒 ③50 mL 烧杯 ④电子天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒
A.①③⑤⑥⑦ B.②③⑦⑤⑥ C.③⑤⑦⑥① D.④③⑦⑤⑥
难度: 简单查看答案及解析
-
右图所示的装置最适宜于干燥、收集的气体是

A.NO B.HC1 C.NO2 D.NH3
难度: 简单查看答案及解析
-
下列说法正确的是
A.在熔化状态下能导电的化合物为离子化合物
B.根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸
C.CO2、SiO2、NO2、P2O5均为酸性氧化物,Na2O、Na2O2为碱性氧化物
D.因为Na2O的水溶液能导电,所以Na2O是电解质
难度: 简单查看答案及解析
-
标准状况下,将a LSO2和Cl2组成的混合气体通入100mL0.1mol·L-1Fe2(SO4)3溶液中,充分反应后,溶液的棕黄色变浅。向反应后的溶液中加入足量的BaCl2溶液,将所得沉淀过滤、洗涤、干燥后称重,其质量为11.65g。则下列关于该过程的推断不正确的是
A.混合气体中SO2的体积为0.448L(标况) B.所得沉淀为0.05mol的BaSO4
C.a L混合气体的物质的量为0.04mol D.a的取值范围为 0.672<a<0.896
难度: 中等查看答案及解析
-
某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是
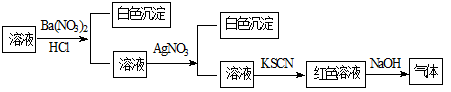
A.原溶液中一定含有SO42-离子 B.原溶液中一定含有NH4+离子
C.原溶液中一定含有Cl-离子 D.原溶液中一定含有Fe3+离子
难度: 中等查看答案及解析
-
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2 。在含3 mol NaHSO3的溶液中逐滴加入KIO3
溶液。加入KIO3和析出I2的物质的量的关系曲线如下图所示。下列说法不正确的是

A.0~b间反应:3HSO3-+ IO3-= 3SO42-+ I-+ 3H+
B.a点时消耗NaHSO3的物质的量为1.2 mol
C.b~c间反应:I2仅是氧化产物
D.当溶液中I¯与I2的物质的量之比为5∶2时,加入的KIO3 为1.08mol
难度: 中等查看答案及解析
-
金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以金红石为原料制取Ti的反应为
aTiO2 + bCl2+eC
aTiCl4+eCO Ⅰ
TiCl4+2Mg
Ti+2MgCl2 Ⅱ
关于反应Ⅰ、Ⅱ的分析不正确的是
①TiCl4在反应Ⅰ中是还原产物,在反应Ⅱ中是氧化剂;②C、Mg在两个反应中均被还原;
③在反应Ⅰ、Ⅱ中Mg的还原性大于C,C的还原性大于TiCl4;
④a=1,b=e =2 ⑤每生成19.2 g Ti,反应Ⅰ、Ⅱ中共转移4.8 mol e-。
A.①②④ B.②③④ C.③④ D.②③⑤
难度: 中等查看答案及解析
-
操作1:将1 L 1.00 mol·L-1的Na2CO3溶液逐滴加入到1 L 1.25 mol·L-1的盐酸中;操作2:将1 L 1.25 mol·L-1的盐酸逐滴加入1 L 1.00 mol·L-1 的Na2CO3溶液中,两次操作产生的气体体积之比(同温同压下)是
A.5∶2 B.2∶5 C.1∶1 D.2∶1
难度: 中等查看答案及解析
-
将同温同压下的NO、NO2、O2三种气体按以下体积比混合后通入水中,气体不能完全溶于水的是
A.1∶2∶1 B.1∶1∶1 C.5∶1∶4 D.6∶2∶5
难度: 中等查看答案及解析
-
将13.0g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生气体6.72L(标况)。另取等质量的合金溶于过量的稀硝酸中生成6.72L(标况)NO,向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量是
A.11.85g B.12.7g C.27.45 g D.28.3g
难度: 中等查看答案及解析