-
(2010•泰安)逻辑推理是化学学习常用的思维方法.下列推理正确的是( )
A.酸性溶液的pH都小于7,所以酸溶液pH一定小于7 B.有机物都含碳元素,所以含碳元素的化合物都是有机物 C.水是纯净物,所以海水也是纯净物 D.中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 难度: 中等查看答案及解析
-
(2011•河西区一模)将含有少量泥沙的粗盐提纯,并用制得的精盐配制一定质量分数的氯化钠溶液.下列说法错误 的是( )
A.过滤时搅拌漏斗中的液体可以加快过滤速度 B.蒸发滤液时,要不断用玻璃棒搅动蒸发皿中的液体 C.配制氯化钠溶液的实验过程需要经过计算、称量、溶解、装液等步骤 D.配制氯化钠溶液时需用的仪器有托盘天平、量筒、烧杯、玻璃棒等 难度: 中等查看答案及解析
-
(2010•鄂州)古语道:“人要实,火要虚”.此话的意思是说:做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺.从燃烧的条件看,“火要虚”的实质是( )
A.增大可燃物的热值 B.提高空气中氧气的含量 C.提高可燃物的着火点 D.增大可燃物与空气的接触面积 难度: 中等查看答案及解析
-
(2009•顺义区一模)医疗上,用C-14呼气试验取代胃镜,可以无痛、快速检测幽门螺旋杆菌.已知C-14原子中核电荷数为6,中子数为8,则该原子核外电子数为( )
A.14 B.6 C.8 D.12 难度: 中等查看答案及解析
-
(2013•天河区一模)合理使用化肥,有利于农作物的生长和减少环境污染.下列有关化肥的说法正确的是( )
A.为保证高产大量施用化肥 B.不能将氯化铵与碱性物质混合施用 C.CO(NH)2是一种常用的复合肥料 D.所有化肥都能全部溶于水 难度: 中等查看答案及解析
-
下列变化中,属于化学变化的是( )
A.钟乳石的形成 B.冰川融化 C.蒸发食盐水 D.玉石雕刻 难度: 中等查看答案及解析
-
(2009•桂平市二模)下列说法中,你认为不科学的是( )
A.食用碘盐可防治碘缺乏病 B.使用含氟牙膏可预防龋齿 C.缺乏维生素A,会导致夜盲症 D.实施“酱油加铁”,可减少厨房污染 难度: 中等查看答案及解析
-
(2009•黄石)下列实验数据合理的是:①用托盘天平称取15.6gNaCl固体;②用pH试纸测得某溶液的pH为3.52;③用普通温度计测得某液体温度为25.62℃;④用10mL量筒量取6.6mL某溶液.( )
A.①② B.②③ C.③④ D.①④ 难度: 中等查看答案及解析
-
(2008•南通)把少量物质分别加入到另一物质中,充分搅拌,可以得到溶液的是( )
A.碘加入汽油中 B.面粉加入水中 C.高锰酸钾加入汽油中 D.植物油加入水中 难度: 中等查看答案及解析
-
(2013•怀柔区一模)如图表示的是A,B,C三种溶液两两混合发生反应的实验现象,符合该实验现象的A,B,C三种溶液依次是( )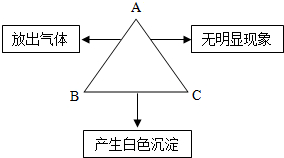
A.盐酸、碳酸钠溶液、氢氧化钠溶液 B.氯化钠溶液、澄清石灰水、氢氧化钠溶液 C.盐酸、碳酸钠溶液、澄清石灰水 D.氢氧化钙溶液、盐酸、硫酸钠溶液 难度: 中等查看答案及解析