-
化学与生产、生活、环境等密切相关。下列说法正确的是
A.开发氟氯代烷制冷剂,有利于保护臭氧层
B.绿色食品就是不使用农药,不含任何化学物质的食品
C.推广使用煤液化技术,可减少二氧化碳温室气体的排放
D.使用可降解的无毒聚乳酸塑料代替乙烯作食品包装袋,可减少白色污染
难度: 简单查看答案及解析
-
下列化学用语表示正确的是
A.甲基的电子式:
B.CH4分子的球棍模型:
C.(CH3)2C=CH2的命名:1-甲基-2-丙烯
D.甲醛的结构式:
难度: 简单查看答案及解析
-
下列说法正确的是
A.温度越高,酶对某些反应的催化效率越高
B.重金属盐使蛋白质变性,误食硫酸铜可立即吞服牛奶
C.甲烷、汽油、酒精都是碳氢化合物,都可作燃料
D.石油裂解和油脂皂化都是由高分子生成小分子的过程
难度: 简单查看答案及解析
-
下列实验可达到实验目的的是
A.用酸性KMnO4溶液可除去乙烷中混有的乙烯
B.向CH3CH2Br中滴入AgNO3溶液以检验溴元素
C.通过红外光谱分析可以区分乙酸和甲酸甲酯
D.乙酰水杨酸(
)与适量NaOH溶液反应制备(
)
难度: 简单查看答案及解析
-
下列有关物质的性质、制取或应用等说法正确的是
A.乙烯能发生加成反应,可用于合成塑料
B.在工业上,通过分馏石油可得到甲烷、乙烯、苯
C.实验室用苯和溴水混合,并加铁粉制取溴苯
D.可利用丁达尔效应来区别葡萄糖和蔗糖溶液
难度: 简单查看答案及解析
-
下列实验装置或操作中,正确的是
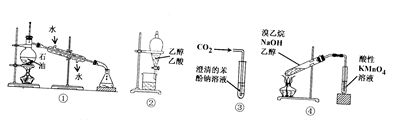
A.装置①用于蒸馏石油
B.装置②可用来分离乙醇和乙酸
C.装置③可用于比较碳酸、苯酚酸性的强弱
D.装置④可用于证明溴乙烷与NaOH乙醇溶液共热生成乙烯
难度: 中等查看答案及解析
-
甲、乙、丙、丁的相互转化关系如图所示(部分反应物及反应条件已略去,箭头表示一步转化)。下列各组物质中,不能满足图示转化关系的是
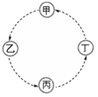
选项
甲
乙
丙
丁
A
CH2=CH2
CH2BrCH2Br
CH2OHCH2OH
B
NaAlO2
Al(OH)3
Al2O3
Al
C
CH3CH2OH
CH3CHO
CH3COOH
CH3COOC2H5
D
SiO2
H2SiO3
Na2SiO3
Si
难度: 中等查看答案及解析
-
短周期元素X、Y、Z、W的原子序数依次递增,它们的原子序数之和为32,且原子最外层电子数之和为10,X、Z原子的最外层电子数之和等于Y原子的次外层电子数,X与Z,Y与W均为同主族元素。下列叙述正确的是
A. Z、W单质的熔点:Z>W
B. 最高价氧化物对应的水化物的酸性:Y>W
C. 四种元素的原子半径:X>Y>Z>W
D. Z元素处于元素周期表中第三周期第ⅡA族
难度: 中等查看答案及解析
-
下列方程式书写正确的是
A.醋酸的电离:CH3COOH=CH3COO-+H+
B.苯与浓硫酸、浓硝酸混合液水浴加热制硝基苯:
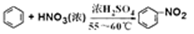
C.用新制Cu(OH)2悬浊液检验乙醛中的醛基:
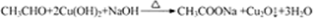
D.苯酚钠溶液中通入少量CO2:
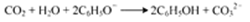
难度: 中等查看答案及解析
-
污水治理越来越引起人们重视,现通过膜电池除去废水中的乙酸钠和对氯苯酚(
),其原理如图所示。下列说法正确的是
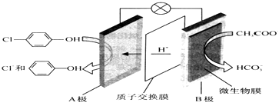
A.该装置实现电能转化为化学能
B.B为电池的正极,发生还原反应
C.电流方向为从B极沿导线经小灯泡流向A极
D.A极的电极反应式为:
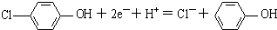
难度: 困难查看答案及解析
-
下列有关说法正确的是
A.反应CH3Cl(g)+Cl2(g)
CH2Cl2(g)+HCl(g) 能自发进行,该反应的△H>0
B.多电子原子中,1s、2s、3s电子的能量逐渐增大,2p、3p、4p能级的轨道数依次增多
C.由
 △H=+23kJ•mol-1可知,
△H=+23kJ•mol-1可知,比
更稳定
D.丙酸甲酯的水解反应,加入稀硫酸会使平衡向正反应方向移动
难度: 中等查看答案及解析
-
合成抗哮喘及抗过敏药普仑司特的某种中间体结构如下图:
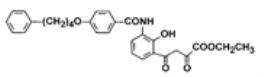
有关该中间体的说法正确的是
A.该分子中含有1个手性碳原子
B.能发生氧化、取代、加成反应
C.1mol该化合物与足量NaOH溶液反应,最多消耗4molNaOH
D.1mol该化合物与足量浓溴水反应,最多消耗1molBr2
难度: 中等查看答案及解析
-
下列设计的实验方案能达到实验目的的是
A.检验淀粉溶液是否发生水【解析】
取少量试液于试管中,加入碘水,看溶液是否变蓝B.提纯含少量苯酚的苯:加入氢氧化钠溶液,振荡后静置分液,并除去有机相的水
C.制取少量乙酸乙酯:向试管中加入浓硫酸,再加入无水乙醇,冷却后加入冰醋酸,加热,将生成的蒸气导至盛有氢氧化钠溶液的试管中
D.验证生成乙烯:浓硫酸和乙醇混合后加热,将产生的混合气体(C2H4、SO2、CO2等)通入溴水,观察溶液是否褪色
难度: 中等查看答案及解析
-
物质Ⅲ(2,3-二氢苯并呋喃)是一种重要的精细化工原料,其合成的部分流程如下:
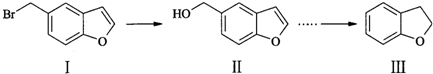
下列叙述正确的是
A.物质I的分子式为C9H7OBr
B.可用FeCl3溶液鉴别化合物II 和Ⅲ
C.物质I可发生消去反应
D.物质II中所有原子可能位于同一平面内
难度: 中等查看答案及解析
-
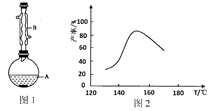
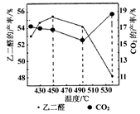
利用CO和H2在催化剂的作用下合成甲醇,反应如下:CO(g)+2H2(g)
CH3OH(g)。在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是

A.该反应的△H<0,且p1<p2<p3
B.在C点时,H2转化率为75%
C.反应速率:ν逆(状态A)>ν逆(状态B)
D.在恒温恒压条件下,向该密闭容器中再充入1molCH3OH,达平衡时CH3OH的体积分数增大
难度: 极难查看答案及解析
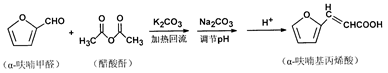


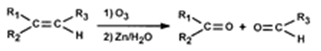
 )的合成路线如下(部分反应试剂和条件已略去):
)的合成路线如下(部分反应试剂和条件已略去):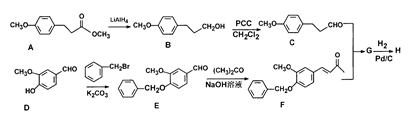
 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
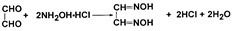 )
)