-
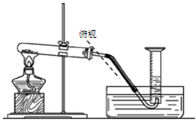
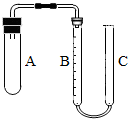
若用实验证明CuSO4溶液显蓝色不是由SO42-离子造成的,下列实验无意义的是( )
A.观察K2SO4溶液的颜色
B.向CuSO4溶液滴加适量的NaOH溶液,振荡后静置,溶液颜色消失
C.向CuSO4溶液滴加适量的BaCl2溶液,振荡后静置,溶液颜色未消失
D.加水稀释后CuSO4溶液颜色变浅难度: 中等查看答案及解析
-
下列实验过程的评价,正确的是( )
A.某固体中加入稀盐酸,产生了无色气体,证明该固体一定含CO32-
B.某溶液中滴加氯化钡溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含有SO42-
C.某无色溶液中滴入酚酞试液显红色,该溶液不一定是碱溶液
D.验证烧碱中是否含Cl-,先加足量稀硝酸,再加硝酸银溶液,有白色沉淀出现,证明含Cl-难度: 中等查看答案及解析
-
不法分子用铜锌合金制成假金元宝行骗的事件常有发生,下列不易区别其真伪的方法是( )
A.放入硫酸中
B.放入盐酸中
C.测定密度
D.观察外观难度: 中等查看答案及解析
-
超临界流体是温度和压力同时高于临界值的流体,也即压缩到具有接近液体密度的气体,是物质介于气态和液态之间的一种新的状态.目前应用最广的是超临界二氧化碳,它可作为溶剂、发泡剂取代某些有机溶剂、氟氯代烷等.下列有关说法中错误的是( )
A.超临界二氧化碳与其气态或液态之间的转化是物理变化
B.超临界二氧化碳的形成,引起二氧化碳化学性质的改变
C.超临界二氧化碳可用于中药、香料中有效成分的提取
D.用超临界二氧化碳代替氟氯代烷可减轻对臭氧层的破坏难度: 中等查看答案及解析
-
很多化学物质名称中含有“水”,“水”通常有三种含义:①表示水这种物质;②表示水溶液;③表示物质处于液态.下列物质名称中的“水”不属于以上三种含义的是( )
A.水晶
B.水银
C.氨水
D.蒸馏水难度: 中等查看答案及解析
-
浓硫酸和20%的稀硫酸,在实验室中敞口放置.它们的溶液质量和放置天数的关系如图,分析a、b曲线变化的原因是( )
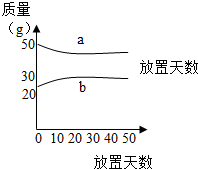
A.a升华、b冷凝
B.a蒸发、b吸水
C.a蒸发、b潮解
D.a冷凝、b吸水难度: 中等查看答案及解析
-
下列说法,违反科学原理的是( )
A.干冰可用于人工降雨
B.将煤隔绝空气强热可得到某种气体燃料
C.添加少量某物质将水变成汽油
D.在一定条件下石墨可变成金刚石难度: 中等查看答案及解析
-
在消毒剂家族中,臭氧和过氧乙酸的贡献并驾齐驱.O3可以看成是一个O2分子携带一个O原子,利用其自身的强氧化性杀灭病菌,反应后放出无污染的O2.下列关于O3说法中正确的是( )
A.O3与O2化学性质完全相同
B.等质量的O3与O2所含的原子个数相同
C.使用时浓度大小对人体无害
D.O3遇氟氯代烷不会分解难度: 中等查看答案及解析
-
常温下,向某浓度的硫酸溶液中逐滴滴入某浓度的氢氧化钡溶液,生成沉淀的质量与加入氢氧化钡溶液的体积关系如图所示.a、b、c、d分别表示实验时不同阶段的反应结果,下列说法中正确的是( )
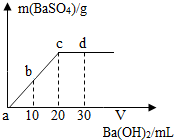
A.溶液的导电能力:a>b>c>d
B.溶液的pH大小:a>b>c>d
C.a,b溶液呈酸性
D.c,d溶液呈碱性难度: 中等查看答案及解析
-
反应前后化合价有变化的化学反应称为氧化还原反应.据最新报道,科学家发现了如下反应:O2+PtF6=O2(PtF6),已知
O2(PtF6)为离子化合物,其中Pt为+5价,对于此反应,下列说法正确的是( )
A.该反应既属于化合反应,又属于氧化还原反应
B.O2(PtF6)中氧元素的化合价为+1价
C.O2(PtF6)组成元素之一F的原子结构示意图为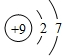
D.O2(PtF6)固体有良好的导电能力难度: 中等查看答案及解析
-
t℃时,甲、乙两个烧杯中各盛有100g相同浓度的KCl溶液.现将甲烧杯中的溶液蒸发掉35.0g H2O,恢复到t℃时,析出KCl固体5.0g;乙烧杯中的溶液蒸发掉45.0gH2O,恢复到t℃时,析出KCl固体10.0g.下列说法正确的是( )
A.原溶液的质量分数为33.3%
B.t℃时,KCl的溶解度为50.0g
C.原溶液的质量分数为50%
D.两烧杯中剩余溶液的溶质质量分数不同难度: 中等查看答案及解析
-
已知Si+2NaOH+H2O═Na2SiO3+2H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,硅不与盐酸反应.将含铁铝硅的合金样品分为等质量的两份,分别与足量的稀盐酸和烧碱溶液充分反应,测得放出氢气的质量相同.则该合金样品中铁铝硅的质量比不可能是( )
A.112:81:28
B.336:27:84
C.324:135:36
D.56:81:56难度: 中等查看答案及解析