-
下图为自米水生产过程示意图。下列说法正确的是
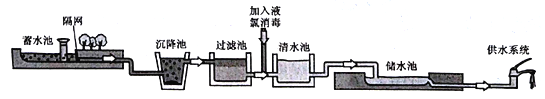
A. 清水池中的水是溶液 B. 过滤池中主要发生化学变化
C. 消毒用的液氯是化合物 D. 供水系统流出的水是纯净物
难度: 简单查看答案及解析
-
电脑芯片的制作要用到高纯度的硅。目前广泛采用石英砂(主要成分是SiO2)为原料制取,其中一步反应为:SiO2+2C
Si+2CO↑。对该反应分析正确的是
A. 该反应属于置换反应 B. 碳发生了还原反应
C. 碳元素化合价由0价变为+4价 D. 该反应利用了CO的还原性
难度: 中等查看答案及解析
-
肝脏中含有过氧化氢酶。某同学利用动物肝脏研究酶的某些特点,实验记录如下表:
试管
实验材料及处理
产生气泡快慢
1
5毫升5%H2O2溶液+2滴蒸馏水,常温
最慢
2
5毫升5%H2O2溶液+2滴3.5%FeCl3溶液,常温
较快
3
5毫升5%H2O2溶液+2滴肝脏研磨液,常温
最快
4
5毫升5%H2O2溶液+2滴肝脏研磨液,70℃水浴加热
较慢
分析实验结果,无法得出过氧化氢酶
A. 具有专一性 B. 能加快过氧化氢分解
C. 具有高效性 D. 活性受温度影响
难度: 中等查看答案及解析
-
下列选项所示的物质转化均能一步实现的是
A. Fe
Fe2O3
Fe(OH)3 B. CuO
CuSO4
CuCl2
C. S
SO2
H2SO4 D. CO2
Na2CO3
NaOH
难度: 中等查看答案及解析
-
某固体由Ba2+、Cu2+、Na+、Cl-、CO32-、SO42-中的几种离子构成,取一定质量的该固体样品,进行如下实验:
①将固体溶于水得无色透明溶液,加入足量BaCl2溶液,过滤后得到5克白色沉淀。
②在沉淀中加入过量稀硝酸,仍有3克白色沉淀。
③在滤液中滴加AgNO3溶液,产生白色沉淀。则该固体中一定含有
A. Na+、CO32-、SO42- B. Cu2+、CO32-、SO42-
C. Cl-、CO32-、SO42- D. Na+、Ba2+、Cl-
难度: 困难查看答案及解析