-
物质在化学反应前后,可能发生变化的是
A.原子总数 B.质子总数 C.电子总数 D.分子总数
难度: 简单查看答案及解析
-
下列说法中错误的是
A.0.3 mol H2SO4 B.1 mol H2O
C.0.5 mol 硫 D.3 mol 氢原子
难度: 简单查看答案及解析
-
下列电离方程式错误的是
A.NaHCO3==Na++H++CO32- B.NaHSO4(溶液)==Na++H++SO42-
C.MgCl2==Mg2++2Cl— D.Ba(OH)2==Ba2++2OH-
难度: 简单查看答案及解析
-
下列溶液中与50 mL 1 mol·L-1的AlCl3溶液中氯离子浓度相等的是
A.150 mL 1 mol·L-1 的NaCl B.75 mL 2 mol·L-1 的NH4Cl
C.150 mL 3 mol·L-1 的KCl D.75 mL 2 mol·L-1 的CaCl2
难度: 中等查看答案及解析
-
关于胶体和溶液的区别,下列叙述中正确的是
A.溶液呈电中性,胶体带有电荷
B.溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸
C.溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现明显光带
D.溶液稳定,放置后不会生成沉淀;胶体不稳定,放置会生成沉淀
难度: 简单查看答案及解析
-
下列化学反应中,属于氧化还原反应的是
A、Na2CO3+2HCl=2NaCl+CO2↑+H2O
B、CaO+H2O=Ca(OH)2
C、CaCO3
CaO+CO2↑
D、2CO +O2
2CO2
难度: 中等查看答案及解析
-
下列化合物中,不能由单质直接化合得到的是
A.NO B.Na2O2 C.FeCl2 D.CuCl2
难度: 中等查看答案及解析
-
在下列反应类型中,一定属于非氧化还原反应的是
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
难度: 简单查看答案及解析
-
下列变化中,必须使用氧化剂才能发生的是
A.HC1→NaCl B.SO2→S C.Na→Na2O2 D.NaHCO3→CO2
难度: 中等查看答案及解析
-
下列各组离子在水溶液中能大量共存的是
A.Na+、Ba2+、Cl、SO42- B.Ca2+、HCO3、C1、K+
C.Mg2+、Ag+、NO3、Cl D.H+ 、Cl 、Na+ 、CO32
难度: 中等查看答案及解析
-
氧化还原反应的实质是
A.化合价的升降 B.分子中各原子重新组合
C.电子的得失或偏移 D.氧原子的得失
难度: 简单查看答案及解析
-
为了除去FeCl2溶液中混有的少量FeCl3,最好的方法是向此溶液中
A.通入氯气 B.加入Zn C.加入Fe D.加入Cu
难度: 中等查看答案及解析
-
金属钠着火,能用来灭火的是
A.水 B.湿抹布 C.泡沫灭火剂 D.干沙
难度: 简单查看答案及解析
-
起固定氮作用的化学反应是
A.N2与H2在一定条件下反应生成NH3 B.NO遇O2转化为NO2
C.硝酸工厂用NH3氧化制NO D.由NH3制碳酸氢铵和硫酸铵
难度: 简单查看答案及解析
-
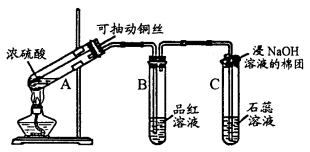
下列关于浓硫酸的叙述中,正确的是
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D.浓硫酸在常温下能够使铁、铝等金属形成氧化膜而钝化
难度: 中等查看答案及解析
-
制备干燥氨气所需的药品是
A.NH4CI溶液、NaOH溶液、浓H2SO4 B.饱和氨水
C.NaOH溶液、NH4CI晶体、浓H2SO4 D.NH4CI固体、碱石灰、氢氧化钙
难度: 中等查看答案及解析
-
下列关于Na2CO3和NaHCO3的叙述中错误的是
A.等质量的两种盐分别与足量的盐酸反应,在相同情况下,Na2CO3产生的二氧化碳多。
B.等物质的量的Na2CO3和NaHCO3分别与足量的盐酸反应,在相同情况下产生的二氧化碳体积相等。
C.等物质的量的Na2CO3和NaHCO3分别与同浓度的盐酸反应,Na2CO3消耗盐酸的体积是NaHCO3消耗盐酸体积的2倍
D.将石灰水加入NaHCO3溶液中会产生白色沉淀,而加入Na2CO3溶液中也会产生白色沉。
难度: 困难查看答案及解析
-
下列对于硝酸的认识,不正确的是
A、浓硝酸和稀硝酸都具有氧化性 B、铜与硝酸的反应属于置换反应
C、硝酸可氧化Fe2+ D、可用铁或铝制品盛装浓硝酸
难度: 中等查看答案及解析
-
.不能鉴别二氧化碳与二氧化硫的试剂是
A.品红溶液 B.澄清的石灰水
C.溴水 D.酸性高锰酸钾溶液
难度: 简单查看答案及解析
-
石英沙(主要成分SiO2)是一种常见工业原料,其中常混有少量碳酸钙。要除去石英沙中的少量碳酸钙,应采用的方法是
A.用稀硫酸溶解后过滤分离 B.用酒精灯加热
C.用水溶解后过滤分离 D.用稀盐酸溶解后过滤分离
难度: 中等查看答案及解析