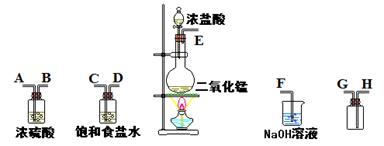
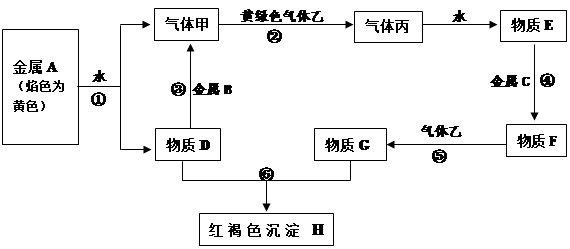
-
材料与化学密切相关。下列物质与材料对应关系不正确的是( )
A.晶体硅——光导纤维 B.氧化铝——耐火材料
C.铁碳合金——碳素钢 D.硅酸盐——普通玻璃
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A.潮湿的氯气遇二氧化硫其漂白性减弱
B.NO中有少量的NO2,用水洗涤后再干燥
C.一氧化氮可以由氮气和氧气在放电条件下直接化合得到
D.二氧化氮能与水反应生成硝酸,所以二氧化氮是硝酸的酸酐
难度: 中等查看答案及解析
-
制备氯化物时,常用两种方法:①用金属与氯气直接化合制得②用金属和盐酸反应制得;用以上两种方法都可以制得的氯化物是( )
A.CuCl2 B.FeCl2 C.FeCl3 D.AlCl3
难度: 中等查看答案及解析
-
下列实验现象描述不正确的是( )
A.一瓶98%的浓H2SO4敞口放置一段时间后,质量增加
B.SO3溶于水能导电。所以SO3是电解质
C.标准状况下,用一充满氨气的干燥烧瓶做喷泉实验,当水充满整个烧瓶后(假设溶液不外溢),烧瓶内氨水的物质的量的浓度为(1/22.4)mol/L
D.用蘸有稀氨水的毛笔,在浸有酚酞溶液的滤纸上写出的字呈红色
难度: 中等查看答案及解析
-
下列说法中正确的是( )
A.铵盐热分解一定有氨气产生。
B.因为SO2可以使酸性KMnO4溶液褪色,所以SO2有漂白性;
C.二氧化硫和二氧化氮都能形成酸雨,酸雨的pH<5.6;
D.用铜和稀硝酸反应制取NO,并用向上排空气法收集气体
难度: 中等查看答案及解析
-
下列各组物质中,因反应条件、用量、浓度等不同而发生不同化学反应的是( )
①Cu与硝酸;②SO2与NaOH溶液;③AlCl3溶液与KOH溶液;④CO2与Na2SiO3溶液;
⑤Zn和硫酸;⑥SO2和H2S
A.除②外 B.除⑥外 C.除⑤外 D.全部
难度: 中等查看答案及解析
-
由锌、铜、铝、镁四种金属中的两种组成的混合物32.5g,与足量的盐酸反应产生的氢气在标准状况下为11.2L,则混合物中一定含有的金属是( )
A.锌 B.铜 C.铝 D.镁
难度: 中等查看答案及解析
-
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的( )
A.将NaHCO3固体加入新制氯水,有无色气泡(H+)
B.滴加AgNO3溶液生成白色沉淀(Cl-)
C.向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈血红色(Cl2)
D.使红色布条褪色(HCl)
难度: 中等查看答案及解析
-
锥形瓶内盛有气体X,滴管内盛有液体y。若挤压滴管胶头,使液体y滴入锥形瓶中,振荡,过一会儿,可见小气球a鼓胀起来。气体X和液体y不可能是( )

X y
A NH3 H2O
B SO2 KOH溶液
C CO2 6mol∕L H2SO4溶液
D HCl 6mol∕L NaNO3溶液
难度: 困难查看答案及解析
-
在溶液中能共存,加入OH-有沉淀析出,加入H+能放出气体的是( )
A.Na+、H+、NO3-、Cl- B.K+、H+、Cl-、SO
C.Ca2+、NO3-、HCO3-、Cl- D.Fe3+、NH4+、SCN-、Cl-
难度: 困难查看答案及解析
-
下列离子方程式书写正确的是( )
A.漂白粉溶液中通入过量的CO2:Ca2++2ClO-+ CO2+ H2O = CaCO3↓+2HClO
B.氯气与水的反应: Cl2+H2O
2H++Cl-+ClO—
C.金属铁与稀硝酸反应 Fe + 2H+ = Fe2+ + H2↑
D.氢氧化钠溶液与氯化铵溶液混合NH4+ +OH-= NH3.H2O
难度: 困难查看答案及解析
-
在一定温度和压强下,把装有NO和 NO2的混合气体的试管倒立于水中,充分反应后,试管内气体的体积缩小为原气体体积的3/5,则原混合气体中NO和NO2的体积比为( )
A.2:3 B.3:2 C. 5:3 D.3:5
难度: 中等查看答案及解析
-
下图所示的实验或操作中,能达到实验目的的是( )
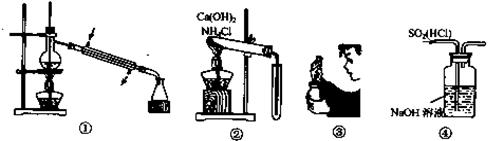
A.图①常用于分离沸点不同且彼此互溶的液态混合物
B.图②可用于实验室制备并收集少量的NH3
C.图③表示的是实验室闻氯气气味的方法
D.图④可用于除去SO2中的HCl气体
难度: 中等查看答案及解析
-
类推思维是化学解题中常用的一种思维方法,下列有关离子方程式的类推正确的是( )
已知 类推
A 将Fe加入CuSO4溶液中
Fe+Cu2+=Cu+Fe2+ 将Na加入到CuSO4溶液中
2Na+Cu2+=Cu+2Na+
B 向稀硫酸加入NaOH溶液至中性
H++OH-=H2O 向H2SO4溶液加入Ba(OH)2溶液至中性
H++OH-=H2O
C 向氯化铝溶液中加入足量NaOH溶液
Al3+ + 4OH- = AlO2- + 2H2O 向氯化铝溶液中加入足量氨水
Al3+ + 4NH3·H2O = AlO2- + 2H2O +4NH4+
D 向Ca(OH)2溶液中通入过量CO2
CO2 + OH- = HCO3- 向Ca(OH)2溶液中通入过量SO2
SO2 + OH- = HSO3-
难度: 困难查看答案及解析
-
100mL 0.1mol/L AlCl3溶液中,加入1mol/L NaOH溶液v mL后,再滴加1mol/L盐酸。滴加盐酸的体积(横坐标)与生成沉淀的质量(纵坐标)如图示的关系,则加NaOH溶液的体积为( )
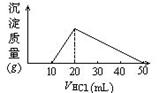
A.50mL B.40mL C.30mL D.10mL
难度: 中等查看答案及解析
-
将Cu放入0.1mol/LFeCl3溶液中,反应一段时间后取出Cu片,溶液中Fe3+与Fe2+的物质的量浓度之比为4:3,则反应后溶液中Cu2+与Fe3+的物质的量之比为( )
A.3:2 B.3:8 C.4:3 D.3:4
难度: 中等查看答案及解析
-
在1 L 1mol?L-1的氨水中( )
A.含1 mol NH3分子 B.含NH3、NH4+之和为1 mol
C.含1 mol NH3?H2O D.含NH3、NH3?H2O、NH4+之和为1 mol
难度: 中等查看答案及解析
-
等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是( )
A.2 mol·L-1 H2SO4溶液 B.18 mol·L-1 H2SO4溶液
C.6 mol·L-1 KOH溶液 D.3 mol·L-1 HNO3溶液
难度: 中等查看答案及解析
-
X、Y、Z、W有如右图所示的转化关系,则X、Y、Z可能是
① N2、NO、NO2 ② AlCl3、Al(OH)3 、NaAlO2
③S、SO2 、SO3 ④ NaOH、Na2CO3、NaHCO3
A.①②③④ B.①② C.②④ D.③④
难度: 困难查看答案及解析
-
物质的量之比为2:5的镁与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后镁没有剩余,则该反应中未被还原的硝酸与被还原的硝酸的物质的量之比是
A.1:4 B.4:1 C.2:3 D.2:5
难度: 中等查看答案及解析