-
下列各组物质的燃烧热相等的是
A.碳和一氧化碳 B.1moL碳和2moL碳
C.1moL乙炔和2moL碳 D.淀粉和纤维素
难度: 中等查看答案及解析
-
下列关于原电池的叙述正确的是
A.构成原电池的正极和负极必须是两种不同的金属
B.原电池是将化学能转变为电能的装置
C.原电池中电子流出的一极是负极,该极被还原
D.原电池放电时,电流的方向是从负极到正极
难度: 中等查看答案及解析
-
反应:A(气)+3B(气)
2C(气); ΔH < 0 达平衡后,将气体混合物的温度降低,下列叙述中正确的是
A.正反应速率加大,逆反应速率变小,平衡向正反应方向移动
B.正反应速率变小,逆反应速率加大,平衡向逆反应方向移动
C.正反应速率和逆反应速率都变小,平衡向正反应方向移动
D.正反应速率和逆反应速率都变小,平衡向逆反应方向移动
难度: 中等查看答案及解析
-
已知C(石墨) = C(金刚石),ΔH =+119KJ/mol,则可判断
A.金刚石比石墨稳定 B.一样稳定
C.石墨比金刚石稳定 D.无法判断
难度: 中等查看答案及解析
-
反应A+3B=2C+D在四种不同情况下的反应速率分别为:①v(A) =0.15mol/(L·s) ;②v(B)=0.6mol/(L·min);③v(C)=0.5mol/(L·s);④v (D) =0.45mol/(L·s) ,则反应进行由快到慢的顺序为
A.④>③>①>② B.②>④>③>①
C.②>③>④>① D.④>③>②>①
难度: 中等查看答案及解析
-
下列物质在水溶液中其电离方程式书写正确的是
A.CH3COOH
H++CH3COO-
B.NaHSO4
Na++HSO4-
C.H3PO4
3H++PO43-
D.NaHCO3
Na++H++CO32-
难度: 中等查看答案及解析
-
下列说法正确的是
A.需要加热才能发生的反应一定是吸热反应
B.任何放热反应在常温条件下一定能发生反应
C.反应物和生成物所具有的总能量决定了放热还是吸热
D.吸热反应在任何条件下都不能发生反应
难度: 中等查看答案及解析
-
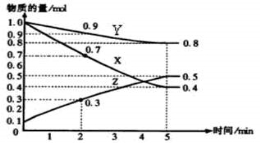
一定温度下,下列叙述不能作为可逆反应A(g)+3B(g)
2C (g) 达到平衡状态标志的是
(1)C生成速率与C分解速率相等
(2)单位时间内生成amolA,同时生成3amolB
(3)A、B、C的浓度不再变化
(4)A、B、C的物质的量不再变化
(5)混合气体的总压不再变化
(6)混合气体的物质的量不再变化
(7)单位时间内消耗a molA,同时生成3a molB
(8)A、B、C的分子数之比为1:3:2
A.(2) (8) B.(1) (6) C.(2) (4) D.(3) (8)
难度: 中等查看答案及解析
-
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是
A、加热
B、不用稀硫酸,改用98%的浓硫酸
C、滴加少量CuSO4溶液
D、不用铁片,改用铁粉
难度: 中等查看答案及解析
-
25℃时,水的电离达到平衡:H2O
H++OH;ΔH>0,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH―)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量稀硫酸,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,pH不变
难度: 中等查看答案及解析
-
化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是

A.该反应是吸热反应
B.断裂1molA-A键和 1molB-B键可放出xkJ能量
C.断裂2molA-B键需要吸收ykJ能量
D.2molAB的总能量高于1molA2和1molB2的总能量
难度: 中等查看答案及解析
-
已知2SO2(g) + O2(g)
2SO3(g)。若在500℃和催化剂的作用下,该反应在容积固定的密闭容器中进行,下列有关说法不正确的是
A.若升高温度,可以加快反应速率
B.使用催化剂是为了加快反应速率
C.在上述条件下,SO2不能完全转化为SO3
D.达到平衡时,SO2的浓度与SO3的浓度相等
难度: 中等查看答案及解析
-
下列装置或操作能达到实验目的的是
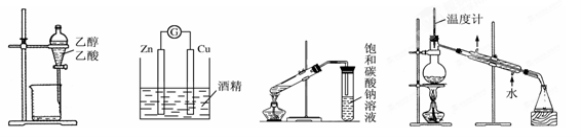
A.分离乙酸和乙醇 B.构成锌铜原电池 C.制备乙酸乙酯 D.制备蒸馏水
难度: 中等查看答案及解析
-
锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:
Zn(s)+2MnO2(s)+H2O(l)= Zn(OH)2(s)+Mn2O3(s),下列说法中错误的是
A.电池工作时,锌失去电子 ,锌是负极
B.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
C.电池负极的电极反应式为:Zn-2e-+2OH—=Zn(OH)2
D.电池工作时,电子由负极流向正极,溶液中OH—向正极移动,K+、H+向负极移动
难度: 中等查看答案及解析
-
已知“凡气体分子总数增多的反应一定是熵增大的反应”。根据所学知识判断,下列反应中,在任何温度下都不能自发进行的是
A. 2O3(g)===3O2(g) ΔH<0
B. 2CO(g)===2C(s)+O2(g) ΔH>0
C. N2(g)+3H2(g)===2NH3(g) ΔH<0
D. CaCO3(s)===CaO(s)+CO2(g) ΔH>0
难度: 中等查看答案及解析
-
X、Y、Z、M代表四种金属元素,金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为
A.X>Z>Y>M B.X>Y>Z>M
C.M>Z>X>Y D.X>Z>M>Y
难度: 中等查看答案及解析