-
如果你在厨房不小心将花生油与凉开水混在一起,你将采用下列何种方法进行分离( )
A.过滤 B.蒸馏 C.分液 D.萃取
难度: 简单查看答案及解析
-
下列类型的反应,一定发生电子转移的是 ( )
A.分解反应 B.离子反应
C.置换反应 D.复分解反应
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数的数值,下列说法正确的是 ( )
A.常温下,23 g NO2含有NA个氧原子
B.1 L 0.1 mol·L-1氨水含有0.1 NA个OH-
C.常温常压下,22.4 L CCl4含有NA个CCl4分子
D.1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子
难度: 简单查看答案及解析
-
下列关于溶液和胶体的叙述,正确的是 ( )
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质分子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
难度: 简单查看答案及解析
-
下表中对于相关物质的分类全部正确的一组是 ( )
编号
纯净物
混合物
弱电解质
非电解质
A
明矾
蔗糖
NaHCO3
CO2
B
漂白粉
石膏
SO2
C2H5OH
C
王水
冰
H2SiO3
Cl2
D
胆矾
玻璃
H2CO3
NH3
难度: 简单查看答案及解析
-
除去下列物质中少量杂质的方法正确的是 ( )
A.除去CO2中混有的HCl:用饱和碳酸钠溶液洗气
B.除去NO2中混有的NO:用水洗气
C.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤
D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤
难度: 简单查看答案及解析
-
同温同压下,质量忽略不计的两气球A和B,分别充入X气体和Y气体,且充气后两气球的体积相同.若相同条件下,A气球放在CO中静止不动,B气球放在O2中上浮.下列叙述或表示正确的是 ( )
A.X气体的相对分子质量比Y气体的相对分子质量大
B.X可能是N2,Y可能是CH4
C.X气体的密度小于Y气体的密度
D.充气后A气球质量比B气球质量大
难度: 简单查看答案及解析
-
如下图所示,纵坐标表示导电能力,横坐标表示所加溶液的量,以下各组反应,符合该图的是 ( )
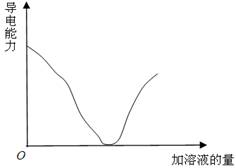
A.Ba(OH)2溶液中滴加稀H2SO4 B.NaOH溶液中滴加稀HCl
C.CH3COOH溶液中滴加KOH溶液 D.Cu(OH)2悬浊液中滴加HNO3溶液
难度: 简单查看答案及解析
-
下列各组离子,在溶液中能大量共存、加入NaOH溶液后加热既有气体放出又有沉淀生成的一组是 ( )
A. H+、NH4+、Fe2+、NO3- B.H+、K+、SiO32—、NO3—
C. K+、Ba2+、HCO3—、Cl- D. Mg2+、NH4+、SO42-、K+
难度: 简单查看答案及解析
-
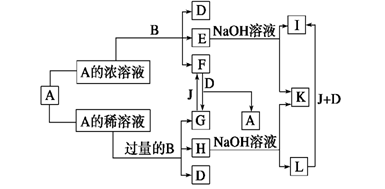
铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见物质,四种物质间的反应关系如下图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是 ( )
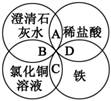
A.OH -+HCl === H2O+Cl-
B.Ca(OH)2+Cu2+ === Ca2++Cu(OH)2
C.Fe+Cu2+ === Cu+Fe2+
D.Fe+2H+ === Fe3++H2↑
难度: 简单查看答案及解析
-
下列各组物质依次表示为a、b、c、d,图中箭头表示一步转化。满足如图所示转化关系的是 ( )
A. Na Na2O2 NaOH Na2CO3 B. S SO2 H2SO3 NaHSO3
C. Cu CuO Cu(OH)2 CuSO4 D. Si SiO2 H2SiO3 Na2SiO3
难度: 简单查看答案及解析
-
已知:①向KMnO4晶体中滴加浓盐酸,产生黄绿色气体;
②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;
③取少量实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。
下列判断正确的是 ( )
A.上述实验证明氧化性:KMnO4>Cl2>Fe3+>I2
B.上述实验中,共有两个氧化还原反应
C.实验①生成的气体通入紫色石蕊试液中,溶液只有变红的现象
D.实验②证明Fe2+既有氧化性又有还原性
难度: 简单查看答案及解析
-
在甲乙两个坩埚中分别盛等质量的碳酸氢钠:将甲充分加热,之后冷却至室温;乙不加热。分别向甲、乙两坩埚中加入足量的相同物质的量浓度的盐酸,反应后甲、乙两坩埚中实际消耗的HCl的物质的量之比为 ( )
A.2:1 B.1:1 C.1:2 D.无法确定
难度: 简单查看答案及解析
-
将a mol H2、Cl2混合气体(体积比为1:2)经光照充分反应后,所得气体恰好使溶液中 b mol NaOH 完全转变为盐,则 a、b 的关系为 ( )
A.a=b B.2a=b C.4a=3b D.2a=3b
难度: 简单查看答案及解析
-
标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g/mL),所得溶液的密度为ρ g/mL,质量分数为w,物质的量浓度为c mol/L,则下列关系式中不正确的是 ( )
A.c=1 000Vρ/(17V+22 400) B. w=17c/(1 000ρ)
C. w=17V/(17V+22 400) D. ρ=(17V+22 400)/(22.4+22.4 V)
难度: 简单查看答案及解析
-
现有等体积混合而成的4组气体:①NO2+NO、②NO2+O2、③HCl+N2、④Cl2+SO2. 现将其分别通入体积相同的试管中并立即倒立在足量水中,试管内水面上升的高度分别为h1、h2、h3、h4,则高度关系是 ( )
A.h4>h2>h3>h1 B. h4>h3>h2>h1 C. h2>h3>h1>h4 D. h3>h2>h1>h4
难度: 简单查看答案及解析
-
1.92 g铜投入一定量的浓硝酸中,铜完全溶解,生成气体颜色越来越浅,共收集到672 mL气体(标准状况),将盛有此气体的容器倒扣在水中,通入氧气恰好使气体完全溶解在水中,则需要标准状况下的氧气体积为 ( )
A.504 mL B.168 mL C.224 mL D.336 mL
难度: 简单查看答案及解析