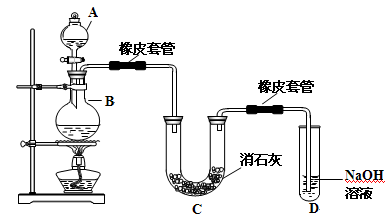
-
下列说法不正确的是( )
A.水晶、玛瑙、石英的主要成分都是SiO2
B.CO2通入水玻璃中可以得到硅酸沉淀
C.提前建成的三峡大坝使用了大量水泥,水泥是硅酸盐材料
D.高纯度的硅单质广泛用于制作光导纤维
难度: 中等查看答案及解析
-
关于Na2CO3和NaHCO3性质的有关叙述正确的是( )
A.在水中溶解性:Na2CO3<NaHCO3
B.热稳定性:Na2CO3<NaHCO3
C.与酸反应的速度:Na2CO3<NaHCO3
D.Na2CO3不能转化成NaHCO3,而NaHCO3能转化为Na2CO3
难度: 中等查看答案及解析
-
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ⑧氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
难度: 中等查看答案及解析
-
下列事实与胶体性质无关的是( )
A.在豆浆里加入盐卤做豆腐
B.江河流入大海处易形成沙洲
C.一支钢笔使用两种不同牌子的墨水,易出现堵塞
D.往氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀
难度: 简单查看答案及解析
-
下列叙述中正确的是( )
A.金属阳离子被还原时一定生成金属单质
B.非金属单质在氧化还原反应中只能作氧化剂
C.金属阳离子在氧化还原反应中只能作氧化剂
D.金属单质在氧化还原反应中只能作还原剂
难度: 简单查看答案及解析
-
用下列实验装置进行相应实验,能达到实验目的的是( )
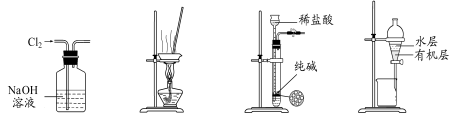
图1 图2 图3 图4
A.用图1 所示装置除去Cl2中含有的少量HCl
B.用图2 所示装置蒸发结晶提纯后的粗盐溶液,得NaCl晶体
C.用图3 所示装置制取少量纯净的CO2气体
D.用图4 所示装置分离用苯萃取碘水后已分层的有机层和水层
难度: 中等查看答案及解析
-
下列说法中正确的是( )
A.1 mol·L-1的NaCl溶液是指此溶液中含有1 mol NaCl
B.从1L 0.5mol·L-1的NaCl溶液中取出10mL溶液,其物质的量浓度仍为0.5mol·L-1
C.1L水中溶解58.5g NaCl,该溶液中NaCl的物质的量浓度为1mol·L-1
D.1 mol·L-1的CaCl2溶液中,Cl-的物质的量浓度为1 mol·L-1
难度: 中等查看答案及解析
-
下列各金属的混合物2.5g和足量的盐酸反应,放出的H2在标准状况下体积为2.24L,其中可能的是( )
A.Zn和Fe B.Mg和Zn C.Al和Mg D.Cu和Fe
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.1 mol N2所含有的原子数为NA
B.标准状况下,22.4 L水中含有的水分子数为NA
C.等物质的量的N2和CO所含分子数均为NA
D.常温常压下32g SO2与标准状况下11.2L N2含有相同的分子数
难度: 简单查看答案及解析
-
用0.1 mol/L的Na2SO3溶液30 mL,恰好将2×10-3 mol XO4-还原,则元素X在还原产物中的化合价是( )
A.+4 B.+3 C.+2 D.+1
难度: 简单查看答案及解析
-
已知:KClO3+6HCl(浓) KCl+3Cl2↑+3H2O。如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是( )
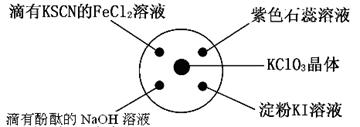

难度: 简单查看答案及解析
-
常用氯气给自来水消毒,某同学用自来水配制下列物质的溶液,会产生明显药品变质的是( )
①FeCl2 ②AgNO3 ③Na2CO3 ④AlCl3 ⑤KI ⑥石蕊试液
A.①②④ B.①②③⑤⑥ C.①②④⑥ D.全部
难度: 简单查看答案及解析
-
用98%的浓硫酸(密度为1.84g/cm3)配制100mL 1 mol/L的稀硫酸,现给出下列仪器(配制过程中可能用到):①100mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒,配制中使用仪器的先后顺序排列正确的是( )
A.④③⑦⑤⑥ B.②⑤⑦⑥ C.①③⑤⑥⑦ D.②⑥③⑦⑤⑥
难度: 简单查看答案及解析
-
下列反应的离子方程式正确的是( )
A.铝粉投入到NaOH溶液中:2Al +2OH- = 2AlO2- + H2↑
B.铁粉加入三氯化铁溶液中:2Fe +Fe3+ = 3Fe2+
C.AlCl3溶液中加入足量的氨水:Al3+ + 3OH- = Al(OH)3↓
D.FeCl2溶液中加入氯水:Cl2 +2 Fe2+ ="2" Fe3+ + 2Cl-
难度: 简单查看答案及解析
-
某无色溶液放入铝片后有氢气产生,在该溶液中一定可以大量共存的离子组( )
A.Na+、K+、Cl-、SO42- B.Al3+、Na+、NO3-、SO42-
C.Na+、K+、CO32- 、SO42- D.Na+、K+、HCO3-、SO42-
难度: 简单查看答案及解析
-
VmL Al2(SO4)3溶液中含a
SO42-,若把此溶液取一半加水稀释至2V mL,则稀释后溶液中Al3+的物质的量浓度为( )
A.
mol/L B.
mol/L C.
mol/L D.
mol/L
难度: 简单查看答案及解析
-
下列离子的检验方法合理的是( )
A.向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+
B.向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+
C.向某溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+
难度: 简单查看答案及解析
-
氢化钠(NaH)是一种生氢剂,可发生如下反应:NaH+H2O = NaOH+H2↑对这一反应的描述正确的是( )
A.NaH是氧化剂 B.NaH是氧化产物
C.NaOH是还原产物 D.氧化产物与还原产物的质量比是1:1
难度: 简单查看答案及解析
-
某无色溶液中含有H+、Al3+、Mg2+三种阳离子,逐滴加入0.1moL/L NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如下图所示,则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为( )

A.1:1:1 B.2:2:1 C.2:1:1 D.1:1:2
难度: 简单查看答案及解析
-
把a g 铝铁合金粉末溶于足量盐酸中,再加入过量氢氧化钠溶液。过滤出沉淀,经洗涤、干燥、灼烧,得到红棕色粉末的质量仍为a g,则此合金中铝的质量分数为( )
A.70% B.30% C.52.4% D.22.2%
难度: 简单查看答案及解析