-
甲、乙、丙三种溶液中各含一种卤离子,往甲中加入淀粉和氯水,溶液变为蓝色,再往丙中加入淀粉和氯水,颜色无明显变化,则甲、乙、丙依次含有( )
A.Br-、Cl-、I-
B.Cl-、I-、Br-
C.I-、Br-、Cl-
D.Br-、I-、Cl-难度: 中等查看答案及解析
-
环境污染已成为人类社会面临的重大威胁,酸雨是一种严重的环境污染,酸雨的形成主要是由于( )
A.森林遇到乱砍乱伐,破坏了生态平衡
B.燃放烟花爆竹
C.大气中二氧化碳的含量增加
D.大量燃烧含硫化石燃料难度: 中等查看答案及解析
-
新型净水剂高铁酸钾(K2FeO4)为暗紫色固体,可溶于水.工业上制备K2FeO4的常用方法之一是次氯酸盐氧化法:
①2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O,②Na2FeO4+2KOH═K2FeO4+2NaOH.
下列说法不正确的是( )
A.反应①为氧化还原反应,反应②为复分解反应
B.反应①中NaClO 是氧化剂
C.反应②的产物K2FeO4中Fe为+4价,具有强氧化性,能杀菌消毒
D.若有2 mol FeCl3 发生反应,转移电子的物质的量为 6 mol难度: 中等查看答案及解析
-
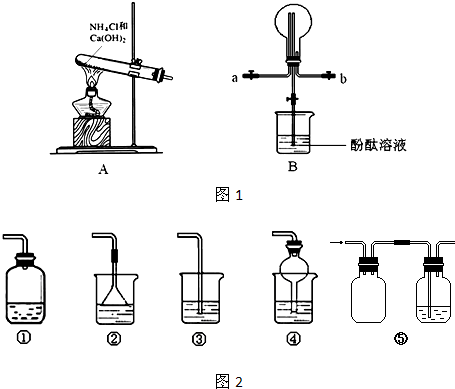
下列气体中,既可用浓硫酸干燥,又可用碱石灰干燥的是( )
A.O2
B.Cl2
C.SO2
D.NH3难度: 中等查看答案及解析
-
下列各组物质中,所含分子数相同的是( )
A.10 g H2与10 g O2
B.2240mL Cl2和0.1mol N2
C.9g H2O和0.5 mol Br2
D.常温常压下11.2 L SO2与3.01×1023个CO2难度: 中等查看答案及解析
-
下列化合物中,不能通过两种单质间化合直接制取的是( )
A.FeCl3
B.CuCl2
C.HCl
D.FeCl2难度: 中等查看答案及解析
-
合金是一类用途广泛的金属材料,下列物质属于合金的是( )
A.钢
B.铜
C.金刚石
D.磁性氧化铁难度: 中等查看答案及解析
-
可以用向下排空气法收集的气体是( )
A.NO
B.H2
C.SO2
D.NO2难度: 中等查看答案及解析
-
当光束通过下列分散系时:①氯化钠溶液,②CuSO4溶液,③淀粉溶液,④Fe(OH)3胶体,能观察到丁达尔效应的是( )
A.①②
B.②③
C.②④
D.③④难度: 中等查看答案及解析
-
下列变化,需加入还原剂才能实现的是( )
A.H2SO4→SO2
B.Al(OH)3→AlO2-
C.HCl→Cl2
D.HSO3-→SO32-难度: 中等查看答案及解析
-
下列物质的分类正确的是( )
混合物 电解质 碱 酸式盐 A 漂白粉 SO2 氨水 NaHCO3 B 玻璃 Cl2 KOH 明矾 C 胆矾 HNO3 纯碱 NH4Cl D 食醋 BaSO4 苛性钠 NaHSO3
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
欲使AlCl3溶液中的铝离子尽可能多地沉淀出来,最好选用的试剂是( )
A.石灰水
B.氢氧化钠溶液
C.氨水
D.硫酸难度: 中等查看答案及解析
-
下列有关实验的叙述中,不正确的是( )
A.用酒精萃取碘水中的碘
B.少量金属钠保存在煤油中
C.不慎洒出的酒精在桌上着火时,立即用湿抹布盖灭
D.配制1.00 mol/L NaCl溶液时,将称好的NaCl固体放入烧杯中溶解难度: 中等查看答案及解析
-
下列说法错误的是( )
A.硅是制造太阳能电池的常用材料
B.二氧化硅是制造光导纤维的材料
C.水玻璃的主要成分是Na2SiO3,可用作木材防火剂
D.常温下硅的化学性质活泼,可以与氯气、强酸、强碱溶液等起反应难度: 中等查看答案及解析
-
区别NaCl、FeCl3和NH4Cl三种溶液,可选用下列试剂中的( )
A.KSCN溶液
B.BaCl2溶液
C.NaOH溶液
D.AgNO3溶液难度: 中等查看答案及解析
-
能实现下列物质间直接转化的元素是( )
单质氧化物
酸或碱
盐.
A.硅
B.硫
C.铜
D.铁难度: 中等查看答案及解析
-
在①Al2O3 ②Al(OH)3③Na2CO3④NH4HCO3四种物质中,与盐酸和氢氧化钠溶液均可反应的是( )
A.①②③
B.②③④
C.①②④
D.①③④难度: 中等查看答案及解析
-
下列实验现象与氧化还原反应有关的是( )
A.氨水中滴加石蕊试液显蓝色
B.NO2 通入水中,气体由红棕色逐渐转变为无色
C.向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀
D.向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成难度: 中等查看答案及解析
-
将足量的新制氯水分别滴加到下列溶液或滤纸上,对所观察到的现象描述合理的一组是( )
AgNO3溶液 蓝色石蕊试纸 Na2CO3溶液 A 产生沉淀 变红 有气泡 B 无明显现象 变红 产生沉淀 C 产生沉淀 先变红后褪色 有气泡 D 产生沉淀 先变红后褪色 产生沉淀
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
一定条件下,将等体积NO和O2充入一试管,并将试管倒立于水槽中,充分反应后剩余气体的体积约为原总体积的( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.pH=12的溶液:K+、Na+、CO32-、SO42-
B.1.0 mol/L的NaNO3溶液:H+、Fe2+、Cl-、SO42-
C.使pH试纸显红色的溶液:NH4+、Ba2+、HCO3-、Cl-
D.与铝反应产生大量氢气的溶液:Na+、K+、Fe3+、NO3-难度: 中等查看答案及解析
-
用以下三种途径制取相同质量的硝酸铜:①铜与浓硝酸反应;②铜与稀硝酸反应;③铜与氧气反应生成氧化铜,氧化铜再与稀硝酸反应.下列叙述不正确的是( )
A.对环境造成的危害:③最小
B.所消耗的硝酸的物质的量:①>②>③
C.三种途径所消耗的铜的质量相同
D.铜与浓硝酸反应速率最快,故制取硝酸铜最佳方案是①难度: 中等查看答案及解析
-
NA代表阿伏加德罗常数,下列说法正确的是( )
A.0.1 molNa2O2与足量的CO2充分反应转移的电子数为0.2NA
B.0.1 mol铁在0.1 mol Cl2中充分燃烧,有0.3NA个电子转移
C.等物质的量的钠分别在足量的氧气和氯气中燃烧,转移的电子数相等
D.1.5 mol NO2与足量H2O反应,转移的电子数为2NA难度: 中等查看答案及解析
-
某课外实验小组设计的下列实验不合理的是( )
A.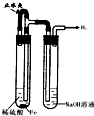
制备并观察氢氧化亚铁
B.
证明过氧化钠与水反应放热
C.
制备并收集少量NO2气体
D.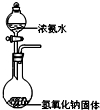
实验室制备少量氨气难度: 中等查看答案及解析
-
在100mL某混合溶液中,c(HNO3)=0.4mol•L-1,c(H2SO4)=0.1mol•L-1,现向混合液中加入1.92g铜粉,微热,充分反应后溶液中Cu2+的物质的量浓度约为(假设反应前后溶液的体积保持不变)( )
A.0.15 mol/L
B.0.225 mol/L
C.0.3 mol/L
D.0.6 mol/L难度: 中等查看答案及解析
-
16.8g NaHCO3和7.8gNa2O2在密闭容器中灼烧,充分反应后,将密闭容器保持温度为500℃.最后容器内的物质是( )
A.Na2CO3、Na2O2、O2
B.NaHCO3、Na2CO3、O2
C.Na2CO3、NaOH、CO2、O2
D.Na2CO3、O2、H2O(g)难度: 中等查看答案及解析
-
一定量的氢气在氯气中燃烧,所得混合物用100mL 3.00mol•L-1的NaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.10mol,则反应的氢气和氯气的物质的量之比n(H2):n(Cl2)是( )
A.3:2
B.1:3
C.4:1
D.1:5难度: 中等查看答案及解析
-
下列反应的离子方程式正确的是( )
A.铜溶于浓硝酸:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
B.氯化铝溶液与过量氨水反应:Al3++4NH3•H2O=AlO2-+4NH4++2H2O
C.氯气与水反应:Cl2+H2O=2H++Cl-+ClO-
D.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO难度: 中等查看答案及解析
-
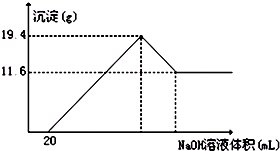
某同学用NaHCO3和KHCO3组成的混合物进行实验,测得如下数据(盐酸的物质的量浓度相等).下列分析推理不正确的是( )
50mL盐酸 50mL盐酸 50mL盐酸 m(混合物) 9.2g 15.7g 27.6g V(CO2)(标准状况) 2.24L 3.36L 3.36L
A.盐酸的物质的量浓度为3.0mol/L
B.加入混合物9.2g时盐酸过量
C.15.7g混合物未与盐酸完全反应
D.根据表中数据不能计算出混合物中NaHCO3的质量分数难度: 中等查看答案及解析
-
1.92g Cu投入到一定量的浓HNO3中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2的体积为( )
A.504mL
B.336mL
C.224mL
D.168mL难度: 中等查看答案及解析