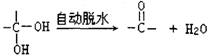
-
2010年我国“两会”“一号提案”锁定“低碳经济”.下列做法不符合“低碳经济”的是
①禁止电动自行车上路; ②以煤等燃料作为主要生活燃料; ③鼓励私人购买和使用小汽车以代替公交车; ④利用太阳能、风能和氢能等新能源代替化石燃料.
A.①②③ B.②④ C.①④ D.②③④
难度: 简单查看答案及解析
-
下列各选项所述的两个量,前者一定大于后者的是
A.同温下分别在100g水中最多能溶解的无水CuSO4和CuSO5·5H2O的质量
B.纯水在25℃和90℃时的pH值
C.25℃时,等体积的pH都等于3的盐酸和AlCl3溶液中,已电离的水分子数
D.在反应NH3+NO→N2+H2O中,被氧化和被还原的N原子数
难度: 简单查看答案及解析
-
下列说法不正确的是
A.NaCl和SiO2晶体熔化时,克服粒子间作用力的类型不相同
B.将烧黑的铜丝伸入酒精灯火焰的焰心又变红色光亮
C.氯化亚铁溶液长期敞放于空气中会因被氧化而呈黄色
D.室温下,某溶液中由水电离出的c(H+)=10
mol·L
,则此溶液可能是稀硫酸
难度: 简单查看答案及解析
-
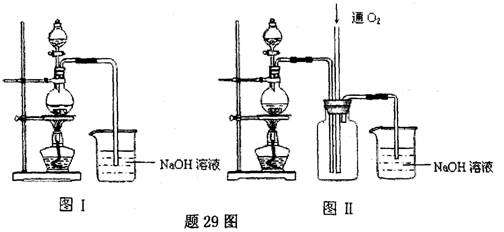
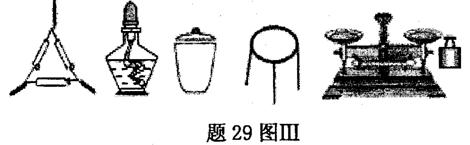
如题9图所示的实验中,能达到实验目的的是
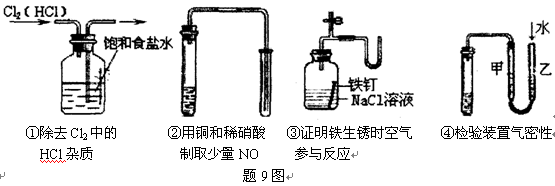
A.①②③④ B.②③④ C.③④ D.①④
难度: 简单查看答案及解析
-
已知反应mA(g)+nB(g)
qC(g)的正反应为吸热反应,m + n < q,在恒容密闭容器中反应达到平衡时,下列说法正确的是
A.A的正反应速率是B的逆反应速率的
倍
B.通入稀有气体使压强增大,平衡将逆向移动
C.若平衡时A、B的转化率相等,说明反应开始时A、B的物质的量之比为n:m
D.升高温度,混合气体的平均相对分子质量变大
难度: 简单查看答案及解析
-
海南的毒豇豆、毒黄瓜等毒蔬菜中含有禁用农药水胺硫磷,水胺硫磷的结构简式如题11图所示:对该化合物的下列叙述正确的是
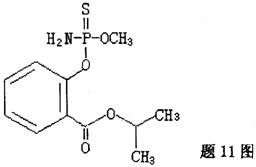
A.该化合物属于芳香烃
B.该化合物的分子式为C11H14O4NPS
C.该化合物能发生加聚反应、水解反应和酯化反应
D.该化合物中至少有7个碳原子在同一平面
难度: 简单查看答案及解析
-
下列说法正确的是
A.Na+、Fe3+、Cl
、SCN
能大量共存于同一溶液中
B.碳酸氢钠溶液与足量的氢氧化钡溶液混合后,其离子方程式为:HCO3
+ Ba2+ + OH
== BaCO3↓+H2O
C.若R
和M+的电子层结构相同,则原子序数的比较为:R>M
D.若X原子中的质子数为a,中子数为b,则X的质量数为:
难度: 简单查看答案及解析
-
有100mLMgCl2和AlCl3的混合溶液,其中c (Mg2+)为0.2mol/L,c (Cl
)为1.3mol/L,要使Mg2+转化为沉淀分离出来,至少需加2mol/L NaOH溶液体积是
A.40mL B.60mL C.80mL D.120mL
难度: 简单查看答案及解析
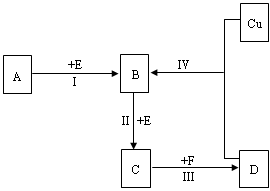
 (弱碱性,易被氧化)
(弱碱性,易被氧化)