-
向AgNO3溶液中加人一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液.关于该滤渣和滤液有下列四种说法:①向滤渣中加入稀盐酸,一定有气泡产生.②向滤液中加入稀盐酸,一定有沉淀产生.③滤渣中一定含有Ag.④滤液中一定含有Fe(NO3)2,一定不含AgNO3,可能含有Al(NO3)3.以上说法正确的个数为( )
A.0个
B.1个
C.2个
D.3个难度: 中等查看答案及解析
-
下列现象中,不是化学变化引起的是( )
A.古建筑中石像变模糊
B.地下煤层自燃
C.溶洞的形成
D.北方湖面出现“冬捞碱夏盐”难度: 中等查看答案及解析
-
饮料中的果味大多来自酯类.丁酸乙酯(C6H12O2)是无色具有菠萝香味的液体,常用作食品、饮料的调香剂.下列叙述中正确的是( )
A.丁酸乙酯是由20个原子构成的
B.丁酸乙酯中碳元素的质量分数为27.6%
C.丁酸乙酯中碳、氢、氧元素的质量比为18:3:8
D.一个丁酸乙酯分子中,碳、氢、氧原子的个数比为3:6:2难度: 中等查看答案及解析
-
下列图示实验操作中,正确的是( )

A.①④
B.①②④
C.①③④
D.①②③④难度: 中等查看答案及解析
-
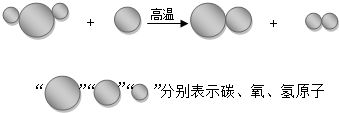
在一定条件下,置于密闭容器中的下列各组物质,充分反应后,再冷却至常温.密闭容器中有气态物质且属于纯净物的是( )
A.质量比为1:8的H2和O2
B.质量比为3:9的C和O2
C.质量比为1:4的CH4和O2
D.质量比为7:2的CO和O2难度: 中等查看答案及解析
-
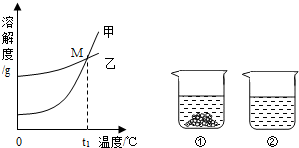
下列图形能正确反映对应变化关系的是( )
A B C D 
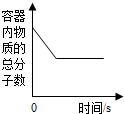
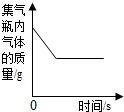

加热一定量氯酸钾和二氧化锰混合物 在密闭容器中,甲烷完全燃烧 碳在盛有氧气的密闭集气瓶内燃烧 电解水
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
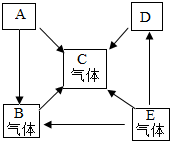
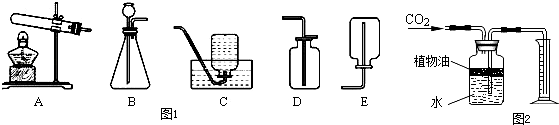
有关下图中甲、乙、丙、丁所示实验的说法错误的是( )
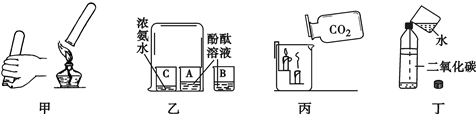
A.甲实验目的是检验氢气的纯度,如果听到尖锐的爆鸣声,则氢气不纯
B.乙实验既证明浓氨水易挥发,也说明分子是不断运动的
C.丙实验可证明通常情况下二氧化碳的密度比空气大且二氧化碳不能燃烧也不支持燃烧
D.丁实验既可证明二氧化碳能溶于水也可证明二氧化碳能与水反应难度: 中等查看答案及解析
-
实验室里,用如图所示装置还原氧化铁的过程中,可能生成四氧化三铁、氧化亚铁或铁等固体物质.关于该实验,下列说法不正确的是( )
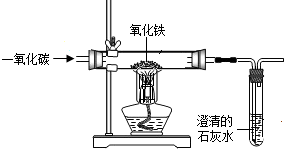
A.实验开始时,应该先点燃酒精灯,一段时间后再通入一氧化碳
B.实验过程中,试管中澄清的石灰水变浑浊,证明该反应有二氧化碳生成
C.实验结束后,玻璃管中红色的氧化铁粉末变成黑色,该产物不一定是铁
D.该反应中,一氧化碳转化为无毒无害的二氧化碳,故不需要尾气处理装置难度: 中等查看答案及解析