-
我国古代科技发达,下列有关古代文献的说法错误的是
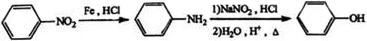
A.明朝的《本草纲目》记载“烧酒非古法也,自元时创始,其法用浓酒和糟入甑(指蒸锅),蒸令气上,用器承滴露。”该段文字记载了白酒(烧酒)的制造过程中采用了蒸馏的方法来分离和提纯。
B.汉朝的《淮南万毕术》、《神农本草经》记载“白青(碱式碳酸铜)得铁化为铜”,“石胆……能化铁为铜”都是指铜可以采用湿法冶炼。
C.清初《泉州府志》物产条载: “初,人不知盖泥法,元时南安有黄长者为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之
。”该段文字记载了蔗糖的分离提纯采用了黄泥来吸附红糖中的色素。
D.晋代葛洪的《抱朴子》记载“丹砂烧之成水银,积变又成丹砂”,是指加热时丹砂(HgS)熔融成液态,冷却时重新结晶为HgS晶体。
难度: 困难查看答案及解析
-
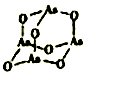
分枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述正确的是
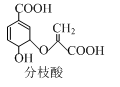
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
难度: 中等查看答案及解析
-
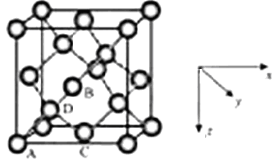
A、B、C三种物质中均含有同一种元素M,它们之间有如下图所示的转化关系,(部分反应物质已略去)。A为一种金属单质,反应①②③均为化合反应,反应④为置换反应。下列有关说法正确的是
A.①中所加试剂只能是Cl2
B.③中需要加具有还原性的试剂
C.A与稀硝酸反应一定能实现元素M 在①中发生的价态变化
D.元素M在②中发生的价态变化也能通过加KI溶液实现
难度: 中等查看答案及解析
-
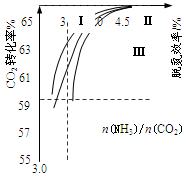
已知:(HF)2(g)
2HF(g) ΔH>0,且平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
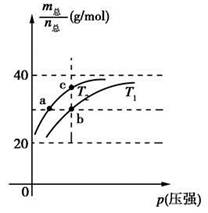
A.温度:T1<T2 B.平衡常数:K(a)=K(b)<K(c)
C.反应速率:vb>va D.当
=30g·mol-1时,n(HF):n[(HF)2]=2:1
难度: 困难查看答案及解析
-
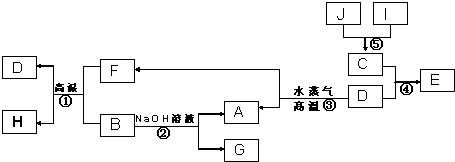
某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如下图所示,下列说法不合理的是
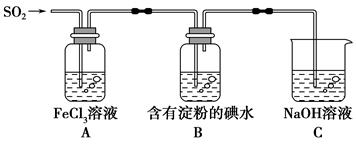
A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液退色
B.装置C的作用是吸收SO2尾气,防止污染空气
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀
D.为了验证A中发生了氧化还原反应,加入KMnO4溶液,紫红色退去
难度: 困难查看答案及解析
-
将足量的KHCO3溶液不断滴入含等物质的量的KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与滴入的KHCO3溶液体积的关系可表示为
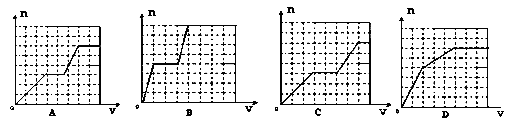
难度: 极难查看答案及解析
-
溶液X中含有右表中的某5种,且其浓度均为 0.1mol/L(不考虑水的电离与离子水解)。向X溶液加入足量稀盐酸,有无色气体生成,经分析反应前后阴离子种类没有变化。下列叙述不正确的是
阳离子
Na+、Ca2+、Fe2+、Al3+、Fe3+、Mg2+
阴离子
OH-、HCO3-、CO32-、Cl-、NO3-、SO42-
A.X溶液中不可能含有HCO3-或CO32-
B.生成无色气体的离子方程式为:3Fe2+ +NO3-+4H+=3Fe3++NO+2H2O
C.根据电荷守恒,原溶液中一定含Mg2+
D.X溶液中一定含3种阳离子、2种阴离子
难度: 极难查看答案及解析