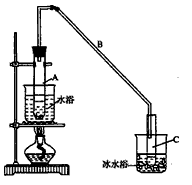
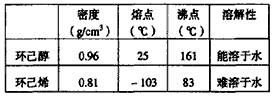
-
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏
B.萃取、蒸馏、分液
C.分液、蒸馏、萃取
D.蒸馏、萃取、分液
难度: 中等查看答案及解析
-
下列描述正确的是( )
A. HCl和NaOH反应的中和热△H=﹣57.3kJ/mol,则H2SO4和Ba(OH)2反应生成1molH2O时会放出57.3kJ的热量。
B. 已知氢氢键键能为akJ/mol,氯氯键键能为bkJ/mol,氢氯键键能为ckJ/mol,则生成1molHCl放出的能量为(a+b-2c)/2kJ
C. 需要加热才能发生的反应一定是吸热反应
D. CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的反应热为:△H=+2×283.0kJ/mol
难度: 中等查看答案及解析
-
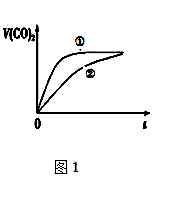
某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
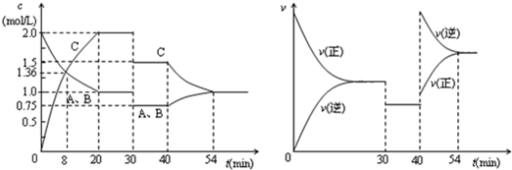
A.30min时降低温度,40min时升高温度
B.反应方程式中的x=1,正反应为吸热反应
C.8min前A的平均反应速率为0.08mol/(L•min)
D.30min~40min间该反应使用了催化剂
难度: 困难查看答案及解析
-
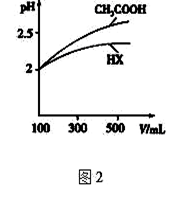
常温下,下列关于粒子浓度大小比较正确的是( )
A. 0.1mol/L的HF溶液和0.1mol/L的NaOH溶液等体积混合:c(Na+)+c(OH-)>c(H+)+c(F-)
B. 向0.10mol/LNaHSO3溶液中通入NH3至溶液pH=7 (体积变化可忽略):c(Na+)>c(NH4+)>c(SO32-)
C. 0.3mol的SO2通入1L0.4mol/L的NaOH溶液中:4c(Na+)=3c(HSO3-)+3c(SO32-)+3c(H2SO3)
D. pH=4的CH3COOH溶液和pH=10的KOH溶液等体积混合:2c(K+)+c(H+)= c(OH-)+ c(CH3COOH)+ 2c(CH3COO-)
难度: 困难查看答案及解析
-
一种碳纳米管能够吸附氢气,用这种材料制备的二次电池原理如下图所示,该电池的电解质溶液为6 mol/L的 KOH溶液。
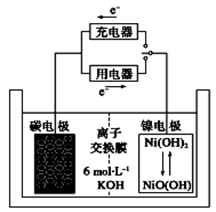
下列说法中正确的是( )
A. 放电时K+ 移向负极
B. 放电时电池正极的电极反应为NiO(OH) + H2O + e- = Ni(OH)2 + OH-
C. 放电时电池负极的电极反应为H2 - 2e- = 2H+
D. 该电池充电时将碳电极与外接电源的正极相连
难度: 中等查看答案及解析
-
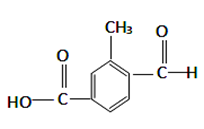
分枝酸可用于生化研究,其结构简式如图。
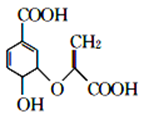
下列关于分枝酸的叙述正确的是( )
A. 分枝酸的分子式为C10H12O6
B. 分枝酸属于芳香化合物
C. 分枝酸能发生酯化反应、加成反应
D. 分枝酸分子中含有3种官能团
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 丙烷没有同分异构体
B. CH(CH3)2CH2CH2CH3 的一氯代物有4种
C. 二氯苯有3种,则四氯苯有6种
D. CH3OH与CH2OH-CH2OH都属于醇,互为同系物
难度: 中等查看答案及解析
-
10mL某种气态烃,在50mL氧气中完全燃烧,得到液态水和体积为35mL的混合气体(所有气体体积都是在同温同压下测定),则下列烃中符合题意的烃是( )
A. CH4 B. C2H2 C. C3H8 D. C2H6
难度: 困难查看答案及解析
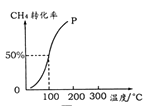
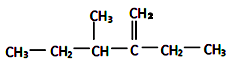
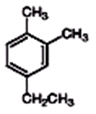 此烃的名称为_______________
此烃的名称为_______________