-
下列做法不符合“节能降耗、保护环境”这一主题的是( )
A.合理和综合利用煤和石油
B.研制开发太阳能电池、氢能电池等
C.大量使用农药化肥提高粮食产量
D.推广垃圾的分类存放、回收和处理难度: 中等查看答案及解析
-
一种新型高效净水剂的化学式为:AlFe(OH)nCl6-n,是以工业生产废料为原料制取的,广泛应用于工业污水的处理.该净水剂中铁元素的化合价为( )
A.0
B.+2
C.+3
D.+6难度: 中等查看答案及解析
-
下列说法不正确的是( )
A.空气中氮气和氧气的体积比约为:4:1
B.CO2使澄清石灰水变浑浊,描述的是化学性质
C.C60 又名足球烯,是一种单质
D.加热KClO3和MnO2混合物后,剩余固体质量减少,故不满足质量守恒定律难度: 中等查看答案及解析
-
打火机给人们生活带来方便,如图是普通电子打火机的实物照片.下面可以做到符合燃烧条件能打火的组合是( )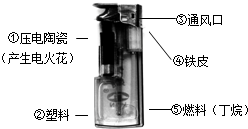
A.①③⑤
B.①③④
C.①②③
D.①②④难度: 中等查看答案及解析
-
X、Y、Z、是三种不同的金属,为比较金属活动性的大小,某同学利用这三种金属单质、盐酸、Z的硝酸盐进行有关实验,结果如下:Y和Z可与盐酸反应,X不能与盐酸反应,且Y 能将Z从Z的硝酸盐中置换出来,那么这三种金属的活动性顺序为( )
A.Y>X>Z
B.X>Y>Z
C.X>Y>Z
D.Y>Z>X难度: 中等查看答案及解析
-
“贵州醇”中的溶质是酒精,有着独特的香味,其主要成分是乙醇,化学式为C2H5OH,下列有关说法正确的是( )
A.乙醇由2个C原子,6个H原子,1个O原子构成
B.乙醇的相对分子质量是46克
C.乙醇属于有机物,广泛用作燃料
D.乙醇中碳元素,氢元素,氧元素之间的质量比是2:6:1难度: 中等查看答案及解析