-
下列化学用语表示正确的是 ( )
A.小苏打电离方程式:NaHCO3 = Na+ + H+ + CO32-
B.Cl-的结构示意图:
C.H2O的电子式:
D.乙烯的最简式:C2H4
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值。下列判断正确的是 ( )
A.32克O2和O3组成的混合气体中含有的氧原子数目为2NA
B.常温常压下,22.4 L乙醇含有的分子数目为NA
C.1 mol Na变为Na+时得到的电子数目为NA
D.44克14C16O2含氧原子数为2NA
难度: 中等查看答案及解析
-
下列叙述正确的是 ( )
A.H2O的摩尔质量为18g
B.3.01×1023个SO2分子的质量为32g
C.标准状况下,1 mol任何物质体积均为22.4L
D.将0.1mol NH3溶于1L水,配成溶液中溶质的物质的量浓度为0.1mol/L
难度: 简单查看答案及解析
-
下列物质分离方法不正确的是 ( )
A.用过滤的方法除去食盐水中的泥沙
B.用蒸馏的方法将自来水制成蒸馏水
C.用酒精萃取碘水中的碘
D.用分液的方法分离汽油和氯化钠溶液
难度: 中等查看答案及解析
-
从物质的组成分类看,碳酸氢钠属于 ( )
A.酸 B.碱 C.盐 D.氧化物
难度: 简单查看答案及解析
-
下列各组离子中,能在同一溶液中大量共存,加入一小块钠后仍能大量共存的是 ( )
A.Na+、K+、Cl-、CO32- B.Cu2+、Na+、SO42-、NO3-
C.Ba2+、K+、Cl-、SO42- D.K+、Na+、HCO3-、CO32-
难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是 ( )
A.铁和盐酸反应 2Fe+6H+ = 2Fe3++3H2↑
B.小苏打溶液与少量澄清石灰水混合:Ca2++OH-+HCO3-=CaCO3↓+H2O
C.AlCl3溶液中加入足量的氨水:Al3+ + 3OH- ═Al(OH)3↓
D.Na2CO3溶液中通入少量CO2:CO32-+ CO2+ H2O=2HCO3-
难度: 中等查看答案及解析
-
黑火药发生爆炸,反应方程式为S+2KNO3+3C=K2S+N2↑+3CO2↑,下列说法错误的是 ( )
A.C在反应中被还原
B.S和KNO3都发生了还原反应
C.每生成3molCO2,反应转移12mol电子
D.K2S和N2都是反应的还原产物
难度: 中等查看答案及解析
-
下列变化中,既属于吸热反应,又属于氧化还原反应的是( )
A.碳酸钙受热分解 B.灼热的木炭与二氧化碳反应
C.铝粉与盐酸的反应 D.硝酸铵溶于水
难度: 中等查看答案及解析
-
将锌片和铜片用导线连接置于稀硫酸溶液中,下列各叙述正确的是 ( )
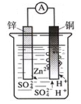
A.锌片做负极,锌发生还原反应
B.铜片做正极,铜得电子
C.溶液中的pH值减小
D.铜片上有气泡冒出
难度: 中等查看答案及解析
-
用FeCl3溶液无法区别的一组试剂是 ( )
A.KSCN溶液、KCl溶液 B.NaOH溶液、NaCl溶液
C.稀盐酸、稀硝酸 D.AgNO3溶液、稀HNO3
难度: 中等查看答案及解析
-
从降低成本和减少环境污染的角度考虑,制取硝酸铜最好的方法是 ( )
A.铜和浓硝酸反应 B.铜和稀硝酸反应
C.氧化铜和硝酸反应 D.氯化铜和硝酸银反应
难度: 中等查看答案及解析
-
下列有关实验操作、现象和解释或结论都正确的是( )
选项
实验操作
现象
解释或结论
A
过量的铁粉加入稀硝酸中,充分反应后,滴入KSCN溶液
溶液呈红色
稀硝酸将Fe氧化为Fe2+
B
AlCl3溶液中滴加过量的氨水
先出现白色沉淀,后沉淀又逐渐溶解
氢氧化铝能溶于氨水
C
铝箔插入稀硝酸中
无明显现象
铝箔表面被稀硝酸氧化形成致密的氧化膜
D
用玻璃棒蘸取浓硫酸点到pH试纸上
试纸变黑色
浓硫酸具有脱水
难度: 困难查看答案及解析
-
下列有关物质的性质与应用的说法中,均正确的是 ( )
A.石英能导电,所以用作光导纤维
B.明矾与水反应生成氢氧化铝胶体,可用于自来水消毒
C.氧化铝熔点高,常用于耐高温材料
D.苏打溶液呈弱碱性,可用作胃酸中和剂
难度: 简单查看答案及解析
-
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是 ( )
A.原子半径:Z>W>X>Y
B.元素X、Y、Z、W的最高化合价分别与其主族序数相等
C.最简单气态氢化物的热稳定性:Y>X>W>Z
D.最高价氧化物对应水化物的酸性:X>W>Z
难度: 中等查看答案及解析
-
14C可用于考古,“14”是指 ( )
A. 质量数 B. 核外电子数 C. 中子数 D. 质子数
难度: 简单查看答案及解析
-
已知一定条件下断裂或生成某些化学键的能量关系如下表:
断裂或生成的化学键
能量数据
断裂1mol H2分子中的化学键
吸收能量436 kJ
断裂1mol I2分子中的化学键
吸收能量151 kJ
形成1mol HI分子中的化学键
释放能量299 kJ
对于反应:H2 + I2=2 HI,下列说法正确的是( )
A.该反应为放热反应
B.该反应中反应物总能量低于生成物总能量
C.HI分子中的化学键比H2分子中的化学键更牢固
D.无法判断
难度: 中等查看答案及解析
-
反应3H2+N2
2NH3在密闭容器中进行。下列关于该反应的说法错误的是 ( )
A.升高温度能加快反应速率
B.使用恰当的催化剂能加快反应速率
C.增大N2的浓度能加快反应速
D.平衡时各组分含量之比一定等于3:1:2
难度: 中等查看答案及解析
-
在一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应2HI(g)
H2(g)+I2(g),2s 时生成0.1 mol H2,则以HI表示该时段的化学反应速率是
( )
A.0.05 mol·Lˉ1·sˉ1
B.0.1 mol·Lˉ1·sˉ1
C.0.2 mol·Lˉ1·sˉ1
D.0.8 mol·Lˉ1·sˉ1
难度: 中等查看答案及解析
-
一定温度下,恒容容器中发生可逆反应C(s)+ 2H2O(g)
CO2(g) + 2H2(g),一定能说明该反应已达到平衡状态的是 ( )
A.生成1molCO2的同时消耗2molH2O
B.n(H2O):n(H2)=1:1
C.2v正(H2O)=v逆(CO2)
D.容器中气体的压强不发生变化
难度: 中等查看答案及解析
-
下列反应属于加成反应的是 ( )
A. 2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑
B.
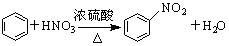
C.

D.
难度: 中等查看答案及解析
-
下列各组中,互称为同分异构体的是 ( )
A.O2与O3
B.35Cl与37Cl
C.CH3CHO与
D.CH4与C2H6
难度: 简单查看答案及解析
-
阿司匹林双名乙酰水杨酸,推断它不应具有的性质( )
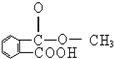
A.与NaOH溶液反应
B.与金属钠反应
C.与乙酸发生酯化反应
D.与乙醇发生酯化反应
难度: 中等查看答案及解析
-
某有机物的结构简式为:HO—CH2—CH
CH—COOH,现有①氯化氢、②溴水、③纯碱溶液、④乙醇、⑤酸性高锰酸钾溶液,试根据该有机物的结构特点,判断在一定条件下,能与其反应的物质是( )
A.只有②④⑤ B.只有①③④ C.只有①②③⑤ D.①②③④⑤
难度: 困难查看答案及解析
-
糖类、油脂、蛋白质为食物中的基本营养物质。下列有关说法正确的是 ( )
A.油脂的主要成分是高级脂肪酸甘油酯
B.糖类、油脂、蛋白质都能发生水解反应
C.糖类、油脂、蛋白质中都只含C、H、O三种元素
D.淀粉、纤维素分子组成都可表示为(C6H10O5)n,二者互为同分异构体
难度: 中等查看答案及解析
-
C、N、O、Al、Si 、Cl、Fe是七种常见元素
(1)N元素位于周期表第 周期,第 族。
(2)用“>”、“<”或“= ”填空:
离子半径
得电子能力
酸性
金属性
O2― Al3+
16O 18O
H2CO3 HNO3
Fe Al
(3)SiO2及硅酸盐在自然界广泛存在,在日常生活、生产、科研及新型材料等方面有着重要的用途。高岭土[Al2(Si2O5)(OH)4]改写成氧化物的形式为 。
(4)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并用单线桥标出电子转移的方向和数目: 。
(5)将铝片(表面除去氧化膜)与碳棒用导线连接后插入稀NaOH溶液中可以构成原电池,电池正极为 ,电池负极反应的电极方程式为 。
难度: 困难查看答案及解析