-
下列说法不正确的是
A. 常温下铁与浓硫酸不反应 B. 燃着的镁能在二氧化碳气体中继续燃烧
C. 干燥的氯气能使品红溶液褪色 D. 久置于空气中的漂白粉会变质
难度: 中等查看答案及解析
-
下列说法不正确的是
A. 碘单质升华克服的是分子间作用力
B. KOH和MgCl2都是离子晶体,均含有共价键和离子键
C. 石英是由硅原子和氧原子构成的原子晶体,每个原子的最外层都具有8电子稳定结构
D. KClO3分解生成KC1和O2的过程中有离子键和共价键的断裂和形成
难度: 中等查看答案及解析
-
下列属于碱的是( )
A. CH3COOH B. CuCl2 C. Ba(OH)2 D. N2O4
难度: 简单查看答案及解析
-
下列属于非电解质的是( )
A. 蔗糖 B. 镁粉 C. 硫酸 D. 胆矾晶体
难度: 简单查看答案及解析
-
能产生“丁达尔效应”的是( )
A. 肥皂水 B. 石灰水 C. 双氧水 D. 氯水
难度: 简单查看答案及解析
-
下列过程中,发生吸热反应的是( )
A. 碘的升华 B. 生石灰溶于水
C. Ba(OH)2·8H2O 与NH4Cl D. 盐酸和氢氧化钠溶液混合
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 制硝基苯时,将浓硝酸沿着内壁慢慢注入盛有浓硫酸的烧杯中,并用玻璃棒不断搅拌
B. 用玻璃棒在过滤器上搅拌以加速硫酸钡沉淀的洗涤
C. 实验室中少量金属钠常保存在煤油中,实验时多余的钠不能放回原瓶中
D. 根据火焰所呈现的特征焰色,用来检验金属或金属离子的存在
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A. C60和纳米碳管互为同素异形体 B. (CH3CH2)2CHCH3的系统命名是2-乙基丁烷
C. 乙醇和丁烷都存在同分异构体 D. 甲烷与新戊烷互为同系物
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 油脂和氨基酸在一定条件下均可以与氢氧化钠溶液反应
B. 棉、麻、丝、毛完全燃烧都只生成二氧化碳和水
C. 鸡蛋白水溶液中滴加硫酸铵溶液可使蛋白质发生变性
D. 煤的干馏是指高温下煤在空气中发生复杂的物理化学变化,得到苯、甲苯、二甲苯等
难度: 简单查看答案及解析
-
固体粉末X中可能含有Fe、FeO、CuO、MnO2、KCl和K2CO3中的若干种。为确定该固体粉末的成分,某同学依次进行了以下实验:
①将X加入足量水中,得到不溶物Y 和溶液Z
②取少量Y加入足量浓盐酸,加热,产生黄绿色气体,并有少量红色不溶物
③用玻璃棒蘸取溶液Z滴于广范pH试纸上,试纸呈蓝色
④向Z溶液中滴加AgNO3溶液,生成白色沉淀
分析以上实验现象,下列结论正确的是( )
A. X中一定不存在FeO
B. 不溶物Y中一定含有MnO2和CuO,而Fe与FeO中至少含有一种
C. Z溶液中一定含有K2CO3
D. 向④中所生成的白色沉淀中滴加盐酸,若沉淀不完全溶解,则粉末X中含有KCl
难度: 中等查看答案及解析
-
仪器名称为“干燥管”的是
A.
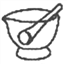 B.
B. C.
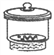 D.
D. 
难度: 简单查看答案及解析
-
下列反应中,非金属单质只作氧化剂的是( )
A. Br2+2NaOH=NaBr+NaBrO+H2O B. 2Al+2NaOH+2H2O=2NaAlO2+3H2↑
C. C+2CuO
2Cu+CO2↑ D. 4Fe(OH)2+O2+2H2O=4Fe(OH)3
难度: 简单查看答案及解析
-
下列表示不正确的是
A. CO2的电子式:
B. 乙烯的结构简式:CH2CH2
C. 水分子的球棍模型:
 D. Na+的结构示意图:
D. Na+的结构示意图: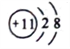
难度: 中等查看答案及解析
-
下列物质的水溶液因电离而呈酸性的是( )
A. NH4Cl B. Na2CO3 C. NaHSO4 D. CH3CH2OH
难度: 中等查看答案及解析
-
在一定条件下发生反应2SO3(g)
2SO2(g)+O2(g),将1mol SO3气体通入1L容积恒定的密闭容器中,维持容器内温度不变,5 min末测得SO3的物质的量为0.4 mol。则下列说法正确的是( )
A. 0~5 min,O2的生成速率v(O2)=0.06 mol·L-1·min-1
B. 若起始时充入3 mol SO3,起始时SO3分解速率不变
C. 若某时刻消耗了0.5 mol SO3同时生成了0.25 mol O2,则表明该反应达到了平衡状态
D. 达到平衡时,SO2和SO3的浓度相等
难度: 简单查看答案及解析
-
下列离子方程式不正确的是( )
A. 硫酸型酸雨的形成会涉及反应:2H2SO3+O2=4H++2SO42-
B. 纯碱溶液显碱性的原因:CO32-+2H2O
H2CO3+2OH-
C. 盛放NaOH溶液的试剂瓶不能用玻璃塞的原因:SiO2+2OH-=SiO32-+H2O
D. 成分为盐酸的洁厕灵与“84”消毒液混合使用易中毒:Cl-+ClO-+2H+=Cl2↑+H2O
难度: 简单查看答案及解析
-
甲~庚等元素在周期表中的相对位置如下表,己的最高价氧化物的水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是( )
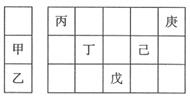
A. 丙与戊的原子序数相差25
B. 气态氢化物的稳定性:庚<己<戊
C. 丁的最高价氧化物可用于制造光导纤维
D. 常温下,甲和乙的单质能与水剧烈反应
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A. 乙醇、乙酸、乙酸乙酯都能发生取代反应
B. 石油裂化和裂解的目的均是为了将长链烃转化为短链烃
C. 石油裂化得到的汽油可使溴水、酸性高锰酸钾溶液褪色,褪色原理不同
D. 等物质的量的乙烯、丙烯分别充分燃烧,所耗氧气的物质的量一样多
难度: 中等查看答案及解析
-
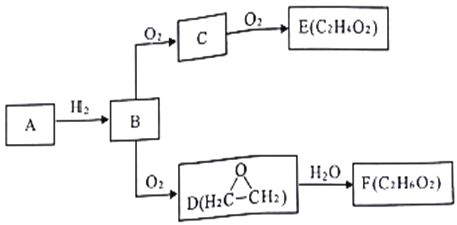
某高能电池以稀硫酸作为电解质溶液,其总反应式为CH2=CH2+O2
CH3COOH。下列说法正确的是( )
A. 在电池工作过程中,溶液中的SO42-向正极移动
B. 随着反应的进行,正极区域附近溶液的pH变小
C. 当转移4mol电子时,溶液中的CH3COOH分子数为NA(NA为阿伏加德罗常数的值)
D. 负极的电极反应式为CH2=CH2-4e-+2H2O
CH3COOH+4H+
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 含有OH-的溶液一定呈碱性
B. pH为3的盐酸的c(H+)是pH为1的盐酸的100倍
C. Na2CO3溶液与NaHCO3溶液中所含微粒的种类一定相同
D. pH相同的氨水与氢氧化钠溶液,分别与同浓度同体积的盐酸完全中和时,消耗氨水与氢氧化钠溶液的体积一定相同
难度: 中等查看答案及解析
-
25 ℃、101 kPa时,有以下能量转化图,下列说法不正确的是

A. 转化Ⅱ的热化学方程式2CO(g)+O2(g)2CO2(g) ΔH=-282.9 kJ·molˉ1
B. 相同条件下,1 mol C(g)和0.5 mol O2(g)总能量高于1 mol CO(g)的能量
C. 由C→CO的热化学方程式2C(s)+O2(g)2CO(g) ΔH=-221.2 kJ·molˉ1
D. CO2(g)分解为C(s)和O2(g)是吸热反应
难度: 中等查看答案及解析
-
已知:2CrO42-+2H+
Cr2O72-+H2O。 25℃时,调节初始浓度为1.0 mol·L-1的Na2CrO4溶液的pH,测定平衡时溶液中c(Cr2O72-)和c(H+),获得如下曲线。下列说法不正确的是( )
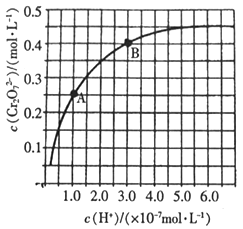
A. 平衡时,pH越小,c(Cr2O72-)越大
B. A、B两点c(CrO42-)之比为5:2
C. B点CrO42-的平衡转化率为40%
D. 平衡时,若溶液中c(CrO42-)=2c(Cr2O72-),则c(H+)=1.0×10-7mol·L-1
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 11g C3H8与CO2的混合气体中所含碳原子数可能为0.5NA
B. 标准状况下,4.48 L甲烷和乙烯的混合气体完全燃烧,产物中所含O-H键数目为0.4NA
C. 4.6 g Na与100 mL 1mol·L-1的盐酸溶液反应,转移电子数目为0.1NA
D. 常温下,1L pH=2 的硫酸溶液中由水电离出的H+的数目为0.01NA
难度: 中等查看答案及解析
-
常温下,用0.1000mol·L-1的盐酸滴定0.1000mol·L-1Na2CO3溶液25.00mL。用 pH传感器测得混合溶液的pH变化曲线如图,下列说法正确的是( )
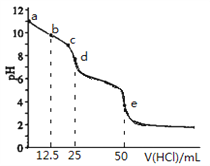
A. c→d发生的主要离子反应:HCO3-+H+=H2O+CO2
B. 在b点 时,c(CO32-)>c(HCO3)->c(OH-)
C. 在d点 时,c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
D. 在e点 时c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)
难度: 困难查看答案及解析
-
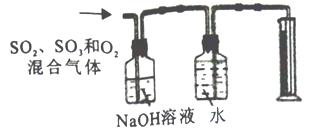
根据海水综合利用的工业流程图,判断下列说法不正确的是( )
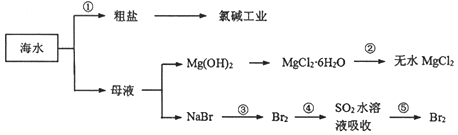
A. 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸
B. 在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2
C. 从能量转换角度看,氯碱工业电解饱和食盐水是一个将电能转化为化学能的过程
D. 从第④步到第⑤步的目的是富集Br2
难度: 中等查看答案及解析