-
在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色,有关判断正确的是( )
A. 滤渣中一定有银、没有铜和锌
B. 滤渣中一定有银和锌,可能有铜
C. 滤液中一定有硝酸锌、硝酸铜、硝酸银
D. 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
难度: 中等查看答案及解析
-
收藏家收藏的一清末铝制品至今保存仍十分完好,该铝制品不易锈蚀的主要原因是
A、铝不易发生化学反应
B、铝的氧化物易发生还原反应
C、铝易氧化,但铝表面的氧化铝膜具有保护内部铝的作用
D、铝不易氧化
难度: 中等查看答案及解析
-
小明同学在实验室中测定某未知溶液的pH,他的实验操作如下:先用蒸馏水将pH试纸润湿,然后用玻璃棒蘸取待测液于pH试纸上进行测定,你认为小明同学这样测得的结果与该溶液的实际pH比较
A. 偏低 B. 偏高 C. 不变 D. 无法判定
难度: 中等查看答案及解析
-
如图是甲乙两种固体物质的溶解度曲线,下列说法正确的是( )

A. 甲的溶解度受温度的影响比乙小
B. t1℃时,甲、乙溶解度相等
C. t2℃时,甲的饱和溶液的溶质质量分数等于30%
D. 可采用降低温度的方法使乙的饱和溶液变为不饱和溶液
难度: 简单查看答案及解析
-
将10g质量分数为20%的氢氧化钠溶液与20g质量分数为10%的硫酸溶液混合后,下列物质中不能与该溶液发生反应的是( )
A. Na2CO3 B. CuCl2 C. CO2 D. Ba(NO3)2
难度: 中等查看答案及解析
-
下列设计的实验方法或试剂,你认为正确的是
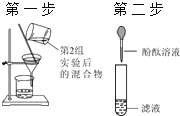
A.检验氢氧化钠是否变质(酚酞溶液)
B.鉴别氢氧化钠、氯化钠、硝酸铵三种固体物质(水)
C.分离氧化钙中混有的碳酸钙粉末(加水溶解,过滤)
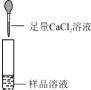
D.验证铁、铜、银的金属活动性顺序(硫酸亚铁溶液、硝酸铜溶液、银)
难度: 中等查看答案及解析
-
区分如表各组物质的两种方法都合理的是( )
A
B
C
D
区分的物质
稀硫酸和氯化钙溶液
硬水与软水
碳粉与氧化铁
氢氧化钠和硝酸铵
方案一
加入酚酞试液
加肥皂水
加入稀盐酸
加水溶解测温度变化
方案二
通入二氧化碳
测pH
观察颜色
观察状态
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列图象与对应实验相符合的是
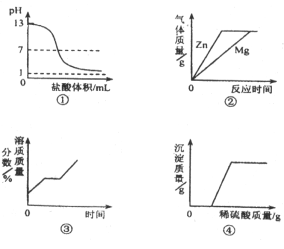
A.图①表示向pH=13的氢氧化钠溶液中逐滴加入pH=1的 盐酸
B.图②表示向溶质质量分数相同、等质量的稀硫酸中分别加入足量的金属镁和锌
C.图③表示将一定质量的不饱和硝酸钾溶液恒温蒸发至有晶体析出
D.图④表示向氢氧化钠与氯化钡的混合溶液中逐滴加入稀硫酸
难度: 困难查看答案及解析
-
甲、乙两种物质的溶解度曲线如右图所示。下列说法正确的是( )

A. a1℃时甲的饱和溶液,升温至a2℃时仍是饱和溶液
B. 乙的溶解度随温度的升高而增大
C. 相同温度时,甲的溶解度一定大于乙的溶解度
D. 分别将甲、乙的饱和溶液从a2℃将至a1℃时,所得溶液中溶质的质量分数相等
难度: 困难查看答案及解析