-
某电镀厂排放的废水中含有超量有毒重金属盐Ba(NO3)2、Cu(NO3)2、AgNO3,该厂想用氢氧化钾溶液、盐酸、硫酸三种试剂,将所排废水中的重金属离子逐一变成沉淀回收,最后得到只含一种化肥的中性溶液.假设每种试剂只用一次,每步操作恰好完全反应.请你按照所加试剂的顺序,写出生成三种沉淀的化学方程式:
第一步:______;
第二步:______;
第三步:______.难度: 中等查看答案及解析
-
有一包白色粉末,可能由碳酸钡、碳酸钠、硫酸钠、硫酸铜和氯化钡中的一种或几种组成.为了确定它的组成,某化学小组同学进行了如下探究活动:
(实验探究):
步骤1:取少量白色粉末,加足量水溶解后过滤,得到白色沉淀和无色滤液.
步骤2:取少量由步骤1得到的白色沉淀,加入足量稀硝酸后,部分沉淀溶解,并有无色气体产生.
(获得结论):
(1)原白色粉末中一定没有______(写化学式),理由是______;
(2)步骤1得到的沉淀是______(写化学式);
(3)原白色粉末的组成可能是______(写化学式).难度: 中等查看答案及解析
-
人体内的CO2排出不畅时,血液的pH会______(填“升高”“降低”或“不变”);浓硫酸敞口长期存放会自动溢出,这是因为它具有______;自来水生产中常通适量氯气杀菌消毒,氯气与水反应的产物之一是盐酸,使水中含有了氯离子,检验氯离子常用______和______.
难度: 中等查看答案及解析
-
(2005•普宁市二模)在H、O、C、Cl、Ca五种元素中,选择适当元素,组成符合下列要求的物质,将其化学式填入空格中.
①可用于人工降雨的氧化物______②可用于金属层表面除锈的酸______
③可改良酸性土壤的碱______ ④可作建筑材料的盐______.难度: 中等查看答案及解析
-
下列四种物质,每一种中均有一种物质与其它物质所属类别明显不同,请你在下面的横线上填写出这种物质的化学式:
①石灰石、粗盐、生铁、胆矾 ②冰、干冰、金刚石、氧化镁
③碳酸钠、硫酸铵、苛性钠、锰酸钾 ④碳酸、甲醇、乙醇、乙酸
①______ ②______ ③______ ④______.难度: 中等查看答案及解析
-
下列化学肥料属于复合肥料的是______.
①KH2PO4 ②NH4Cl ③NH4NO3 ④K2SO4.难度: 中等查看答案及解析
-
经实验测得某一溶液由Na+、Mg2+、Cl-、SO42-四种离子组成,其中Na+、Mg2+、SO42-的个数比为4:3:1,则可推断该溶液中Na+、SO42-、Cl-离子的个数比为______.
难度: 中等查看答案及解析
-
某溶液中仅含有AgNO3和Cu(NO3)2两种溶质,某校初三学生课外活动小组的同学将其分为A、B、C三份,各加入一定量的铁粉,充分反应后过滤、洗涤,得到滤液和滤渣.
①若将A得到的滤渣加入到稀盐酸中有气泡产生,则滤液中一定有______.
②若将B得到的滤渣加入到稀盐酸中没有气泡产生,则滤渣中一定有______.
③若向C得到的滤液中滴加稀盐酸,有白色沉淀生成,则滤液中含有的溶质是______,滤渣中含有的物质是______.难度: 中等查看答案及解析
-
已知某溶液里大量含有Ag+、Ba2+、Cu2+等三种阳离子中的一种离子和Cl-、OH-、CO32-等三种阴离子中的两种离子,则该溶液里大量存在的离子有______.
难度: 中等查看答案及解析
-
鉴别①MgSO4②NaOH ③CuSO4④KCl四种溶液,不用其它试剂,可用先鉴别出来的物质鉴别剩余溶液,则被鉴别出来的物质的顺序为______.
难度: 中等查看答案及解析
-
托盘天平两边烧杯中盛有从同一瓶中倒出的质量相同的足量稀硫酸,调节天平指针至平衡.向左边烧杯中加入5.6g铁粉,向右边烧杯加入Mg与MgO的混合粉末5.6g,充分反应后,天平仍保持平衡状态,则右边混合粉末中Mg与MgO的质量比为______.
难度: 中等查看答案及解析
-
根据要求书写化学方程式:
(1)市售紫葡萄的表皮上常附有一种浅蓝色的斑点,它是为了防治葡萄霉菌而喷洒的农药波尔多液.波尔多液可由硫酸铜溶液与石灰水混合制得,配制时不能用铁制容器.其中石灰水可由生石灰与水反应得到,而生石灰可由煅烧石灰石得到.按下列要求写出以上叙述中涉及反应的化学方程式:
化合反应______;
分解反应______ CaO+CO2↑难度: 中等查看答案及解析
-
(2006•珠海模拟)如图,在一只倒扣的大烧杯中,正放两只小烧杯,其中A杯中盛有足量浓盐酸,B杯中盛有少量滴有酚酞的NaOH溶液.请回答:
(1)放置一段时间后,B杯中会有怎样的现象?______
(2)上述现象能说明浓盐酸具有的物理性质为______;
上述现象说明盐酸具有的化学性质为______.难度: 中等查看答案及解析
-
某硝酸钠溶液中混有少量NaCl、Na2SO4和Na2CO3杂质,仅提供3种药品:AgNO3溶液、BaCl2溶液和稀盐酸.请设计合理的顺序将杂质逐一除去,并填写下面实验报告.(简要回答)
实验步骤 实验现象 化学方程式 加入适量的______ 有______产生 ______ 加入适量的______ 有______产生 ______ 加入适量的______ 有______产生 ______ 难度: 中等查看答案及解析
-
水蒸气通过炽热的焦炭得到的水煤气,其主要成分是CO和H2,还含有少量CO2和水蒸气,请用下列装置设计一个实验,以证明水煤气中含有CO和H2.
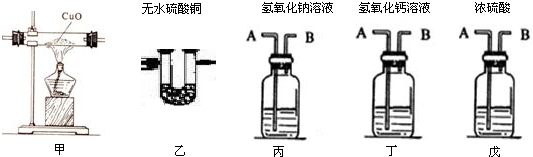
(1)连接上述所有装置的正确顺序是(用甲、乙、丙、丁、戊填入横线上):
水煤气→______→______→______→______→______
(2)装置丁在连接时,气体必须由______进入(用“A”或“B”填写)
(3)确认水煤气中含有H2的实验现象主要是______.
(4)确认水煤气中含有CO的实验现象主要是______.
(5)上述实验有何安全缺陷:______.你认为应如何改进______.难度: 中等查看答案及解析
-
有一包粉末,可能由NaCl、Na2CO3、Na2SO4、FeCl3、MgCl2中的一种或几种组成,现做如下试验:①取少量粉末,加水溶解的无色透明溶液;②取①所得溶液少许加入氢氧化钠溶液,看不到明显现象;③另取少量粉末滴加稀盐酸,也看不到明显现象.试回答:
(1)根据上述实验,可得知原粉末中可能有的物质为______.
为了确定原粉末是纯净物还是混合物,继续如下实验:④取①所得溶液少许,滴加溶液A,有白色沉淀生成;⑤继续滴加溶液A,直至再无白色沉淀生成,静置,取上层清液少许,滴加溶液B,无明显现象.
(2)由实验④可知原粉末中一定有______;由实验⑤可知原粉末中一定没有______,试写出④⑤两实验中所用溶液A、B中溶质的化学式:A______,B______;实验④中反应的化学方程式______.难度: 中等查看答案及解析
-
(2004•云南)下图是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:
(1)欲配置100g溶质质量分数为14.6%的稀盐酸,需用这种盐酸多少毫升?(计算结果精确到0.1)盐酸(分析纯)
化学式:HCl 相对分子质量:36.5
密度:1.18g/cm3 质量分数:36%
(2)取上述配置得到的足量稀盐酸与6.5g锌充分反应后,理论上可制得氢气多少克?难度: 中等查看答案及解析
-
取一定量25%的氢氧化钠溶液,将其蒸发掉12g水后,溶液中溶质的质量分数变为40%,再向其中加入一定质量的硫酸铜溶液,恰好完全反应,所得溶液中溶质的质量分数为20%.求加入的硫酸铜溶液中溶质的质量分数.(计算结果精确到0.1%)
难度: 中等查看答案及解析