-
下列有关化学用语使用正确的是( )
A. 用
表示某微粒,则其所含电子数为A-n
B. 次氯酸的结构式:H-Cl-O
C. 乙烯的比例模型:

D. CO2的电子式:
难度: 中等查看答案及解析
-
用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如下图所示。关于其性质的描述不正确的是( )
能使溴水和酸性KMnO4溶液褪色 B、1mol该物质可与3molH2完全加成C、该物质在空气燃烧产生刺激性气体 D、 该物质属于烯烃
难度: 中等查看答案及解析
-
有关物质性质及用途的说法,正确的是( )
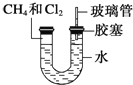
A. 甲烷与氯气在光照的条件下可以制取纯净的一氯甲烷
B. 将溴水加入己烷中,溴水的颜色变浅,这是由于发生了加成反应
C. 裂化汽油可使酸性高锰酸钾溶液褪色
D. 等质量的乙烯和聚乙烯充分燃烧所需氧气的量不相等
难度: 中等查看答案及解析
-
两种元素可以形成AB2型共价化合物的是( )
A. 无中子的原子与最外层有6个电子的短周期元素的原子
B. 核电荷数分别为12和17的元素
C. ⅣA族和ⅥA族中原子半径均为最小的元素
D. 最高正价都为奇数的两种短周期元素
难度: 中等查看答案及解析
-
硒(Se)是人体健康必需的一种微量元素,已知Se的原子结构示意图如图:
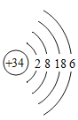 。下列说法不正确的是( )
。下列说法不正确的是( )A. 该原子的质量数为34 B. 该元素处于第四周期第ⅥA族
C. SeO2既有氧化性又有还原性 D. 酸性:HClO4>H2SeO4
难度: 简单查看答案及解析
-
NA为阿伏加德罗常数,下列说法正确的是( )
A. 标准状况下,11.2L的戊烷所含的分子数为0.5NA
B. 28g乙烯所含共用电子对数目为4NA
C. 标准状况下,11.2L二氯甲烷所含分子数为0.5NA
D. 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA
难度: 中等查看答案及解析
-
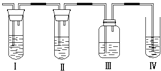
将溴水分别与酒精、己烯、己烷和四氯化碳四种试剂混合,充分振荡后静置,下列现象与所加试剂不相吻合的是
A
B
C
D
与溴水混
合的试剂
酒精
己烯
己烷
四氯化碳
现象
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
青蒿素是抗疟特效药,属于萜类化合物,如图所示有机物也属于萜类化合物,该有机物的一氯取代物有(不考虑立体异构)( )
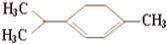
A. 6种 B. 7种 C. 8种 D. 9种
难度: 困难查看答案及解析
-
原子结构决定元素的性质,下列说法中正确的是
A. Na、Al、Cl的原子半径依次减小,Na+、Al3+、Cl-的离子半径也依次减小,
B. 在第ⅥA族元素的氢化物(H2R)中,热稳定性最强的其沸点也一定最高
C. 第二周期元素的最高正化合价都等于其原子的最外层电子数
D. 非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强
难度: 中等查看答案及解析
-
W、X、Y、Z是四种原子序数依次增大的短周期主族元素,W元素的最高正化合价与最低负化合价的代数和为0,X元素原子的电子层数是最外层电子数的3倍,Y元素原子M层上的电子数为6。则下列说法正确的是( )
A. 原子半径:Z>Y>X
B. 简单阴离子还原性:Z>Y
C. 最高价氧化物对应水化物的酸性:Z>Y
D. W与Z形成的化合物一定是易溶于水的气体
难度: 中等查看答案及解析
-
表中所列的都是烷烃,它们的一卤取代物均只有一种,分析下表中各项的排布规律,按此规律排布第6项X应为( )
1
2
3
4
5
6
X
A.
B.
C.
D.
难度: 困难查看答案及解析
-
2甲基1,3丁二烯和足量的溴发生加成反应,其加成产物中二溴代烃有(考虑顺反异构体)( )
A. 一种 B. 二种 C. 三种 D. 四种
难度: 困难查看答案及解析
-
在一定的温度、压强下,向100 mL CH4和Ar的混合气体中通入400 mL O2,点燃使其完全反应,最后在相同条件下得到干燥气体460 mL,则反应前混合气体中CH4和Ar的物质的量之比为
A. 1∶4 B. 1∶3 C. 1∶2 D. 1∶1
难度: 中等查看答案及解析
-
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性,下列说法正确的是
A. X、Y、Z、W的原子半径依次减小
B. W与X形成的化合物中只含离子键
C. W的气态氢化物的沸点一定高于Z的气态氢化物的沸点
D. 若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3
难度: 简单查看答案及解析
-
短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性, r溶液是一种常见的强酸,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是
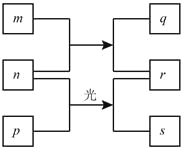
A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸
难度: 简单查看答案及解析
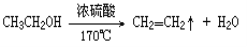 。常因温度控制不当而发生副反应,有人设计如图实验以确认上述混合气体中有乙烯和二氧化硫。
。常因温度控制不当而发生副反应,有人设计如图实验以确认上述混合气体中有乙烯和二氧化硫。