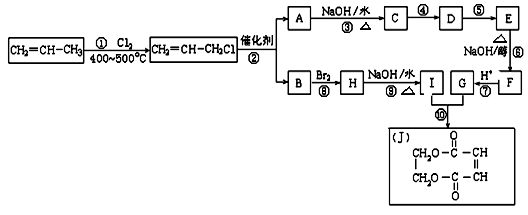
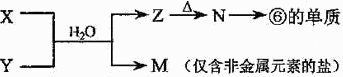-
水热反应是指在高温高压的水环境条件下,将二氧化碳转化为有机物的技术。水热反应不仅能实现二氧化碳到有机物的转化,还可以将有机质转化成矿物能源,也可将废水中的有机物转化成煤炭等资源。下列说法不正确的是
A.水热反应一定包含化学变化 B.水热反应可以实现低碳经济
C.水热反应可以改善温室效应 D.水热反应可重建地球上碳资源的和谐循环
难度: 中等查看答案及解析
-
下列对化学用语的理解正确的是
A.结构示意图
:表示C—12或
B.比例模型
:表示二氧化碳或水分子
C.电子式
:表示羟基或氢氧根离子
D.H+ + OH¯ → H2O:表示盐酸或醋酸和氢氧化钠的反应
难度: 中等查看答案及解析
-
下列有关氧化还原反应的说法正确的是
A.有单质参加,又有单质生成的反应一定是氧化还原反应
B.没有单质参加的反应,一定不是氧化还原反应
C.因为SiO2+2C=====Si+2CO↑,可由此判断非金属性碳强于硅。
D.因为氧化性F2>O2,所以氟气能和水反应,氧气不能和氟化氢反应。
难度: 中等查看答案及解析
-
下列有关物质制备的说法错误的是
A.实验室制备O2可用H2O2和MnO2为原料方便制得
B.人类社会发展史,也是人类金属冶炼史,由于化学工艺所限不活泼金属往往人类先发现并制得,随着化学发展,活泼金属逐渐被人们发现并制得,如金早于铜,铜早于铁,铁早于铝,铝早于钠。
C.工业制备镁采用电解熔融氯化镁的方法
D.工业采用电解饱和食盐水的方法制备氯气。
难度: 中等查看答案及解析
-
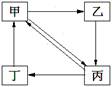
下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
物质
编号
甲
乙
丙
丁
物质转化关系
A
Cu
CuCl2
CuO
Cu(NO3)2
B
Na2CO3
NaOH
NaHCO3
CO2
C
Fe
Fe Cl3
Fe(OH)3
Fe2O3
D
Al2O3
Al(OH)3
NaAlO2
AlCl3
难度: 中等查看答案及解析
-
在下列溶液中,各组离子一定能够大量共存的是
A.含有大量Al3+的溶液: Na+、Cl-、AlO2-、OH-
B.常温下c(H+)/c(OH-)=1012的溶液:Fe2+、Mg2+、NO3-、Cl-
C.能使广泛pH试纸显蓝紫色的溶液:K+、Ba2+、Cl-、Br-
D.能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32-
难度: 中等查看答案及解析
-
据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实。
2CO2(g)+6H2(g)
CH3CH2OH(g)+3H2O(g) 下列叙述错误的是
A.使用Cu-Zn-Fe催化剂可大大提高生产效率
B.反应需在300℃进行可推测该反应是吸热反应
C.充入大量CO2气体可提高H2的转化率
D.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率
难度: 中等查看答案及解析
-
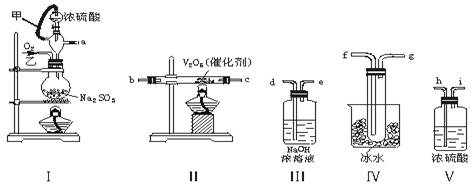
下列实验方案正确且能达到相应实验预期目的的是
A
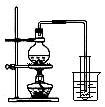 B
B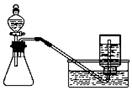
C.
 D.
D.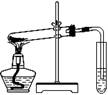

难度: 中等查看答案及解析
-
某稀溶液中含有等物质的量的ZnSO4、Fe2(SO4)3、H2SO4、CuSO4,向其中逐渐加入铁粉。下列各图表示溶液中Fe2+的物质的量和加入铁粉的物质的量之间的关系,其中可能正确的是
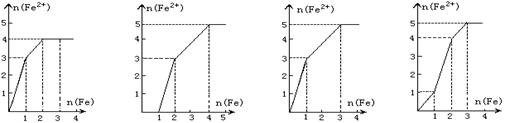
A B C D
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.常温下,4.48 L N2和O2的混合气体所含原子数为0.4NA
B.常温下,1.0L 1.0 mol·L-1NaAlO2溶液中含有的氧原子数为2NA
C.7.8 g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA
D.0.1 mol Fe参加氧化还原反应,转移的电子数目一定是0.2 NA
难度: 中等查看答案及解析
-
某澄清透明溶液中,可能含有Na+、NH4+、Fe2+、Cl¯、CO32¯、SO32¯六种离子中的几种。将该溶液进行如下实验:①加入足量的过氧化钠,有无色无味气体产生,无沉淀生成;②在“①”所得溶液中,加入盐酸至溶液呈酸性,又有气泡产生;③再加入BaCl2溶液,有白色沉淀生成。下列说法正确的是
A.该溶液的pH<7 B.一定存在CO32¯、SO32¯
C.一定不存在NH4+、Fe2+、Cl¯ D.需要通过焰色反应才能确定Na+的存在
难度: 中等查看答案及解析
-
下列现象或反应的原理解释正确的是
现象或反应
原理解释
A
铝箔在酒精灯火焰上加热熔化但不滴落
铝箔表面生成的氧化物具有高熔点
B
钠和氧气在加热条件下进行反应
该反应为吸热反应
C
碳酸钠和氢氧化钠溶液中滴加酚酞,溶液都呈红色
碳酸钠和氢氧化钠都是碱
D
铁制容器可用于盛装冷的浓硫酸
铁与浓硫酸不反应
难度: 中等查看答案及解析
-
将足量CO2通入KOH和Ca(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2体积(V)的关系正确的是
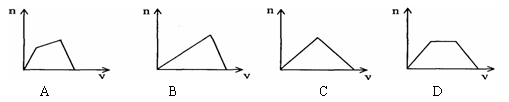
难度: 中等查看答案及解析
-
取a g某物质在氧气中完全燃烧,将其产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了a g。下列物质中不能满足上述结果的是
A.H2 B.CO C.CH3COOH D.C2H5OH
难度: 中等查看答案及解析
-
下列判断正确的是
A.测定硫酸铜晶体中结晶水含量时,灼烧至固体发黑,测定值小于理论值
B.相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量
C.0.1 mol·L-1的碳酸钠溶液的pH大于0.1 mol·L-1的醋酸钠溶液的pH
D.1L 1 mol·L-1的碳酸钠溶液吸收SO2的量大于1L 1 mol·L-1硫化钠溶液吸收SO2的量
难度: 中等查看答案及解析
-
由H2、CH4、CO组成的混合物的混合气体a mL,完全燃烧时消耗相同条件下O2的体积也为a mL,则原混合气中CH4的体积分数为
A.1/3 B.2/3 C.1/2 D.3/5
难度: 中等查看答案及解析
-
1.92gCu投入适量的浓硝酸中,充分反应后,共收集到1.12L标准状态下的气体,如将此气体通过足量水,最后剩余气体的体积是(标准状态下)
A、448mL B、560mL C、224mL D、896mL
难度: 中等查看答案及解析
-
下列离子方程式表达正确的是
A.用稀硝酸洗涤做银镜反应的试管:3Ag +4 H++ NO3¯ →3Ag++ NO↑+ 2H2O
B.用氢氧化钠溶液除去铝表面的氧化膜:Al(OH)3 + OH¯ →AlO2¯+ 2H2O
C.用双氧水和稀硫酸溶解印刷电路铜板:Cu+H2O2+2H+→Cu2++2H2O
D.用食醋除去水瓶中的水垢:CO32¯+ 2CH3COOH →2CH3COO¯+ CO2↑+ H2O
难度: 中等查看答案及解析
-
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2 。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。
下列说法正确的是
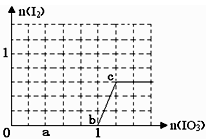
A.反应过程中的氧化产物均为SO3
B.a点时剩余NaHSO3的物质的量为1.2 mol
C.b点时的还原产物可能是KI或NaI
D.当溶液中I¯与I2的物质的量之比为1:1时,加入的KIO3为9/8mol
难度: 中等查看答案及解析
-
由乙酸、乙二酸和甲酸组成的混合物xg,经完全燃烧生成CO2 4.48L(标准状况) ,完全中和同质量的混合物需80mL2mol/LNaOH溶液,则x的数值可能是A. 5.40g B.6.25g C.7.85g D.8.10g
难度: 中等查看答案及解析
-
下列溶液中微粒浓度关系一定正确的是
A.氨水与氯化铵的pH=7的混合溶液中:[Cl-]>[NH4+]
B.pH=2的一元酸和pH=12的一元强碱等体积混合: [OH-]= [H+]
C.0.1 mol·L-1的硫酸铵溶液中:[NH4+]>[SO42-]>[H+]
D.0.1 mol·L-1的硫化钠溶液中:[OH-]=[H+]+[HS-]+2[H2S]
难度: 中等查看答案及解析
-
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:

下列说法正确的是
A.滤液A中的阳离子为Fe2+、Fe3+、H+ B.样品中Fe元素的质量为2.24 g
C.样品中Fe元素的质量为2.49 g D.样品CuO的质量一定为0.80 g
难度: 中等查看答案及解析