-
下列物质中属于纯净物的是:①由同种元素组成的物质;②具有固定熔沸点的物质;③由相同种类和相同数目的原子组成的分子;④只有一种元素的阳离子和另一种元素的阴离子组成的物质;⑤在氧气中燃烧只生成二氧化碳的物质;⑥只含有一种分子的物质
A.②③⑥ B.④⑤⑥ C.①④ D.②⑥
难度: 中等查看答案及解析
-
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.能使甲基橙变黄的溶液中:Na+、K+、SO42-、Al3+
B.pH=2的溶液中:Na+、ClO-、NH4+、SO42-
C.某透明澄清的溶液中:NH4+、Cu2+、NO3-、Cl-
D.0.1 mol·L-1NaHCO3溶液中:K+、Ba2+、OH-、Cl-
难度: 中等查看答案及解析
-
现有CuO和Fe2O3的混合物a g,向其中加入1 mol·L-1的HNO3溶液200 mL恰好完全反
应,若将2a g该混合物用足量CO还原,充分反应后剩余固体质量为
A.(2a-1.6)g B.2(a-1.6)g C.(a-1.6)g D.3.2 g
难度: 中等查看答案及解析
-
(NH4)2SO4在一定条件下发生如下反应:4(NH4)2SO4 =N2↑+6NH3↑+3SO2↑+SO3↑+7H2O
将反应后的混合气体通入BaCl2溶液,产生的沉淀为
A.BaSO4 B.BaSO3 C.BaS D.BaSO4和BaSO3
难度: 中等查看答案及解析
-
有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
A.氧化剂和还原剂的物质的量之比为1∶8
B.该过程说明Fe(NO3)2溶液不宜加酸酸化
C.每1 mol NO3-发生氧化反应,转移8 mol e-
D.若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+
难度: 中等查看答案及解析
-
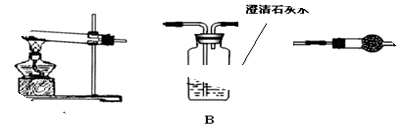
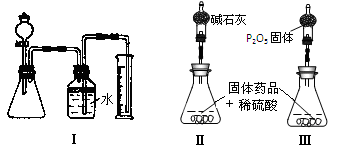
关于下列各装置图的叙述中,正确的是:

‚ ƒ ④
A.装置①中X若为苯,可用于吸收氨气,并防止倒吸
B.装置②将化学能转化为电能
C.图③用于配制一定物质的量浓度的稀硫酸
D. 实验室用装置④收集氨气
难度: 中等查看答案及解析
-
将amol小苏打和bmol过氧化钠置于某体积可变的密闭容器中充分加热,反应后测得容器内的氧气为1mol,下列说法一定正确的是
A.b=2 B.容器中一定没有残余的CO2和水蒸气
C.a:b≥1 D.反应中转移的电子数一定为2NA
难度: 中等查看答案及解析
-
对下列过程中发生反应的叙述正确的是
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.Na+、Mg2+、Al3+得电子能力很弱,故常用电解熔融氧化物的方法来制备其单质
C.从铝土矿中分离出氧化铝的过程中不涉及氧化还原反应
D.从海水中提取溴单质的过程所涉及的反应均为置换反应
难度: 中等查看答案及解析
-
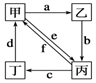
下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
物质
编号
物质转化关系
甲
乙
丙
丁
①
Cu[
CuO
CuCl2[
Cu(NO3)2[
②[
Na2CO3
NaOH
NaHCO3
CO2
③
(NH4)2SO3
CaSO3
SO2
NH4HSO3
④
Al(OH)3
Al2O3
NaAlO2
AlCl3
A.①②③④ B.①②③ C.①③④ D.②④
难度: 中等查看答案及解析
-
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如下图所示)。
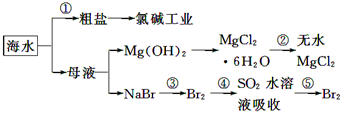
下列有关说法不正确的是
A.从能量转换角度来看,框图中的氯碱工业是一个将电能转化为化学能量的过程
B.过程②中结晶出的MgCl2·6H2O要在HCl氛围中加热脱水制得无水MgCl2
C.在过程③⑤中溴元素均被氧化
D.过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
难度: 中等查看答案及解析
-
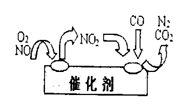
新型纳米材料氧缺位铁酸盐(MFe2Ox 3<x<4,M=Mn、Co、Zn或Ni,在该盐中均显+2价)由铁酸盐(MFe2O4)经高温与氢气反应制得,常温下,它能使工业废气中的酸性氧化物(SO2、NO2等)转化为其单质除去,转化流程如图。关于此转化过程的叙述不正确的是
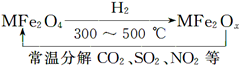
A.MFe2O4在与H2的反应中表现了氧化性
B.MFe2O4与MFe2Ox的相互转化反应均属于氧化还原反应
C.MFe2Ox与SO2反应中MFe2Ox被还原
D.若4 mol MFe2Ox与1 mol SO2恰好完全反应,则MFe2Ox中x的值为3.5
难度: 中等查看答案及解析
-
新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化。某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式如下:

下列说法正确的是
A.维生素C的分子式为C6H8O6
B.维生素C在酸性条件下水解得到3种产物
C.维生素C不溶于水,可溶于有机溶剂
D.上述反应为取代反应
难度: 中等查看答案及解析
-
短周期主族元素X、Y、Z、W的原子序数依次增大,元素X的原子半径最小,Y元素和X元素在一定条件下能形成YX,Z和W的原子序数相差8,W原子的电子总数是其电子层数的5倍。下列叙述正确的是
A.Y可用于制造高性能可充电电池
B.WX3的沸点高于ZX3
C.W的最高价含氧酸的酸性强于Z的最高价含氧酸的酸性
D.原子半径的大小顺序:rZ>rY>rX
难度: 中等查看答案及解析
-
下列离子方程式书写正确的是
A.澄清石灰水与少量小苏打溶液混合:Ca2+ +2OH- +2HCO3- = CaCO3↓+ CO32- + 2H2O
B.氯化铝溶液中加入过量的氨水:Al3+ + 4NH3·H2O = Al(OH)4-+ 4NH4+
C.漂白粉溶液中通入少量SO2气体:Ca2+ +2ClO- +SO42- +H2O =CaSO3↓+2HClO
D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全: Ba2+ + 2OH- + NH4+ + H+ + SO4 2- = BaSO4↓+ NH3·H2O + H2O
难度: 中等查看答案及解析
-
对于反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,下列说法正确的是
A.只有硫酸铜作氧化剂
B.SO42-既不是氧化产物又不是还原产物
C.被氧化的硫与被还原的硫的质量比为3:7
D.1mol硫酸铜可以氧化5/7mol的硫
难度: 中等查看答案及解析
-
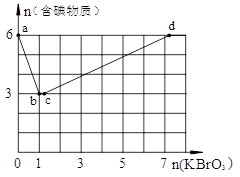
某Na2CO3、NaAlO2的混合溶液中逐滴加入1 mol/L的盐酸,测得溶液中CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是
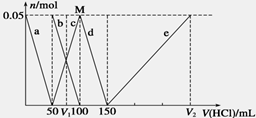
A.原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2
B.V1∶V2=l∶5
C.M点时生成的CO2为0.05 mol
D.a曲线表示的离子方程式为AlO2-+H++H2O==Al(OH)3↓
难度: 中等查看答案及解析
 ①由C、H、O三种元素组成;
①由C、H、O三种元素组成;