-
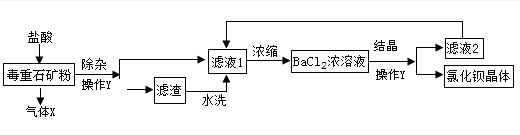
从反应原理和产物纯度两个角度考虑,下列制取Fe2(SO4)3溶液的方案中最佳的是( )
A、过量的Fe粉与稀硫酸反应,过滤
B、过量的Fe2O3与稀硫酸反应,过滤
C、过量的稀硫酸与Fe2O3反应
D、过量的Fe粉与CuSO4溶液反应,过滤
难度: 中等查看答案及解析
-
高铁酸钠(Na2FeO4)是一种新型高效的水处理剂。下列有关高铁酸钠的说法正确的是( )
A.属于氧化物
B.钠、铁、氧三种元素质量比是2∶1∶4
C.铁元素化合价为+6
D.由两种金属和一种非金属组成
难度: 中等查看答案及解析
-
下列除杂试剂使用正确的是 ( )
选项
物质(括号内为杂质)
除杂试剂
A
C(CuO)
盐酸
B
CaCl2溶液(HCl)
Ba(OH)2溶液
C
CO(CO2)
碱石灰(CaO和NaOH混合物)
D
NaOH溶液(Na2CO3)
HCl溶液
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
三种金属锌、铁、铜同时放入一定量的硝酸银溶液中,充分反应后过滤,若滤纸上的金属有a种,滤液中的溶质有b种,则下列说法中正确的( )
A. 滤液中加NaCl溶液产生沉淀,b一定等于4 B. 若a=2,则b等于2或3
C. 滤纸上的金属加硫酸溶液产生气体,a一定等于4 D. 若a=1,则b一定等于3
难度: 困难查看答案及解析
-
下列食品中富含蛋白质的是

A.菠菜 B.米饭 C.鲤鱼 D.豆油
难度: 简单查看答案及解析
-
下列各组转化中,在一定条件下均能一步实现的组合是
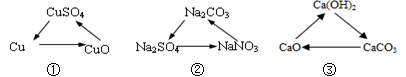
A.①②③ B.①② C.①③ D.②③
难度: 困难查看答案及解析
-
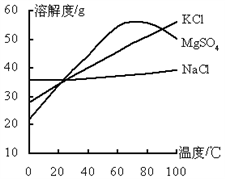
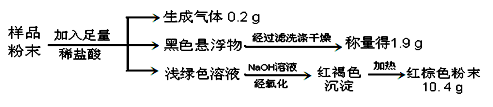
“钾泻盐”的化学式为MgSO4•KCl•xH2O,是一种制取钾肥的重要原料,它溶于水得到KCl与MgSO4的混合溶液。化学活动小组设计了如下种实验方案:以下说法不正确的是
(相对分子量:MgSO4—120 BaSO4—233 AgCl─ 143.5 KCl─74.5)( )
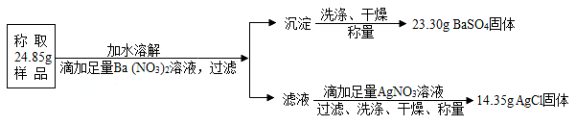
A. 该方案能够计算出“钾泻盐”中KCl的质量分数
B. 足量Ba(NO3)2溶液是为了与MgSO4充分反应
C. “钾泻盐”化学式中x=2
D. 上述实验数据的测定利用学校实验室里的托盘天平即可完成
难度: 困难查看答案及解析
 B. 测定某溶液的pH
B. 测定某溶液的pH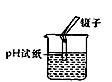
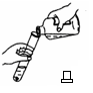 D. 称取氢氧化钠固体
D. 称取氢氧化钠固体