-
在指定环境中,下列各组离子可以大量共存的是( )
A.在中性溶液中:Al3+、K+、S042-、HCO3-
B.在由水电离的c(OH-)=10-14mol•L-1的溶液中:Fe2+、NH4+、NO3-、ClO-
C.在pH=11的溶液中:S032-、K+、Na+、C032-
D.在酸性溶液中:AlO2-、I一、NO3-、Na+难度: 中等查看答案及解析
-
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流.电池总反应为:4A1+3O2+6H2O=4A1(OH)3,下列说法不正确的是( )
A.铂做成网状的目的是为了节省铂的用量
B.正极反应式为:O2+2H2O+4e-=4OH-
C.电池工作时,阴离子向负极移动
D.该电池的一大优点是只需更换铝板就可继续使用难度: 中等查看答案及解析
-
化学与生活是紧密相联的,下列说法正确的是( )
A.为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰
B.海水淡化能解决淡水供应危机,向海水中加净水剂明矾可以使海水淡化
C.用鸡蛋壳膜和蒸馏水除去淀粉胶体中的食盐不涉及化学变化
D.为防止铁制品生锈,可在铁制品的外层涂油漆或局部镀铜难度: 中等查看答案及解析
-
化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
A.CO2的电子式:
B.S2-的结构示意图:
C.羟基的结构式:O-H
D.质量数为37的氯原子:3717Cl难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
A.标准状况下,11.2L乙醇完全燃烧生成CO2分子数为NA
B.pH=13的氢氧化钠溶液中所含Na+数为0.1NA
C.14g乙烯和丙烯的混合气体中所含原子总数为3NA
D.5.6g铁与足量的氯气反应失去电子数为0.2NA难度: 中等查看答案及解析
-
丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如图所示,下列说法不正确的是( )
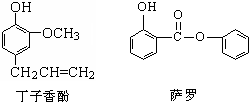
A.萨罗的分子式为C13H10O3
B.丁子香酚与浓溴水只发生取代反应
C.萨罗和丁子香酚均能发生氧化反应
D.丁子香酚和萨罗均能与氯化铁溶液发生显色反应难度: 中等查看答案及解析
-
已知下述三个实验均能发生化学反应
下列判断正确的是( )① ② ③ 将铁钉放入硫酸铜溶液中 向硫酸亚铁溶液中滴入几滴浓硝酸 将铜丝放入氯化铁溶液中
A.实验①中铁钉只做还原剂
B.上述实验证明Fe3+既显氧化性又显还原性
C.实验③中发生的是置换反应
D.上述实验证明氧化性:Fe3+>Cu2+>Fe2+难度: 中等查看答案及解析
-
下列反应的离子方程式正确的是( )
A.Fe3O4与稀硝酸反应:Fe3O4+8H+═Fe2++2Fe3++4H2O
B.向硝酸银溶液中逐滴滴入稀氨水直至过量:Ag++2NH3•H2O═[Ag(NH3)2]++2H2O
C.钠与水的反应2Na+2H2O=2Na++2OH-+H2↑
D.Na2S溶液呈碱性:S2-+2H2OH2S+2OH-
难度: 中等查看答案及解析