-
下列说法正确的是( )
A.在水中加入氯化铁晶体,再加热就可制备氢氧化铁胶体
B.稀释浓硫酸时,将水缓缓倒入盛浓硫酸的烧杯中,并用玻璃棒不断搅拌
C.用酒精萃取碘水中的碘单质的操作,可选用分液漏斗,而后静置分液
D.鉴别氯化铁溶液与氢氧化铁胶体较简便的方法是用激光束照射难度: 中等查看答案及解析
-
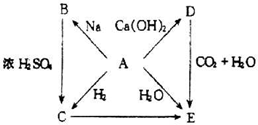
某学生运用所学知识研究钠的性质:将一粒金属钠和一块铜片分别盛在表面皿中,来研究它们在空气中的稳定性.该学生采用的研究方法是( )
①假说法 ②实验法 ③分类法 ④比较法.
A.①②
B.①③
C.②④
D.①③难度: 中等查看答案及解析
-
根据下列反应判断氧化剂的氧化性由强到弱的顺序正确的是( )
①Cl2+2KI═I2+2KCl
②2FeCl3+2HI═I2+2FeCl2+2HCl
③2FeCl2+Cl2═2FeCl3
④I2+SO2+2H2O═2HI+H2SO4.
A.Cl2>I2>Fe3+>SO2
B.Fe3+>Cl2>I2>SO2
C.Cl2>Fe3+>I2>SO2
D.Cl2>Fe3+>SO2>I2难度: 中等查看答案及解析
-
下列变化需要加入氧化剂才能实现的是( )
A.Na2O2→Na2O
B.Fe→FeCl3
C.CuSO4→Cu
D.HClO→Cl2难度: 中等查看答案及解析
-
一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
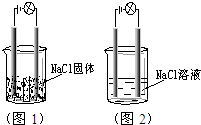
A.NaCl是非电解质
B.NaCl溶液是电解质
C.NaCl溶液中水电离出大量的离子
D.NaCl在水溶液中电离出了可以自由移动的离子难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数,下列说法不正确 的是( )
A.2g氢气所含分子数目为NA
B.在标准状况下,NA个水分子所占有的体积约为22.4 L
C.18g水中含有的电子数为10NA
D.2.4g金属镁变为镁离子时失去的电子数为0.2 NA难度: 中等查看答案及解析
-
把一小粒金属钠放入足量的硫酸铜溶液中,充分反应后在烧杯中的最终产物是( )
A.Cu
B.NaOH
C.CuO
D.Cu(OH)2难度: 中等查看答案及解析
-
实验中需要2mol•L-1的Na2CO3溶液950mL,配制时,你认为应该选用的容量瓶的规格和称取的碳酸钠质量分别是( )
A.1 000mL,212g
B.950mL,201.4g
C.500mL,286g
D.任意规格,572g难度: 中等查看答案及解析
-
能正确表示下列化学反应的离子方程式是( )
A.小苏打溶液中加入少量NaOH溶液:H -+2OH-═H2O
B.铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑
C.硫酸铜溶液与氢氧化钡溶液混合:Cu2++2OH-═Cu(OH)2↓
D.氧化铁与稀硫酸反应:Fe2O3+6H+═Fe2++3H2O难度: 中等查看答案及解析
-
下列各组溶液中的离子能大量共存,且向溶液中加入NaOH溶液时产生白色沉淀,加入盐酸时放出气体的是( )
A.OH-、Ba2+、NO3-、K+
B.Na+、SO42-、Cu2+、Cl-
C.HCO3-、Cl-、Na+、Ba2+
D.Fe2+、Fe3+、Br-、NO3-难度: 中等查看答案及解析
-
下列实验能达到预期目的是( )
A.向某无色液中加BaCl2溶液产生不溶于稀HNO3的白色沉淀,说明原溶液中一定有SO42-
B.向某无色溶液中加入盐酸,有无色无味的气体产生,则说明原溶液中一定有CO32-
C.向某溶液中滴加KSCN溶液,溶液不变红,再滴加氯水,溶液变红,说明原溶液含有Fe2+
D.将淀粉溶液和食盐溶液混合装入半透膜,浸入纯水中,过一段时间,取半透膜内的液体滴入碘水呈蓝色,说明利用渗析可提纯胶体难度: 中等查看答案及解析
-
对于相同物质的量的SO2和SO3,下列说法中正确的是( )
A.硫元素的质量比为5:4
B.分子数之比为1:1
C.原子总数之比为4:3
D.质量之比为1:1难度: 中等查看答案及解析
-
下列反应属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )
A.2Na+2H2O═2NaOH+H2↑
B.3NO2+H2O═HNO3+NO
C.3Fe+4H2O(g)Fe2O4+4H2
D.SO2+H2O═H2SO3难度: 中等查看答案及解析
-
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C
2AlN+3CO下列叙述正确的是( )
A.在氮化铝的合成反应中,N2是还原剂,Al2O3氧化剂
B.上述反应中每生成2mol AlN,N失去6mol电子
C.氮化铝中氮元素的化合价为-3
D.氮化铝是氧化产物难度: 中等查看答案及解析