-
为减少汽车对城市大气的污染,近年来中国成功地开发出了以新燃料作能源的“绿色汽车”。这种汽车可避免有毒的有机铅、苯和苯的同系物以及多环芳香烃的排放,保护环境。这种“绿色汽车”的燃料是( )
A.甲醇 B.汽油 C.柴油 D.重油
难度: 简单查看答案及解析
-
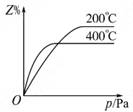
对于反应2SO2(g)+O2(g)2SO3(g),能增大正反应速率的措施是( )
A.通入大量O2 B.增大容器容积 C.移去部分SO2 D.降低体系温度
难度: 简单查看答案及解析
-
可以判定某酸(HA)是强电解质的事实是( )
A.该酸加热至沸腾不分解 B.0.01 mol·L-1该酸的pH=2
C.该酸可以溶解Cu(OH) 2 D.该酸与CaCO3反应放出CO2
难度: 简单查看答案及解析
-
参照反应Br+H2―→HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
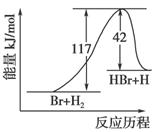
A.正反应为吸热反应
B.正反应为放热反应
C.加入催化剂,该化学反应的反应热增大
D.从图中可看出,该反应的反应热与反应途径有关
难度: 简单查看答案及解析
-
下列溶液一定呈中性的是( )
A.pH=7的溶液
B.c(H+)=c(OH-)的溶液
C.由强酸、强碱等物质的量反应得到的溶液
D.非电解质溶于水得到的溶液
难度: 简单查看答案及解析
-
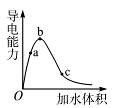
如下图所示曲线a表示放热反应X(g)+Y(g)
Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
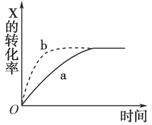
A.升高温度 B.加大X的投入量 C.加催化剂 D.增大体积
难度: 简单查看答案及解析
-
下列说法不正确的是( )
A.物质发生化学反应的反应热仅指反应放出的热量
B.热化学方程式中各物质的化学计量数只表示物质的量,不表示分子的个数
C.所有的燃烧反应都是放热的
D.热化学方程式中,化学式前面的化学计量数可以是分数
难度: 简单查看答案及解析
-
已知下列热化学方程式:
===
H=-483.6
===
H=-241.8
===
H=-571.6
则氢气的燃烧热是( )
A.-483.6
B.-241.8
C.571.6
D.285.8
难度: 简单查看答案及解析
-
可逆反应mA(g)
nB(g)+pC(s) ΔH=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( )


A.m>n,Q>0 B.m>n+p,Q>0 C.m>n,Q<0 D.m<n+p,Q<0
难度: 简单查看答案及解析
-
在298 K、100 kPa时,已知:
===
===2HCl(g)
===
则
与
和
之间的关系正确的是( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
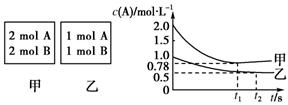
在2 L的密闭容器中,发生反应3A(g)+B(g)
2C(g),若最初加入的A和B都是4 mol,测得10 s内A的平均速率v(A)=0.12
则反应进行到10 s时容器中B的物质的量是( )
A.1.6 mol B.2.8 mol C.3.2 mol D.3.6 mol
难度: 简单查看答案及解析
-
在不同条件下分别测得反应
的化学反应速率,其中表示该反应进行得最快的是( )
A.v
B.v
C.v
.1
D.v
.1
难度: 简单查看答案及解析
-
下列各种试纸,在使用时预先不能用蒸馏水润湿的是( )
A.红色石蕊试纸 B.蓝色石蕊试纸 C.碘化钾淀粉试纸 D.pH试纸
难度: 简单查看答案及解析
-
用蒸馏水逐步稀释0.2 mol/L的稀氨水时,若温度不变,在稀释过程下列数据始终保持增大趋势的是( )
A.c(OH-) B.c(NH4+) C.c(NH3·H2O) D.c(NH4+)/c(NH3·H2O)
难度: 简单查看答案及解析
-
高温下,某反应达平衡,平衡常数K
。恒容时,温度升高
浓度减小。下列说法正确的是( )
A.该反应的焓变为正值 B.恒温恒容下,增大压强
浓度一定减小
C.升高温度,逆反应速率减小 D.该反应化学方程式为
难度: 简单查看答案及解析
-
室温下,若溶液中由水电离产生的c(OH-)=1×10-14mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
A.Al3+、Na+、NO3-、Cl- B.K+、Na+、Cl-、NO3-
C.K+、Na+、Cl-、AlO2- D.K+、NH4+、SO42-、NO3-
难度: 简单查看答案及解析
-
物质的量浓度相同的下列溶液,pH由大到小排列正确的是( )
A.Ba(OH)2、Na2SO3、FeCl3、KCl B.Na2SiO3、Na2CO3、KNO3、NH4Cl
C.NH3·H2O、H3PO4、Na2SO4、H2SO4 D.NaHCO3、C6H5COOH、C2H5OH、HCl
难度: 简单查看答案及解析
-
将氨水缓缓地滴入盐酸中至中性,下列有关的说法:①盐酸过量 ②氨水过量 ③恰好完全反应 ④c(NH4+)=c(Cl-) ⑤c(NH4+)<c(Cl-)正确的是( )
A.①⑤ B.③④ C.②⑤ D.②④
难度: 简单查看答案及解析