-
用于制造隐形飞机的某种物质结构为:
,则该物质属于
A.烯烃 B.无机物 C.有机物
D.烷烃
难度: 中等查看答案及解析
-
以下现象与电化腐蚀无关的是
A.黄铜(铜锌合金)制作的铜锣不易产生铜绿 B.生铁比软铁芯(几乎是纯铁)容易生锈
C.铁器件上附有铜配件,在接触处易生铁锈 D.银制奖牌久置后表面变暗
难度: 中等查看答案及解析
-
NA表示阿伏加德罗常数的值,下列说法正确的是
A.1mol苯乙烯(
)中含有的C=C数为4NA
B.标准状况下,2.24L己烷含有的分子数为0.1NA
C.1mol甲基含10NA个电子
D.某温度下,2.6g乙炔和苯的混合气体中所含碳原子数为0.2NA
难度: 困难查看答案及解析
-
为验证烷烃分子中含有碳、氢两种元素,可将其燃烧产物通过:①浓硫酸;②澄清石灰水;③无水硫酸铜。正确的顺序是
A.①②③ B.②③ C.②③① D.③②
难度: 中等查看答案及解析
-
有①、②、③三瓶体积相等,浓度都是1mol·L-1的盐酸溶液,将①加热蒸发至体积一半;向②中加入少量的CH3COONa固体(加入后仍显酸性);③不作任何改变。若以酚酞作指示剂,用NaOH溶液滴定上述三种溶液,所耗NaOH溶液的体积为
A. ①=②>③ B. ③>②>① C. ③=②>① D. ①=②=③
难度: 中等查看答案及解析
-
下列化学
反应属于取代反应的是
A.乙炔与酸性高锰酸钾溶液的反应
B.乙烯通入溴的四氯化碳溶液中的反应
C.在镍作催化剂、加热的条件下苯与氢气的反应
D.在浓硫酸作用下,苯在55℃左右与浓
硝酸的反应
难度: 中等查看答案及解析
-
某同学为了使反应2HCl+2Ag = 2AgCl↓+H2↑能进行,设计了下列四个实验,如下图所示,你认为可行的方案是
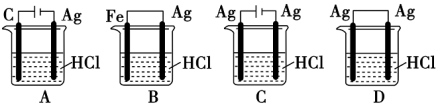
难度: 中等查看答案及解析
-
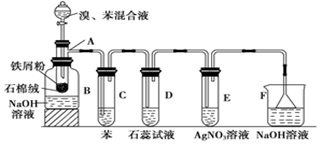
下列实验能获得成功的是
A.用溴水可鉴别苯、CCl4、己烯
B.加浓溴水,然后过滤可除去苯中少量己烯
C.苯、溴水、铁粉混合制成溴苯
D.可用分液漏斗分离己烷和苯的混合物
难度: 中等查看答案及解析
-
常温下,下列各组数据中比值为2:1的是
A.熔融NaHSO4电离出的阳离子与阴离子之比
B.0.2mol·L-1的CH3COOH溶液与0.1mol·L-1的盐酸中c(H+)之比
C.pH=7的氨水与(NH4)2SO4的混合溶液中,c(NH
)与c(SO
)之比
D.pH=12的Ba(OH)2溶液与pH=12的KOH溶液中c(OH-)之比
难度: 中等查看答案及解析
-
对于有机物
,下列说法正确的是
A.该物质的分子式为C10H12
B.该物质能与4 mol Br2完全加成
C.该物质能发生加聚反应
D.该物质苯环上的一氯代物有3种
难度: 中等查看答案及解析
-
在盛有饱和Na2CO3溶液的烧杯中,插入两个Pt电极,保持温度不变,通电一段时间后,下列判断正确的是
A.溶液的pH将增大 B.Na+数和CO32-数的比值将变小
C.溶液浓度不变,有晶体析出 D.溶液浓度逐渐增大并有晶体析出
难度: 中等查看答案及解析
-
某烯烃与氢气加成后得到饱和烃
,则该烯烃可能结构的种数
A.1种 B.2种 C.3种 D.4种
难度: 中等查看答案及解析
-
研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间的含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl 。下列有关“水”电池在海水中放电时的说法正确的是
A.正极反应:Ag+Cl--e-=AgCl
B.每生成1molNa2Mn5O10转移2mol电子
C.Na+不断向“水”电池的负极移动
D.AgCl是还原产物
难度: 中等查看答案及解析
-
在C3H9N中,N原子以三个单键与其他原子相连接,它具有的同分异构体数目
为
A. 1 B. 2 C. 3 D. 4
难度: 中等查看答案及解析
-
某有机物的结构简式如图,下列结论正确的是

A.该有机物分子式为C13H16
B.该有机物属于苯的同系物
C.该有机物分子中至少有4个碳原子共直线
D.该有机物分子中最多有13个碳原子共平面
难度: 中等查看答案及解析
-
下列叙述正确的是
A. 组成元素相同,各元素质量分数也相同的不同物质属于同系物
B. 分子式相同的不同物质一定是同分异构体
C. 相对分子质量相同的不同物质一定是同分异构体
D. 通式相同的不同物质一定属于同系物
难度: 中等查看答案及解析
-
有一种烃,其结构简式可以表示为:
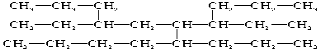 ,命名该有机物时,应认定它的主链上的碳原子数目是
,命名该有机物时,应认定它的主链上的碳原子数目是A.8 B.9 C.11 D.12
难度: 中等查看答案及解析
-
wg含有双键的不饱和烃X与VL的氢气(标准状况)恰好反应,若X的相对分子质量为
,阿伏加德罗常数为
,则1 mol X中含有双键数目为
A.
B.
C.
D.
难度: 中等查看答案及解析
-
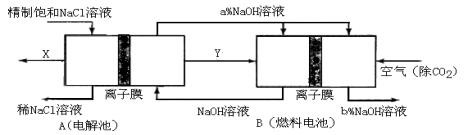
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是
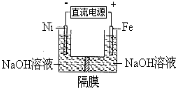
A.铁是阳极,电极反应为Fe-6e-+4H2O=FeO42-+ 8H+
B.若隔膜为阴离子交换膜,则OH-自右向左移动
C.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极
D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
难度: 困难查看答案及解析
-
将1molCH4与氯气发生取代反应,待反应完全后,测定四种有机物的物质的量相等,则产生HCl的物质的量是
A.0.5mol B.2 mol C. 2.5 mol D.4mol
难度: 中等查看答案及解析
-
标准状况下11.2 L某烃A在一定的条件下,可与1 g H2起加成反应生成通式为CnH2n的直链烃,将加成产物燃烧可得二氧化碳88g。下列可能为烃A名称的是
A.2—甲基丙烷 B.1,3—丁二烯 C.2—甲基丙炔 D.2—甲基丙烯
难度: 困难查看答案及解析
-
将 AgNO3 、Ba(NO3)2 、Na2SO4 、NaCl 四种电解质按物质的量之比1∶1∶1∶2加入足量蒸馏水中,然后用铂电极电解该混合物至不再有溶质离子参与反应时,则所得氧化产物与还原产物的质量比为
A.71∶2 B.35.5∶108 C.108∶35.5 D.71∶109
难度: 中等查看答案及解析
-
用惰性电极电解 2L 1 mol·L-1的硫酸铜溶液,在电路中通过 0.5mol 电子后,将电源反接,电路中又通过 1mol 电子,此时溶液中c(H+)是(设溶液体积不变)
A.0.25 mol·L-1 B.0.5 mol·L-1 C.0.75 mol·L-1 D.1.5 mol·L-1
难度: 困难查看答案及解析
-
在25℃和101kPa时,甲烷、乙炔和乙烯组成的混合烃10mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小17.5mL,则原混合烃中乙炔的体积分数为
A.12.5
% B.25% C.50% D.75%
难度: 困难查看答案及解析