-
将少量灰黑色的生铁粉末,投入盛有过量稀硫酸的烧杯中,充分搅拌,待完全反应后过滤,滤纸上留有黑色的残渣.该黑色残渣的主要成分是( )
A.铁
B.碳
C.铁、碳混合物
D.硫酸亚铁难度: 中等查看答案及解析
-
下列有关金属的说法错误的是( )
A.金属具有金属光泽,常温下金属都是固体
B.生铁和钢是含碳量不同的铁合金,其中生铁的含碳量大于钢的含碳量
C.炒完菜后,应及时除掉锅底的水,这样可以防止铁锅生锈
D.金属的回收利用是保护金属资源的有效途径之一难度: 中等查看答案及解析
-
钨是熔点最高的金属,广泛应用于拉制灯丝,有“光明使者”的美誉.我省蕴藏着丰富的钨矿资源冶炼金属钨常用到白钨矿石,其主要成分是钨酸钙(CaWO4),钨酸钙中钨(W)的化合价为( )
A.-6
B.+4
C.+6
D.+7难度: 中等查看答案及解析
-
地沟油长期食用可能会引发癌症,下列辨别某瓶装油是否为“地沟油”的简易方法,一定涉及化学变化的是( )
A.看油是否透明
B.闻油是否有异味
C.问油的生产厂家
D.取油燃烧,听是否发出噼啪响声难度: 中等查看答案及解析
-
液化石油气作为燃料,已普遍进入城市家庭,它是含有下列物质的混合物,在常压下,这些物质的沸点如下表所示:
在常温下使用至无气体放出时,钢瓶中常剩余一些液态物质,这些物质最有可能是( )物质名称 乙烷 丙烷 丁烷 戊烷 己烷 沸点/℃ -88.6 -42.2 -0.5 36.1 69.2
A.乙烷、丙烷和丁烷
B.乙烷和丙烷
C.只有乙烷
D.戊烷和己烷难度: 中等查看答案及解析
-
一个密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得数据见下表.下列说法中正确的是( )
物质 甲 乙 丙 丁 反应前质量 10g 37g 5g 8g 反应后质量 4g X 5g 42g
A.X=9g
B.在该反应中,丙物质一定做催化剂
C.该反应是化合反应
D.在该反应的化学方程式中,丙、丁的化学计量数之比为1:l难度: 中等查看答案及解析
-
农业科技人员向农民建议:利用温室进行植物生产时,可向温室内通入适量的二氧化碳,这是因为( )
A.二氧化碳可使害虫窒息死亡从而防治病虫害
B.二氧化碳可产生温室效应从而提高室温
C.施用后可促进植物的光合作用
D.施用后可防止火灾难度: 中等查看答案及解析
-
下列物质中,属于纯净物的是( )
A.双氧水溶液
B.空气
C.水
D.石灰石难度: 中等查看答案及解析
-
人体中缺少某些元素,会影响健康,甚至引起疾病.下列说法正确的是( )
A.缺铁易患贫血病
B.缺碘易患夜盲症
C.缺锌易患甲状腺疾病
D.缺钙易患动脉硬化疾病难度: 中等查看答案及解析
-
上海世博会上最受欢迎的中国馆,处处蕴含着“低碳”理念.下列做法不符合 该理念的是( )
A.提倡步行
B.一水多用
C.少用空调
D.焚烧垃圾难度: 中等查看答案及解析
-
利尿酸(C13H12Cl2O3)有很强的利尿作用,能快速降低体重并稀释尿液,可以掩盖服用的兴奋剂而逃避检查,因此利尿酸在奥运会上被禁用.下列叙述正确的是( )
A.利尿酸属于氧化物
B.利尿酸由碳、氢、氧、氯四种元素组成
C.利尿酸由30个原子构成
D.利尿酸中各元素的质量比为13:12:2:3难度: 中等查看答案及解析
-
中国科学技术大学钱逸泰教授等以CCl4和金属钠为原料,在700℃制造出纳米级金刚石粉末和另一种化合物.该成果发表在世界最权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”.同学们对此的一些“理解”,不正确的是( )
A.CCl4是一种化合物
B.制造金刚石过程中发生了化学变化
C.金刚石属于金属单质
D.这个反应是置换反应难度: 中等查看答案及解析
-
近来有研究报告称:除去“普通水”里含有的氮气和氧气后,水的去污能力将大大增强.下列对此说法的理解不正确的是( )
A.“普通水”中含有氮分子
B.氮气和氧气在水中有一定的溶解性
C.“普通水”中含有氧分子
D.除去氧气后的水就不再含有氧元素了难度: 中等查看答案及解析
-
加油站必须粘贴的标志是( )
A.
节水标志
B.
严禁烟火
C.
节能标志
D.
绿色食品难度: 中等查看答案及解析
-
黑火药是我国四大发明之一,距今已有一千多年的历史,黑火药爆炸的原理可用下式表示:
2KNO3+3C+SK2S+N2↑+3X↑,根据质量受恒定律可推出X的化学式为( )
A.CO2
B.CO
C.NO
D.SO2难度: 中等查看答案及解析
-
已知在反应A+2B→C+2D中,参加反应的A和B的质量比为1:5.当2g A和足量B完全反应后,生成4g的D,则反应生成的C为( )
A.2g
B.4g
C.6g
D.8g难度: 中等查看答案及解析
-
小明测得某食盐溶液中含有氯元素的质量分数为2.19%,如果以NaCl计算,则该盐水中所含NaCl的质量分数为( )
A.0.71%
B.1.42%
C.2.18%
D.3.61%难度: 中等查看答案及解析
-
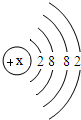
2012年3月有媒体报道,称谢娜代言的化妆品露兰姬娜因汞超标在美被禁.如图为元素周期表中的一格,下列有关说法不正确的是( )
A.该元素的原子序数为80
B.该元素的相对原子质量为200.6
C.该元素为非金属元素
D.该元素的原子核外有80个电子难度: 中等查看答案及解析
-
用X表示某化合物的化学式,X燃烧时发生如下反应:X+3O2
3CO2+3H2O.由此,下列说法正确的是( )
A.X由碳、氢、氧三种元素组成
B.X的相对分子质量为56
C.X中碳的质量分数为75%
D.反应中,X与O2的质量比为30:32难度: 中等查看答案及解析
-
经测定,某含有C、O两种元素的混合气体中,C元素的质量分数为22%,则该混合物中( )
A.一定有CO2
B.一定有CO2、CO
C.一定有O2
D.一定有CO2、CO、O2难度: 中等查看答案及解析