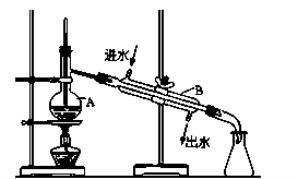
-
容量瓶是用来配制物质的量浓度的溶液的定量仪器,其上标有:①温度、② 浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的
A.②④⑥ B. ①③⑤ C.①②④ D.③⑤⑥
难度: 简单查看答案及解析
-
下列溶液中Cl-的物质的量浓度最大的是
A.300 mL 3.5 mol/L KCl溶液 B.1000 mL 2.5 mol/L NaCl溶液
C.200 mL 2 mol/L MgCl2溶液 D.250 mL1 mol/L AlCl3溶液
难度: 中等查看答案及解析
-
下列各组物质中,按单质、化合物、混合物顺序排列的是
A.金属钙、生石灰、碱石灰 B.铁、四氧化三铁、冰水混合物
C.水银、空气、干冰 D.二氧化硫、水蒸气、天然气
难度: 简单查看答案及解析
-
以下是一些常用的危险品标志,装运酒精的包装箱应贴的图标是

难度: 简单查看答案及解析
-
胶体区别于其他分散系的本质特征是:
A.胶体分散质粒子直径在1nm~100nm之间
B.胶体能产生丁达尔效应
C.胶体的分散质能通过滤纸空隙,而浊液的分散质不能
D.胶体在一定条件下能稳定存在
难度: 中等查看答案及解析
-
下列电离方程式正确的是
A、Ba(OH)2 = Ba2+ + 2OH- B、AlCl3= Al3+ + Cl3-
C、H2SO4 = 2H+ + S6+ + 4O2- D、Na2CO3 = Na2+ + CO32-
难度: 中等查看答案及解析
-
下列各项中,括号里的物质是除杂质所选用的药品,其中错误的是
A. KNO3溶液中混有KCl(AgNO3溶液)
B. CO中混有CO2(石灰水)
C. H2中混有HCl(NaOH溶液)
D. NaOH中混有Na2CO3(盐酸)
难度: 中等查看答案及解析
-
判断给定化学反应是否为氧化还原反应的依据是
A.看反应前后是否有氧原子的得失
B.看反应前后是否有原子的重新组合
C.看反应前后是否有元素的化合价发生改变
D.看反应后是否有气体生成
难度: 简单查看答案及解析
-
下列反应的离子方程式书写正确的是
A.稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑
B.硫酸铜溶液中加入铁粉反应:Cu2++Fe=Fe2++Cu
C.氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-=BaSO4↓
D.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑
难度: 中等查看答案及解析
-
根据下列反应判断有关的物质氧化性由强到弱的顺序是
H2SO3+I2+H2O=2HI+H2SO4
2FeCl3+2HI=2FeCl2+2HCl+I2
3FeCl2+4HNO3=2FeCl3+NO↑+2H2O+Fe(NO3)3.
A. H2SO3>I﹣>Fe2+>NO B. HNO3>Fe3+>I2>H2SO4
C. HNO3>Fe3+>H2SO3>I2 D. NO->Fe2+>H2SO3>I﹣
难度: 困难查看答案及解析
-
鉴别氯化铁溶液与氢氧化铁胶体最简便的方法是
A.萃取 B.蒸馏 C.过滤 D.用激光笔照射
难度: 简单查看答案及解析
-
用NA表示阿伏德罗常数,下列叙述正确的是
A.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
B.标准状况下,22.4LH2O含有的分子数为 NA
C.通常状况下,NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl﹣ 个数为 NA
难度: 中等查看答案及解析
-
为了除去粗盐中的Ca2+, Mg2+,SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序
①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液
A.④②⑤ B.②⑤④①③ C.④①②⑤③ D.①④②⑤③
难度: 困难查看答案及解析
-
在碱性溶液中能大量共存且溶液为无色透明的离子组是
A.K+ 、MnO4-、Na+、Cl-
B.Fe3+、Na+、Cl-、SO42-
C.Na+、H+、NO3-、SO42-
D.K+、Na+、NO3-、CO32-
难度: 中等查看答案及解析
-
在空气中,有下列反应发生:①N2+O2═2NO;②2NO+O2═2NO2; ③3NO2+H2O═2HNO3+NO;④2SO2+O2═2SO3;⑤SO3+H2O═H2SO4;⑥SO2+H2O═H2SO3;⑦3O2═2O3.其中属于氧化还原反应的是
A. ①②③④ B. ①②③④⑦
C. ①②④⑦ D. ①②③④⑤⑥⑦
难度: 中等查看答案及解析
-
一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3=2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为
A.1∶1 B.5∶4 C.5∶3 D.3∶5
难度: 中等查看答案及解析