-
下列有关化学基本概念的判断依据,正确的是( )
A.溶液与胶体:本质区别是否均一、透明
B.纯净物与混合物:是否仅含有一种物质
C.氧化还原反应与非氧化还原反应:是否有单质参加
D.强电解质与弱电解质:化合物溶液导电能力是否强
难度: 中等查看答案及解析
-
点燃的镁条伸入盛有下列气体的集气瓶中,能继续燃烧的是( )
①Cl2 ②O2 ③CO2 ④水蒸气
A.① B.①② C.①②③ D.①②④
难度: 中等查看答案及解析
-
镁铝合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要用于制作窗框、卷帘门、防护栏等。下列与这些用途无关的性质是( )
A.导电性好 B.密度小 C.不易生锈 D.强度高
难度: 简单查看答案及解析
-
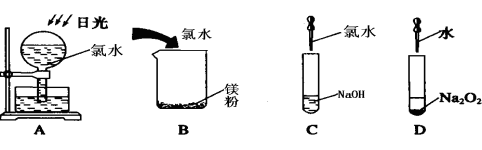
下列试剂的保存不正确的是 ( )
A.漂白粉必须密封保存 B.新制氯水用无色的广口瓶保存
C.少量金属钠保存在煤油中 D.液溴用一层水封盖再密封保存
难度: 中等查看答案及解析
-
新制氯水与久置的氯水相比较,下列结论正确的是 ( )
A.颜色相同 B.都能使有色布条褪色
C.滴加石蕊试剂都只变红 D.加AgNO3溶液都能生成白色沉淀
难度: 中等查看答案及解析
-
下列实验操作中,完全正确的是 ( )
①将试管平放,用纸槽往试管里送入固体粉末,然后竖立试管;②用坩埚钳夹取加热后的蒸发皿;③蒸馏石油时,温度计水银球插入液面以下;④往试管中倾倒液体时,试剂瓶标签向手心;⑤分液漏斗分离四氯化碳和水的混合液时,四氯化碳和水层依次从漏斗下口放出,用不同的容器承接;
A、①②④ B、①④⑤ C、②③⑤ D、①②③④
难度: 中等查看答案及解析
-
用漂白粉溶液浸泡过的有色布条,如果晾置在空气中,过了一段时间,其漂白效果会更好的原因可能是 ( )
A.漂白粉被氧化了
B.漂白粉跟空气中的 CO2反应充分,生成了较多量的 HClO
C.有色布条被空气中的氧气氧化了
D.漂白粉溶液蒸发掉部分水,其浓度增大
难度: 中等查看答案及解析
-
某微粒用符号ZAMn+表示,下列关于该微粒的叙述正确的是 ( )
A.所含质子数为(A-n) B.所含中子数为(A-Z + n)
C.所含电子数为(Z-n) D.中子数-电子数=A-2Z-n
难度: 中等查看答案及解析
-
硫酸镁和硫酸铝溶液等体积混合后,铝离子浓度为0.2mol·L-1,硫酸根离子的浓度为0.4mol·L-1,则混合液中镁离子的浓度为 ( )
A、0.1mol·L-1 B、0.15mol·L-1 C、0.2mol·L-1 D、0.3mol·L-1
难度: 中等查看答案及解析
-
纯碱和小苏打是厨房中两种常见的用品,它们都是白色固体,下列区分这两种物质的方法正确的是 ( )
A.用两只小玻璃杯,分别加入少量的两种样品,再加入等量的食醋,产生气泡快的是小苏打
B.用洁净铁丝蘸取两种样品在煤气火焰上灼烧,火焰颜色发生明显变化的是小苏打
C.分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打
D.将两种样品配成溶液,分别加入石灰水,无白色沉淀生成的是小苏打
难度: 中等查看答案及解析
-
下列说法中错误的是( )
A.从2 L 1 mol·L-1的NaCl溶液中取出10 mL,其浓度仍是1 mol·L-1
B.制成0.5 L 1 mol·L-1的盐酸,需标准状况下氯化氢气体11.2 L
C.1 L 1 mol·L-1 BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023
D.10g 98%硫酸(密度为1.84g·cm-3)与10mL 18.4 mol·L-1硫酸的浓度是不同的
难度: 中等查看答案及解析
-
钠与水反应时,观察到的现象是( )
①钠浮在水面上 ②钠先沉入水中 ③钠熔成光亮的小球 ④四处游动
⑤发出“嘶嘶”的响声,甚至发生轻微的爆炸 ⑥滴入酚酞溶液变红
A.全部 B.①③④⑤⑥ C. ②③⑥ D.②③④⑤⑥
难度: 中等查看答案及解析
-
如下图所示装置可以用来发生、洗涤、干燥、收集(不 考虑尾气处理)气体。该装置可用于( )
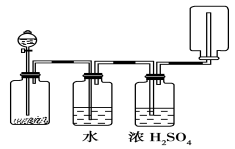
A.KMnO4分解生成氧气
B.二氧化锰和浓盐酸生成氯气
C.碳酸钙和盐酸生成二氧化碳
D.锌和盐酸生成氢气
难度: 中等查看答案及解析
-
常温下,相同物质的量浓度的下列溶液,导电能力最强的是 ( )
A.盐酸 B.氨水 C.醋酸 D.碳酸钠
难度: 简单查看答案及解析
-
下列各组离子能大量共存于同一溶液中,且加入适量NaOH溶液或少量稀硫酸时,都能产生白色沉淀的是( )
A.Ba2+、Mg2+、NO
、Cl- B.Mg2+、Na+、CO
、SO
C.Cu2+、Ba2+、NO
、Cl- D.Fe3+、Ba2+、NO
、SO
难度: 中等查看答案及解析
-
下列的电离方程式,正确的是( )
A.H2CO3
2H+ + CO32-
B.HClO
H+ + ClO-
C.Na2CO3 = Na+ + CO32-
D.KOH = K+ + O2- + H+
难度: 简单查看答案及解析
-
菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有五价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的三价砷。下列说法不正确的是 ( )
A.“两者同食”发生的反应中维生素C作还原剂
B.五价砷在维生素C作用下发生了还原反应
C.河虾中含有的五价砷,没有毒性
D.可以推测砒霜中所含的砷元素化合价为+5
难度: 中等查看答案及解析
-
下列物质属于纯净物的是( )
A.氯水 B.漂白粉 C.液氯 D.食盐水
难度: 简单查看答案及解析
-
下列化学反应中,离子方程式表示正确的是( )
A.少量金属钠加到冷水中:Na+2H2O = Na++OH-+H2↑
B.铁粉加到盐酸中:2Fe+6H+ = 2Fe 3++3H2↑
C.石灰石溶解在稀HCl中:CO32-+ 2H+ = CO2↑+ H2O
D.硫酸溶液与氢氧化钡溶液混合:Ba2+ +2OH- + SO
+2H+ =2H2O+ Ba SO4↓
难度: 中等查看答案及解析
-
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:KClO3+H2C2O4+H2SO4
ClO2↑+K2SO4+CO2↑+H2O(未配平)下列说法正确的是( )
A.KClO3在反应中失去电子 B.ClO2是还原产物
C.H2C2O4在反应中被还原 D.1 mol KClO3参加反应有2 mol电子转移
难度: 中等查看答案及解析