-
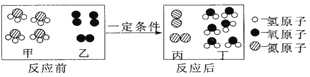
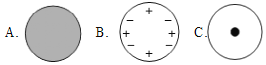
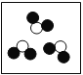
下列是表示物质分子的示意图,图中“
”和“
”分别表示两种有不同质子数的原子,则图中表示化合物的是( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列符号既能表示某种元素,又能表示该元素的一个原子,还能表示一种物质的是( )
A.
B.
C. O D. Hg
难度: 简单查看答案及解析
-
日常生活常接触到“含氟牙膏”、“高钙牛奶、碘盐”、“富硒茶叶”、“加铁酱油”等用品,这里的氟、钙、碘、硒、铁指的是( )
A. 单质 B. 原子 C. 离子 D. 元素
难度: 简单查看答案及解析
-
下列装置中,哪一项是在氧气制取实验中一定不需要用到的( )
A. 试管 B. 酒精灯 C. 玻璃棒 D. 水槽
难度: 简单查看答案及解析
-
中科院的全超导的“人造太阳”——托克马克核聚变试验装置的调试运行成功,使我国在该领域的研究处于世界前列。氘和氚是核聚变的原料(氘、氚原子核内都只有1个质子,但含不同数目的中子),聚变发生后,氘、氚原子核转变为氦原子核。根据以上叙述,下列说法正确的是( )
A.核聚变是化学变化
B.氘原子和氚原子属于不同元素
C.氘原子和氚原子是氢的两种同位素
D.氘原子和氚原子的相对原子质量相同
难度: 中等查看答案及解析
-
下列有关元素的说法正确的是( )
①地壳中最多的金属元素是铝,也就是金属铝
②对人体而言,锌是有害元素
③地壳中非金属元素的总含量大于金属元素,但种类少于金属元素
④人体中H、O元素含量很高,这跟水占人体质量的
以上有关
A.
B.
C.
D.
难度: 简单查看答案及解析
-
下列五种物质中均含有氯元素,它们按氯元素的化合价的顺序排列:①KCl②Cl2③HClO④X⑤NaClO4,则根据这种排列规律,X不可能是( )
A. AgCl B.
C.
D.
难度: 简单查看答案及解析
-
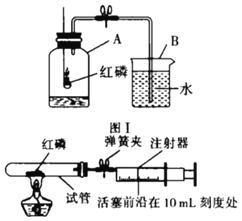
如图,某同学用燃烧红磷的方法测定空气中氧气的体积分数,实验后发现,测得的氧气体积分数小于
,对此,你认为下列做法或想法不可取的是( )
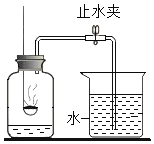
A. 检查实验装置是否漏气
B. 可能红磷的量不足,没有除尽氧气
C. 没有冷却至室温就打开止水夹,进入瓶内的水减少
D. 将红磷改成足量的木炭,重新实验
难度: 简单查看答案及解析
-
小明在家里用冷开水养鱼,结果鱼全死了,原因是冷开水中几乎不含( )
A. 氧分子 B. 氧原子 C. 氧元素 D. 营养元素
难度: 简单查看答案及解析
-
氮肥是含有氮元素的物质,经测定某种硝酸铵(NH4NO3)化肥中氮元素的质量分数是38%,则该硝酸铵化肥中可能含有( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
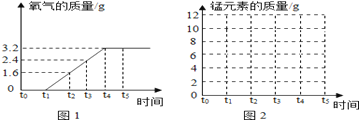
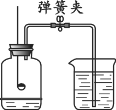
如图所示,利用过量红磷进行空气中氧气含量的测定,下列图像能正确反映对应变化关系的是
A.
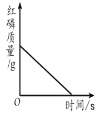 B.
B.  C.
C.  D.
D. 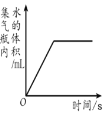
难度: 困难查看答案及解析