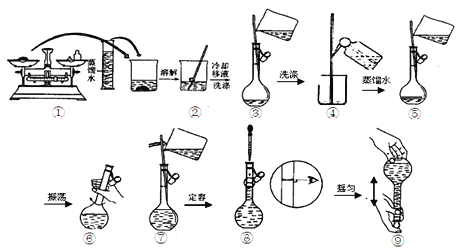
-
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤过滤 正确的操作顺序
A. ①②③⑤④ B. ③②①⑤④ C. ②③①④⑤ D. ③⑤②①④
难度: 中等查看答案及解析
-
下列叙述错误的是( )
①摩尔是国际单位制中七个基本物理量之一; ②1 mol任何物质都含有约6.02×1023个原子;③6.02×1023就是阿伏加德罗常数;④氢原子的摩尔质量是1 g;⑤HCl的摩尔质量等于1 mol HCl分子的质量;⑥1 mol CO2中含有1 mol碳和2 mol氧。
A. ①②③ B. ②③④ C. ②③④⑥ D. 全部
难度: 简单查看答案及解析
-
下列溶液中C(Cl-)最大的是( )
A. 65mL 1mol/L的KCl溶液 B. 25mL 3mol/L的NaCl溶液
C. 20mL 2mol/L的MgCl2溶液 D. 10mL 4.5mol/L的NaClO3溶液
难度: 简单查看答案及解析
-
需要分离下列两种混合物,选用最合适的实验装置是
a.四氯化碳中不小心混入了大量的水;
b.水与丙酮的混合物,已知丙酮是可与水混溶的液体,密度小于水,沸点为56℃。
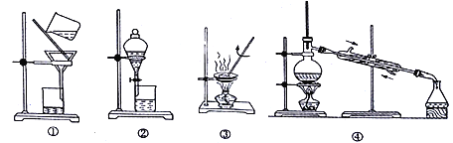
A. ②④ B. ④③ C. ②① D. ④③
难度: 中等查看答案及解析
-
下列物质的分类组合正确的是
A
B
C
D
纯净物
空气
NaOH
稀盐酸
FeSO4·7H2O
非电解质
H2O
Na2O
CO
NH3
电解质
HNO3
Cu
蔗糖
CH3COOH
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列检验方法和结论正确的是
A. 加入硝酸银溶液有白色沉淀生成,证明原溶液中一定有Cl-
B. 加入氯化钡溶液产生白色沉淀,再加稀盐酸沉淀不溶解,证明原溶液中一定有SO42—
C. 加入盐酸后放出能使澄清石灰水变浑浊的气体,证明原溶液中一定含有CO32—
D. 加入紫色石蕊试液,溶液显红色,证明溶液一定呈酸性
难度: 中等查看答案及解析
-
下列电离方程式中,正确的是
A. Na2SO4 = 2Na++SO4﹣2 B. NaHCO3 = Na++H++CO32﹣
C. Al2(SO4)3 = 2Al3++3SO42﹣ D. Ca(NO3)2=Ca2++2(NO3)2﹣
难度: 中等查看答案及解析
-
下列各组离子能在呈酸性的无色溶液中大量共存的是( )
A. Ba2+、Na+、NO3-、MnO4- B. Mg2+、Cl-、Al3+、SO42-
C. K+、OH-、HCO3-、NO3- D. Ca2+、Na+、Fe3+、SO32-
难度: 中等查看答案及解析
-
下列离子方程式书写正确的是
A. 铁和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑
B. 硫酸滴入氢氧化钡中:Ba2++2OH﹣+2H++SO42-=BaSO4↓+2H2O
C. 铜片置于硝酸银溶液中:Cu+Ag+═Cu2++Ag
D. 实验室用大理石与盐酸反应制取二氧化碳:CO32﹣+2H+═CO2↑+H2O
难度: 中等查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法中正确的是
A. 标准状况下,22.4 L H2O 的分子数为 NA
B. 1 mol NH4+ 所含质子数为10NA
C. 物质的量浓度为0.5mol·L-1 的 MgCl2 溶液,含有的 Cl-数为 NA
D. 常温常压下,32g O2和O3的混合气体所含原子数为2NA
难度: 中等查看答案及解析