-
欲配制100ml 1.0 mol/L Na2SO4溶液,正确的方法是( )
①将14.2 g Na2SO4 溶于100ml水中
②将32.2g Na2SO4·10H2O溶于少量水中,再用水稀释至100 ml
③将20 ml 5.0 mol/L Na2SO4溶液用水稀释至100 ml
A. ①② B. ②③ C. ①③ D. ①②③
难度: 简单查看答案及解析
-
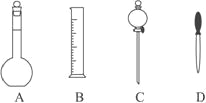
下列实验操作中错误的是( )
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B. 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C. 蒸发结晶时应将溶液蒸干
D. 称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中
难度: 中等查看答案及解析
-
有一份气体样品的质量是14.2 g,体积是4.48 L(标准状况下),该气体的摩尔质量( )。
A. 28.4 B. 28.4 g/mol C. 71 D. 71 g/mol
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A. 标准状况下任何气体的摩尔体积都是 22.4 L
B. 1 mol 气体的体积若是 22.4 L,它必定处于标准状况
C. 两种气体的物质的量之比等于其原子个数比
D. 标准状况下,1 mol H2 和 O2 的混合气体的体积约是 22.4 L
难度: 中等查看答案及解析
-
下列实验操作中,不是从人身安全因素考虑的是( )
A. 酒精灯不使用时,必须盖上灯帽
B. 给试管里的固体加热时,试管口应略向下倾斜,外壁干燥后再加热
C. 给试管里的液体加热时,试管口略向上倾斜(约45°),外壁干燥后再加热
D. 用H2还原CuO时,应先通一会儿H2,再加热CuO
难度: 简单查看答案及解析
-
下列混合物的分离方法不可行的是
A. 互溶的液体混合物可以用分液的方法进行分离
B. 互不相溶的液体混合物可以用分液的方法进行分离
C. 沸点不同的混合物可以用蒸馏的方法进行分离
D. 可溶于水的固体与难溶于水的固体的混合物可用溶解、过滤的方法进行分离
难度: 中等查看答案及解析
-
下列各叙述正确的是( )
A. 3 mol OH-的质量为 51 g B. 铁的摩尔质量等于它的相对原子质量
C. 一个碳原子的实际质量约等于 12/6.02×1023g D. 二氧化碳的摩尔质量是 44 g
难度: 简单查看答案及解析
-
下列溶液中的 c(Cl-)与 50 mL 1 mol·L-1 AlCl3 溶液中 c(Cl-)相等的是( )
A. 150 mL 1 mol·L-1NaCl 溶液 B. 75 mL 3mol·L-1NH4Cl 溶液
C. 150 mL 1 mol·L-1KCl 溶液 D. 75 mL 3mol·L-1AlCl3溶液
难度: 简单查看答案及解析
-
下图是海水蒸馏的装置示意图,下列有关海水蒸馏的叙述正确的是( )
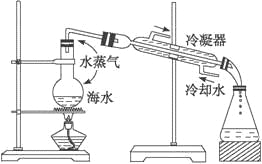
A. 本装置缺少温度计,所以无法进行海水蒸馏
B. 海水经过本装置的蒸镏后,锥形瓶中得到的是淡水
C. 装置中冷凝器中水流的方向不对,应该为上口进水,下口出水,便于水流下
D. 海水蒸馏前无须加入沸石
难度: 中等查看答案及解析
-
体积相同的甲、乙两容器,一个充满 CO,另一个充满 N2 和 C2H4 的混合气体。同温同压下,两容器内气体一定具有相同的
A. 原子总数和分子总数 B. 分子总数和质量
C. 电子总数和密度 D. 质子总数和电子总数
难度: 中等查看答案及解析