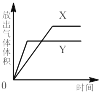
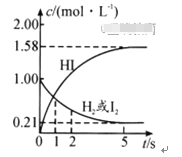
-
据《参考消息》报道,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点。
(1)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)===SiO2(s) ΔH=-989.2 kJ·mol-1,有关键能数据如下表:
化学键
Si—O
O===O
Si—Si
键能/kJ·mol-1
x
498.8
176
已知1 mol Si中含2 mol Si—Si键,1 mol SiO2中含4 mol Si—O键,则x的值为____________。
(2)硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等。硅光电池是一种把________能转化为________能的装置。
(3)假如硅作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法中,你认为不妥当的是_________________________________________。
A.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料
B.硅的来源丰富,易于开采,且可再生
C.硅燃烧放出的热量大,且燃烧产物对环境污染程度低,容易有效控制
D.寻找高效新催化剂,使硅的生产耗能很低,是硅能源开发利用的关键技术
(4)工业制备纯硅的反应为2H2(g)+SiCl4(g)===Si(s)+4HCl(g) ΔH=+240.4 kJ·mol-1,生成的HCl通入100 mL 1 mol·L-1的NaOH溶液恰好反应,则反应过程中________(填“吸收”或“释放”)的热量为________kJ。
难度: 困难查看答案及解析
-
根据要求回答下列问题:
①
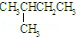 和
和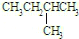 ②
②和
③CH4和CH3CH2CH3 ④金刚石和石墨 ⑤H、D、T ⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3)⑦臭氧(O3)和氧气(O2)⑧
和
⑨
和
⑩CuSO4•5H2O与CuSO4•3H2O
(1)这10组物质中,是同素异形体的是_____(填序号,下同);是同位素的是_____;是同分异构体的是_____;是同一物质的是_____;是同系物的是_____。
(2)写出支链只有一个乙基且相分子质量最小的烷烃的结构简式___________________________。
(3)一定量的稀硫酸和稀NaOH溶液反应,当生成1molH2O时放出的热量为57.3kJ,则中和热的热化学方程式为_____________________________________________________________________。
(4)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是__________。
A.C(s)+H2O(g)═CO(g)+H2(g)△H>0
B.2H2(g)+O2(g)=2H2O(l)△H<0
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H<0.
难度: 中等查看答案及解析
-
KI溶液在酸性条件下能与氧气反应。现有以下实验记录:
实验编号
①
②
③
④
⑤
温度/℃
30
40
50
60
70
显色时间/s
160
80
40
20
10
回答下列问题:
(1)该反应的离子方程式为_____________________________。
(2)该实验的目的是____________________________________。
(3)实验试剂除了1 mol·L-1 KI溶液、0.1 mol·L-1 H2SO4溶液外,还需要的试剂是________,实验现象为________________________。
(4)上述实验操作中除了需要(3)的条件外,还必须控制不变的是________(填字母)。
A.温度
B.试剂的浓度
C.试剂的用量(体积)
D.试剂添加的顺序
(5)由上述实验记录可得出的结论是____________________________________________________。
(6)若要进行酸性对反应速率的影响的探究实验,你会采取的措施是_____________。
难度: 中等查看答案及解析

 B.
B. 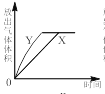 C.
C. 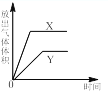 D.
D.