-
对下列各组物质:①NaNO3和NaCl;②CaCl2和CaCO3;③MnO2和KCl;④BaSO4和AgCl。可按照溶解、过滤、蒸发的实验操作顺序,将它们相互分离的是
A. 只有① B. ③④ C. ②③ D. ②④
难度: 简单查看答案及解析
-
欲配制100ml 1.0 mol/L Na2SO4溶液,正确的方法是( )
①将14.2 g Na2SO4 溶于100ml水中
②将32.2g Na2SO4·10H2O溶于少量水中,再用水稀释至100 ml
③将20 ml 5.0 mol/L Na2SO4溶液用水稀释至100 ml
A. ①② B. ②③ C. ①③ D. ①②③
难度: 简单查看答案及解析
-
下列对实验过程的评价正确的是( )
A. 某固体中加入稀盐酸,产生了无色气体,证明该固体一定是CaCO3
B. 某溶液中滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含SO42—
C. 某无色溶液滴入无色酚酞试液显红色,该溶液一定显碱性
D. 验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明含Cl-
难度: 简单查看答案及解析
-
我国明代《本草纲目》中收载药物1892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”这里所用的“法”是指( )
A. 萃取 B. 渗析 C. 蒸馏 D. 干馏
难度: 简单查看答案及解析
-
化学是以实验为基础的学科,化学实验设计和操作中必须十分重视安全问题和环境保护问题。下列操作不是围绕上述问题的是 ( )
A. 用氯酸钾和二氧化锰制氧气时用排水法收集后,应从水中撤出导管后再停止加热
B. 在氢气还原氧化铜停止加热后,还要继续通一会儿氢气
C. 实验室制备CO气体必须在通风橱中进行
D. 一些有机溶剂极易被引燃,使用时必须远离明火和热源,用毕立即塞紧瓶塞
难度: 简单查看答案及解析
-
下列危险化学品标志中最适合用于酒精的是
A.
 B.
B.  C.
C. D.
难度: 简单查看答案及解析
-
下列仪器:①烧杯;②锥形瓶;③圆底烧瓶;④试管;⑤坩埚;其中可以用酒精灯直接加热的仪器是( )
A. ①②③④ B. ④⑤ C. ①③ D. ④
难度: 简单查看答案及解析
-
完成下列实验所需选择的装置或仪器都正确的是
A. 分离植物油和氯化钠溶液

B. 除去氯化钠晶体中混有的氯化铵晶体
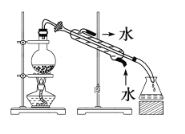
C. 分离CCl4中的Br2
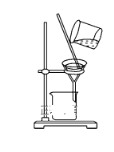
D. 除去CO2气体中的HCl气体

难度: 中等查看答案及解析
-
如图在盛有溴水的三支试管中分别加入酒精、四氯化碳和苯,振荡后静置,出现下列现象,正确的结论是
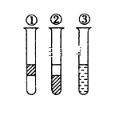
A. ①加了CCl4 ②加了苯 ③加了酒精
B. ①加了苯 ②加了CCl4 ③加了酒精
C. ①加了酒精 ②加了CCl4 ③加了苯
D. ①加了苯 ②加了酒精 ③加了CCl4
难度: 简单查看答案及解析
-
标准状况下,现有①6.72 L CH4 ②3.011023个HCl分子 ③13.6 g H2S ④0.2 mol NH3,对这四种气体的关系有以下四种表述,其中不正确的是
A. 氢原子个数:①>③>④>② B. 质量:②>③>①>④
C. 物质的量:②>③>④>① D. 体积:②>③>①>④
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A. 标准状况下,11.2 L水中含有的分子数是0.5NA
B. 常温常压下,5.6 g乙烯(C2H4)与丁烯(C4H8)的混合物中含有的氢原子的数目为0.8NA
C. 1 mol OH− 中含有质子数为10NA
D. 1 mol/L BaCl2溶液中含有的氯离子数为2NA
难度: 中等查看答案及解析
-
273K、101kPa下,2.8g N2、1.6g O2和2g Ar混合气体的密度是
A. 1.43 g/L B. 1.83 g/L
C. 1.83 mg/L D. 1.43 mg/L
难度: 中等查看答案及解析
-
将2mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度为
A. 2a/b mol/L B. 10a/b mol/L C. 5a/b mol/L D. 4a/b mol/L
难度: 简单查看答案及解析
-
下雪时,常用融雪剂清理路面,醋酸钾(CH3COOK)是效果较好的融雪剂.下列关于1molCH3COOK的叙述正确的是
A. 1 mol CH3COOK含有1 mol钾元素 B. CH3COOK的摩尔质量为98 g
C. 1molCH3COOK含有2 mol氧 D. 1molCH3COOK约含有36.021023个H
难度: 中等查看答案及解析
-
标准状况下a L氨气溶解在1 L水中(水的密度近似为1g/mL),所得溶液的密度为ρ=b g/mL,质量分数为w,物质的量浓度为c mol/L,则下列关系中不正确的是
A. b=(17a+22 400)/(22.4+22.4a) B. w=17c/(1 000b)
C. w=17a/(17a+22 400) D. c=1 000ab/(17a+22 400)
难度: 中等查看答案及解析
-
同温同压下,由N2O和CO2组成的混合气体的密度是C2H4、N2和H2组成的混合气体密度的 2倍,则C2H4、N2和H2组成的混合气体中H2的质量分数为
A. 3/13 B. 10/13 C. 大于3/13,小于10/13 D. 3/143
难度: 困难查看答案及解析


