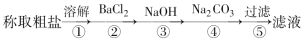
-
实验室中需要2 mol·L-1的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是
A. 950 mL,111.2 g B. 500 mL,117 g
C. 1 000 mL,117 g D. 任意规格,111.2 g
难度: 中等查看答案及解析
-
下列有关实验操作中,正确的是
A. 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
B. Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道
C. 用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干
D. 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
难度: 简单查看答案及解析
-
下列一定量的各物质所含原子个数按由大到小的顺序排列的是
①0.5 mol氨气 ②标准状况下22.4 L氦气 ③4 ℃时9 mL水 ④0.2 mol磷酸(H3PO4)
A. ①④③② B. ④③②① C. ②③④① D. ①④②③
难度: 中等查看答案及解析
-
下列实验操作正确的是
A. 当某实验没有准确的药品用量说明时,为看到明显现象,取用药品越多越好
B. 取用细口瓶里的试液时,先拿下瓶塞,倒放在桌上,然后标签朝外拿起瓶子,瓶口要紧挨着试管口,将液体缓缓地倒入试管
C. 胶头滴管取完一种试液后,可直接取另一种不与其反应的试液
D. 取用粉末状固体或固体小颗粒时,应用药匙或纸槽,取用块状固体时,应用镊子夹取
难度: 简单查看答案及解析
-
中国食盐产量居世界首位。下列实验室中的操作类似“海水晒盐”原理的是( )
A. 蒸馏 B. 蒸发
C. 过滤 D. 搅拌
难度: 简单查看答案及解析
-
下列有关仪器的使用正确的是
A. 手持试管给试管内的物质加热
B. 用燃着的酒精灯去点燃另一盏酒精灯
C. 用天平称量药品时用手直接拿砝码
D. 用滴管滴加液体时滴管应垂直悬垂在容器上方且不能触及容器内壁
难度: 简单查看答案及解析
-
在下列操作中,一般情况下不能相互接触的是
A. 过滤时,玻璃棒与三层滤纸
B. 分液时,分液漏斗下端与烧杯内壁
C. 过滤时,烧杯内壁与漏斗下端
D. 用胶头滴管向试管内滴加液体时,胶头滴管尖端与试管内壁
难度: 简单查看答案及解析
-
在下列物质分类中,前者包含后者的是( )
A. 氧化物、化合物 B. 化合物、电解质
C. 溶液、胶体 D. 溶液、分散系
难度: 简单查看答案及解析
-
以下实验装置一般不用于分离物质的是
A.
B.
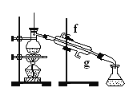 C.
C.  D.
D. 难度: 简单查看答案及解析
-
下列说法中不正确的是
A. 1 mol 氧气中含有1.2041024个氧原子,在标准状况下占有体积22.4 L
B. 1 mol臭氧和1.5 mol氧气含有相同的氧原子数
C. 1 mol任何气体的体积约为22.4L,一定是在标准状态下
D. 等物质的量的CO2和葡萄糖(C6H12O6)中所含碳原子数之比为1∶6,氧原子数之比1∶3
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数,下列说法正确的是 ( )
A. 1 mol氦气中有2NA个氦原子
B. 14 g氮气中含NA个氮原子
C. 2 L 0.3 mol·L-1Na2SO4溶液中含0.6 NA个Na+
D. 18 g水中所含的电子数为8NA
难度: 中等查看答案及解析
-
已知1.505×1023个X气体分子的质量为8 g,则X气体的摩尔质量是( )
A. 16 g B. 32 g C. 64 g/mol D. 32 g/mol
难度: 简单查看答案及解析
-
按照物质的树状分类和交叉分类,HNO3应属于
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤一元酸 ⑥强酸 ⑦化合物 ⑧混合物
A. ①④⑤⑥⑦ B. ①②③④⑤⑥⑦ C. ①②④⑧ D. ①④⑤⑥
难度: 简单查看答案及解析
-
下列分散系中的分散质的粒子大小属于纳米级(1~100 nm)的是
A. Fe(OH)3胶体 B. Fe(OH)3沉淀
C. FeCl3溶液 D. 碘水与CCl4溶液振荡后的混合液
难度: 中等查看答案及解析
-
下列溶液中,物质的量浓度最大的是
A. 1 L H2SO4溶液中含98 g H2SO4 B. 0.5 L含49 g H2SO4的溶液
C. 98 g H2SO4溶于水配成2 L溶液 D. 0.1 L含24.5 g H2SO4的溶液
难度: 简单查看答案及解析
-
下列叙述中,正确的是
A. H2SO4的摩尔质量是98
B. 等质量的O2和O3中所含的氧原子数相同
C. 等质量的CO与CO2中所含碳原子数之比为1︰1
D. 将98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol/L
难度: 简单查看答案及解析