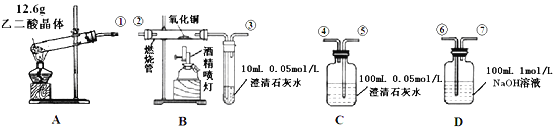
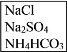-
使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②有些固体溶解会放热,若未经冷却即转移至容量瓶
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,仰视容量瓶的刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
A. ①③⑤⑥ B. ①②⑤⑥ C. ②③④⑥ D. ③④⑤⑥
难度: 简单查看答案及解析
-
下列有关铁与水反应的说法中正确的是( )
A. 在任何条件下,铁与水均能发生反应
B. 在高温时,铁与水蒸气反应生成氢氧化铁和氢气
C. 在高温时,铁与水蒸气反应生成氧化铁和氢气
D. 在高温时,铁与水蒸气反应生成四氧化三铁和氢气
难度: 简单查看答案及解析
-
今有下列三个氧化还原反应:①2FeCl3+2KI = 2FeCl2+2KCl+I2 ②2FeCl2+Cl2 = 2FeCl3 ③2KMnO4+16HCl(浓) =2KCl+2MnCl2+8H2O+5Cl2↑。若某溶液中有Fe2+和I—共存,要氧化除去I—而又不影响Fe2+,可加入的试剂是
A. Cl2 B. KMnO4 C. FeCl3 D. FeCl2
难度: 简单查看答案及解析
-
下列叙述正确的是( )
①Na在空气中放置最终变为NaOH ②Na在空气中燃烧,产物是Na2O
③将一块铝箔用砂纸打磨表面后,在酒精灯上加热至熔化但不滴落,说明Al2O3的熔点比铝高
④镁因在空气中形成了一层致密的氧化物薄膜,保护了里面的镁,故镁不像钠那样需要特殊的保护
⑤铝制品在生活中应用非常普遍,是因为铝不活泼
⑥铁在潮湿的空气中生成的氧化物不致密,不能保护内层金属,故铁制品往往需涂保护层
⑦钠与水的反应中钠块熔成小球说明该反应为放热反应
A. ①③⑤⑥ B. ②③④ C. ①②④⑤ D. ③④⑥⑦
难度: 中等查看答案及解析
-
同温、同压下等质量的SO2气体和CO2气体,下列有关比较的叙述中,说法正确的是
①分子数比为11:16 ②密度比为11:16 ③体积比为16:11 ④原子个数为11:16
A. ①③ B. ①④ C. ②③ D. ②④
难度: 简单查看答案及解析
-
把V L含有MgS04和K2S04的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为
A.mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
难度: 简单查看答案及解析
-
以下关于化学实验中“先”与“后”的说法正确的是
①加热试管时,先均匀加热,后局部加热 ②做H2还原CuO实验时,先通H2,后加热CuO,反应完毕后,先撤酒精灯待试管冷却,后停止通H2 ③制取气体时,先检查装置气密性,后装药品 ④点燃可燃性气体如H2、CO等时,先检验气体纯度,后点燃 ⑤制取蒸馏水时,先通冷却水,后加热蒸馏烧瓶 ⑥进行分液操作时,先从上口倒出上层液体,后从通过下端活塞放出下层液体
A. ①②③④ B. ①②③④⑤ C. ①②③④⑥ D. 全部
难度: 困难查看答案及解析
-
在无色溶液中,能大量共存的离子组是( )
A. K+、Ca2+、CO32-、Cl- B. Na+、Cu2+、Br-、Ba2+
C. K+、MnO4-、NO3-、Na+ D. Na+、SO32-、SO42-、K+
难度: 简单查看答案及解析
-
在空气中,有下列反应发生:①N2+O2═2NO;②2NO+O2═2NO2;③3NO2+H2O═2HNO3+NO;④2SO2+O2═2SO3;⑤SO3+H2O═H2SO4;⑥SO2+H2O═H2SO3;⑦3O2═2O3.其中属于氧化还原反应的是
A. ①②③④ B. ①②③④⑦ C. ①②④⑦ D. ①②③④⑤⑥⑦
难度: 中等查看答案及解析
-
能正确表示下列化学反应的离子方程式的是( )
A. 石灰水与盐酸的反应 OH﹣+H+===H2O
B. 氧化铜与盐酸反应 O2﹣+2H+===H2O
C. 铜片插入硝酸银溶液中 Cu+Ag+===Cu2++Ag
D. 碳酸钙溶于醋酸中 CaCO3+2H+===Ca2++H2O+CO2↑
难度: 困难查看答案及解析
-
己知金属钾投入水中会发生剧烈反应,并有氢气生成。运输金属钾的包装箱应贴有的图标是( )
A. 易燃液体
 B. 遇湿易燃物品
B. 遇湿易燃物品
C. 氧化剂
 D. 腐蚀品
D. 腐蚀品
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数,下列叙述正确的是
A. 标准状况下,22.4LH2O含有的分子数为NA
B. 常温常压下,NA个CO2分子占有的体积为22.4L
C. 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA
D. 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为NA
难度: 困难查看答案及解析
-
下列叙述中正确的是 ( )
A. FeCl3溶液、Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是有没有丁达尔效应
B. 根据分散系的稳定性大小将混合物分为胶体、溶液和浊液
C. 胶体、分散系、混合物概念间的从属关系可用图表示
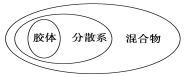
D. 将几滴汽油加入装有10mL水的试管中,用力振荡形成胶体
难度: 简单查看答案及解析
-
汽车尾气处理装置中可发生反应:4CO+2NO2
4CO2+N2,下列对该反应的说法正确的是
A. NO2被氧化 B. CO是氧化剂
C. 该条件下,氧化性CO2<NO2 D. 该条件下,还原性CO<N2
难度: 简单查看答案及解析
-
下列关于二氧化硅的叙述不正确的是( )
①在固态和液态时,导电性能都很差 ②能跟强碱反应,但不能与水反应
③硅与碳最外层都有4个电子,故SiO2的物理性质与CO2相似
④既不是酸性氧化物,又不是碱性氧化物。
A. ②和③ B. ③和④ C. ②和④ D. 只有④
难度: 中等查看答案及解析
-
世界著名的科技史专家、英国剑桥大学的李约瑟博士考证说:“中国至少在距今3000年以前,就已经使用玻璃了。”下列有关玻璃的说法不正确的是( )
A. 制普通玻璃的原料主要是纯碱、石灰石和石英砂
B. 玻璃在加热熔化时有固定的熔点
C. 普通玻璃的成分主要是硅酸钠、硅酸钙和二氧化硅
D. 盛放烧碱溶液的试剂瓶不能用玻璃塞,是为了防止烧碱跟二氧化硅生成硅酸钠而使瓶塞与瓶口粘在一起
难度: 简单查看答案及解析