-
在无土栽培中,需配制一定量含50 mol NH4Cl,16 mol KCl和24 mol K2SO4的营养液。若用KCl、NH4Cl和(NH4)2SO4三种固体为原料来配制,三者的物质的量依次是(单位为mol)
A. 2 ,64 ,24 B. 64 ,2 ,24 C. 32 ,50 ,12 D. 16 ,50 ,24
难度: 简单查看答案及解析
-
某氯化镁溶液的密度为1.18g/cm3,其中镁离子的质量分数为5.1%,300mL该溶液中Cl-离子的物质的量约等于( )
A. 0.37mol B. 0.63mol C. 0.74mol D. 1.5mol
难度: 中等查看答案及解析
-
偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力。下列叙述正确的是
A. 偏二甲肼的摩尔质量为60 g
B. 6.02×1023个偏二甲肼分子的质量约为60 g
C. 1 mol偏二甲肼的质量为60 g·mol-1
D. 6 g偏二甲肼含有NA个偏二甲肼分子
难度: 中等查看答案及解析
-
上海建成了我国第一条磁悬浮铁路。磁悬浮的核心技术是利用超导体的反磁性。高温超导物质(Y2Ba4Cu6O13)是以YmOn、BaO和CuO为原料,经研磨烧结而成,此过程中所有元素的化合价均不变,则高温超导物质(Y2Ba4Cu6O13)中Y元素的化合价是( )
A. +2 B. +3 C. +4 D. +5
难度: 简单查看答案及解析
-
合金具有许多优良的物理、化学或机械性能。下列物质不属于合金的是( )
A. 青铜 B. 金刚砂(SiC) C. 硬铝 D. 生铁
难度: 简单查看答案及解析
-
下列有关电解质的说法中正确的是
A. 液态氯化氢不导电,所以氯化氢不是电解质
B. 氨溶于水形成的溶液能导电,所以氨是电解质
C. 熔融的铜导电性很好,所以铜是电解质
D. 氧化钠、氧化钙熔融时能导电,所以氧化钠、氧化钙是电解质
难度: 简单查看答案及解析
-
标准状况下,两个容积相等的贮气瓶,一个装有O2,另一个装有CH4,两瓶气体具有相同的( )
A. 质量 B. 原子总数 C. 密度 D. 分子数
难度: 中等查看答案及解析
-
下列物质既能用作食品防腐剂,又能用作食品干燥剂的是( )
A. 烧碱 B. 生石灰 C. 氮气 D. 铁粉
难度: 简单查看答案及解析
-
下列变化中只有通过还原反应才能实现的是
A. Fe3+→Fe2+ B. Mn2+→
C. Cl-→Cl2 D. N2O3→HNO2
难度: 简单查看答案及解析
-
下列离子方程式正确的是( )
A. 氢氧化镁与稀盐酸反应:OH-+H+=H2O
B. 醋酸溶液与水垢中的碳酸钙反应:CaCO3+2H+=Ca2++H2O+CO2↑
C. 向碳酸氢钠溶液中滴加盐酸:CO32-+2H+=H2O+CO2↑
D. 向碳酸钠溶液中加过量盐酸:CO32-+2H+=H2O+CO2↑
难度: 简单查看答案及解析
-
下列各组溶液,只要用试管和胶头滴管,不用任何化学试剂就可以鉴别的是
A. HCl和Na2CO3 B. 稀H2SO4和NaHCO3
C. CaCl2和Na2CO3 D. Ba(OH)2和NaHSO4
难度: 中等查看答案及解析
-
能正确表示下列化学反应的离子方程式的是( )
A. 碳酸钙溶于稀盐酸中:CaCO3+2H+=H2O+CO2↑+Ca2+
B. 澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O
C. NaHCO3溶液与NaOH溶液反应:OH﹣+HCO3-=CO2↑+H2O
D. 氢氧化镁与盐酸的反应:OH﹣+H+=H2O
难度: 简单查看答案及解析
-
下列分散系中,分散质微粒直径介于10-9—10-7m (l—100nm)之间的是
A. 溶液 B. 胶体 C. 悬浊液 D. 乳浊液
难度: 简单查看答案及解析
-
某化学兴趣小组利用MnO2和浓HCl及如图装置制备Cl2。下列分析中不正确的是 ( )。
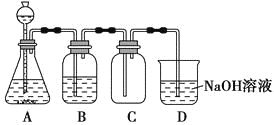
A. A中可用分液漏斗代替长颈漏斗
B. A中缺少加热装置
C. B中盛放的NaOH溶液可以净化Cl2
D. D中的导管口若连接倒置漏斗可防止倒吸
难度: 中等查看答案及解析
-
将12.4克氧化钠溶于87.6克水中,所得溶液溶质的质量分数是( )
A. 8.0% B. 12.4% C. 16% D. 32%
难度: 简单查看答案及解析
-
某无色溶液放入铝片后有氢气产生,下列离子在该溶液中一定不能大量存在的是( )
A. SO42- B. Cu2+ C. K+ D. OH-
难度: 简单查看答案及解析
-
不能使淀粉碘化钾溶液变蓝的是( )
A. 食盐水 B. 氯水 C. 氯化铁溶液 D. 碘水
难度: 简单查看答案及解析
-
下列关于二氧化硅的说法错误的是( )
A. 二氧化硅是一种非金属氧化物
B. 二氧化硅不存在单个的分子
C. 二氧化硅中硅元素与氧元素的质量比为7∶8
D. 二氧化硅分子由一个硅原子和两个氧原子构成
难度: 简单查看答案及解析
-
等质量的甲、乙、丙三种金属,分别与足量的溶质质量分数相同的稀硫酸完全反应后,都生成+2价的硫酸盐,其产生氢气的体积与反应时间的关系如图所示,则下列说法正确的是
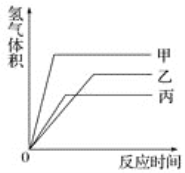
A. 三种金属的活动性顺序为甲>乙>丙
B. 反应结束消耗硫酸的质量一定相同
C. 三种金属的相对原子质量是甲>乙>丙
D. 甲先反应完,乙最后反应完
难度: 中等查看答案及解析
-
下列说法正确的是
A. 用澄清石灰水可以鉴别碳酸钠和碳酸氢钠
B. 新制氯水经光照一段时间pH减小
C. 自然界硅元素贮量丰富,并存在大量的单质硅
D. 等质量的碳酸钠与碳酸氢钠分别与足量盐酸反应,产生二氧化碳质量相同
难度: 简单查看答案及解析
-
黄铜是合金,它是( )
A. 铜的化合物 B. 含铜的混合物
C. 铜的氧化物 D. 铜单质
难度: 简单查看答案及解析
-
下列变化不可能通过一步反应直接完成的是( )
A. Al→AlO2- B. Al2O3→Al(OH)3
C. Al(OH)3→Al2O3 D. Al3+→AlO2-
难度: 简单查看答案及解析
-
石英的主要化学成分是( )
A. 硅酸钠 B. 氧化铝 C. 二氧化硅 D. 单质硅
难度: 简单查看答案及解析
-
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3物质的量浓度分别是4mol/L和2mol/L,取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体为( )
A. 2.24L B. 1.12L C. 0.672L D. 0.448L
难度: 中等查看答案及解析
-
将1molNa和1molAl的混合物投入足量水中,产生气体在标准状况下的体积为 ( )
A. 11.2L B. 22.4L C. 33.6L D. 44.8L
难度: 中等查看答案及解析
-
工业上利用合成氨实现人工固氮。属于合成氨主要原料的是( )
A. 二氧化氮 B. 空气 C. 碳酸钠 D. 硝酸钾
难度: 简单查看答案及解析