-
当钠、钾等金属不慎着火时,可以用来灭火的是:( )
A. 水 B. 煤油 C. 沙子 D. 泡沫灭火剂
-
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3
+H2C2O4+H2SO4 =2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法正确的是( )
A. KClO3在反应中得到电子 B. ClO2是氧化产物
C. H2C2O4在反应中被还原 D. 1mol KClO3参加反应有2 mol电子转移
-
下列说法中正确的是( )
A. 摩尔是国际单位制中的七个物理量之一 B. 0.5 mol H2O中含有的原子数目为1.5NA
C. 64 g氧相当于2 mol氧 D. 1 mol任何物质都约含有6.02×1023个原子
-
下列事实与胶体的性质无关的是( )
A. 在豆浆中加入盐卤做豆腐
B. 在河流入海处易形成沙洲
C. 一束平行光线照射蛋白质溶液时,从侧面可以看到一束光亮的通路
D. FeCl3 溶液中滴入氢氧化钠溶液出现红褐色沉淀
-
在实验室中,通常将金属钠保存在( )
A. 水中 B. 煤油中 C. 四氯化碳中 D. 汽油中
-
下列各组物质,按单质、化合物、混合物的顺序排列的是( )
A. 液态氧、烧碱、碘酒 B. 空气、氮气、胆矾
C. 干冰、铁、氯化氢 D. 生石灰、白磷、熟石灰
-
2013年1月3日晨,昆明长水国际机场出现大雾天气,导致大量航班延误。雾属于下列哪种分散系( )
A. 乳浊液 B. 溶液 C. 悬浊液 D. 胶体
-
下列说法正确的是( )
A. 常温常压下,22.4 L CO2中含有NA个CO2分子
B. 标况下22.4 L空气含有NA个单质分子
C. 22.4 L Cl2中含有NA个Cl2分子
D. 标况下1.12L O2和1.12L CO2均含有0.1NA个氧原子
-
金属钠在空气中燃烧,生成物是( )
A. 氧化钠 B. 过氧化钠 C. 氢氧化钠 D. 碳酸钠
-
下列离子方程式中,正确的是( )
A. 稀硫酸滴在铜片上:Cu+2H+ =Cu2+ +H2O
B. 铜片插入硝酸银溶液中:Cu+Ag+ =Cu2++Ag
C. 氧化镁与稀盐酸混合:MgO+2H+=Mg2+ +H2O
D. 稀硝酸滴在石灰石上:CaCO3+2H+ =Ca2++H2CO3
-
下列各组中的离子,能在溶液中大量共存的是( )
A. Na+、Cu2+、Cl-、SO42- B. Na+、Ca2+、CO32-、NO3-
C. Na+、H+、Cl-、CO32- D. K+、H+、SO42-、OH-
-
下列关于钠的叙述中,不正确的是( )
A. 钠燃烧时发出黄色的火焰 B. 钠燃烧时生成氧化钠
C. 钠有很强的还原性 D. 钠原子的最外层只有一个电子
-
下列关于Na和Na+的叙述中,错误的是( )
A. 它们相差一个电子层 B. 钠原子、钠离子均为同一元素
C. 它们的化学性质相似 D. 灼烧时,它们的焰色反应都呈黄色
-
下列化学反应既是化合反应,又是氧化还原反应的是( )
A. 氧化钙溶于水 B. 氢气还原氧化铜
C. 红磷在氧气中燃烧 D. 盐酸与氢氧化钠
-
少量的金属钠长期暴露在空气中,它的最终产物是 ( )
A. NaOH B. Na2CO3•10H2O C. NaHCO3 D. Na2CO3
-
在反应2KMnO4 = K2MnO4 + MnO2 + O2↑中,氧化产物是( )
A. K2MnO4 B. MnO2 C. KMnO4 D. O2
-
下列化学变化中,物质发生氧化反应的是( )
A. C→CO2 B. CO2→ CO C. CuO→Cu D. H2SO4→BaSO4
-
下列离子中,氧化能力最强的是( )
A. Fe3+ B. Cu2+ C. H+ D. Fe2+
-
下列变化需加入还原剂的是 ( )
A. HCO3-→CO2 B. MnO4-→Mn2+ C. FeO→Fe3O4 D. H3AlO3→HAlO2
-
根据反应式:⑴2Fe3+ + 2I- = 2Fe2+ + I2 ⑵Br2 + 2Fe2+ = 2Br- + 2Fe3+可判断离子的还原性由强到弱的顺序是( )
A. Br-、Fe2+、I- B. Br-、I-、Fe2+ C. I-、Fe2+、Br- D. Fe2+、I-、Br-
-
下列化学反应中,水既不是氧化剂又不是还原剂的是( )
A. 2Na2O2+2H2O===4NaOH+O2↑
B. 2F2+2H2O===4HF+O2
C. 2Na+2H2O===2NaOH+H2↑
D. NaH+H2O===NaOH+H2↑
-
下列离子方程式正确的是( )
A. 钠与水的反应:Na+2H2O=Na++H2↑+2OH-
B. NaHCO3与盐酸的反应:CO32-+2H+=CO2↑+H2O
C. Na2O2与水的反应: 2O22-+2H2O=4OH-+O2↑
D. NaHCO3与氢氧化钠的反应: HCO3-+OH-=CO32-+H2O
-
已知在酸性溶液中的还原性强弱顺序为:SO2 >I– >H2O2> Fe2+>Cl–,下列反应不可能发生的是( )
A. H2O2+ H2SO4 = SO2↑+ O2↑+2H2O B. 2I– +2Fe3+= I2+2Fe2+
C. 2Fe3++ SO2 +2H2O= 2Fe2++SO42– +4H+ D. SO2 +2H2O+ I2= H2SO4+2HI
-
下列物质属于电解质的一组是( )
A. CO2、NH3、HCl B. 液态KNO3、NaOH溶液、C2H5OH
C. H3PO4、H2O、Cu D. H2SO4、HNO3、BaCl2
-
下列离子在无色溶液中能大量共存的是( )
A. Fe3+、NH4+、OH-、Cl- B. Na+、H+、NO3-、SO42-
C. Fe2+、Fe3+、Na+、NO3- D. Fe2+、NH4+、Cl-、OH-
-
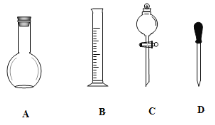
用已准确称量过的氯化钠固体配制1.00 mol·L-1的氯化钠溶液0.5 L,要用到的仪器是( )
①500 mL容量瓶 ②试管 ③烧瓶 ④胶头滴管 ⑤烧杯 ⑥玻璃棒 ⑦托盘天平 ⑧药匙
A. ①④⑤⑥⑦⑧ B. ①②④⑤ C. ①④⑤⑥ D. 全部
-
下列描述的一定是金属元素的是
A. 易失去电子的物质 B. 能与酸反应的物质
C. 原子最外电子层只有一个电子的元素 D. 原子核内有11个质子的元素
-
5.4gAl放入足量氢氧化钠溶液中完全反应,生成氢气的体积(标准状况下)是( )
A. 6.72L B. 3.36L C. 1.12L D. 2.24L
-
只能表示一个化学反应的离子方程式为 ( )
①CaCO3+2H+=Ca2++CO2↑+H2O
②Ba2++2OH-+2NH4++CO32-=2H2O+2NH3↑+BaCO3↓
③Ag++Cl-=AgCl↓
④Fe+Cu2+=Fe2++Cu
⑤SO2+Cl2+H2O=4H++2Cl-+SO42-
A. ①⑤ B. ②⑤ C. ③⑤ D. ④⑤
-
下列各组物质相互混合反应,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液 ②过量NaOH溶液和KAl(SO4)2溶液
③Ba(HCO3)2溶液和NaHSO4溶液 ④NaHCO3投入Ca(OH)2溶液
A. ①④ B. ②③④ C. ①③ D. ②③
2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为____________mol。